Clear Sky Science · it
INCENP e CDCA8 predicono la risposta alla chemioterapia neoadiuvante e gli esiti nel carcinoma squamocellulare esofageo
Perché questa ricerca è importante per i pazienti oncologici
Molte persone con tumori dell’esofago, della mammella o del polmone ricevono chemioterapia intensiva prima dell’intervento chirurgico per ridurre le dimensioni dei tumori. Tuttavia solo circa la metà di questi pazienti ottiene un reale beneficio; per gli altri i farmaci provocano effetti collaterali senza fermare il cancro. Questo studio pone una domanda semplice ma cruciale: è possibile prevedere in anticipo chi risponderà alla chemioterapia e migliorare il trattamento per chi oggi non risponde?
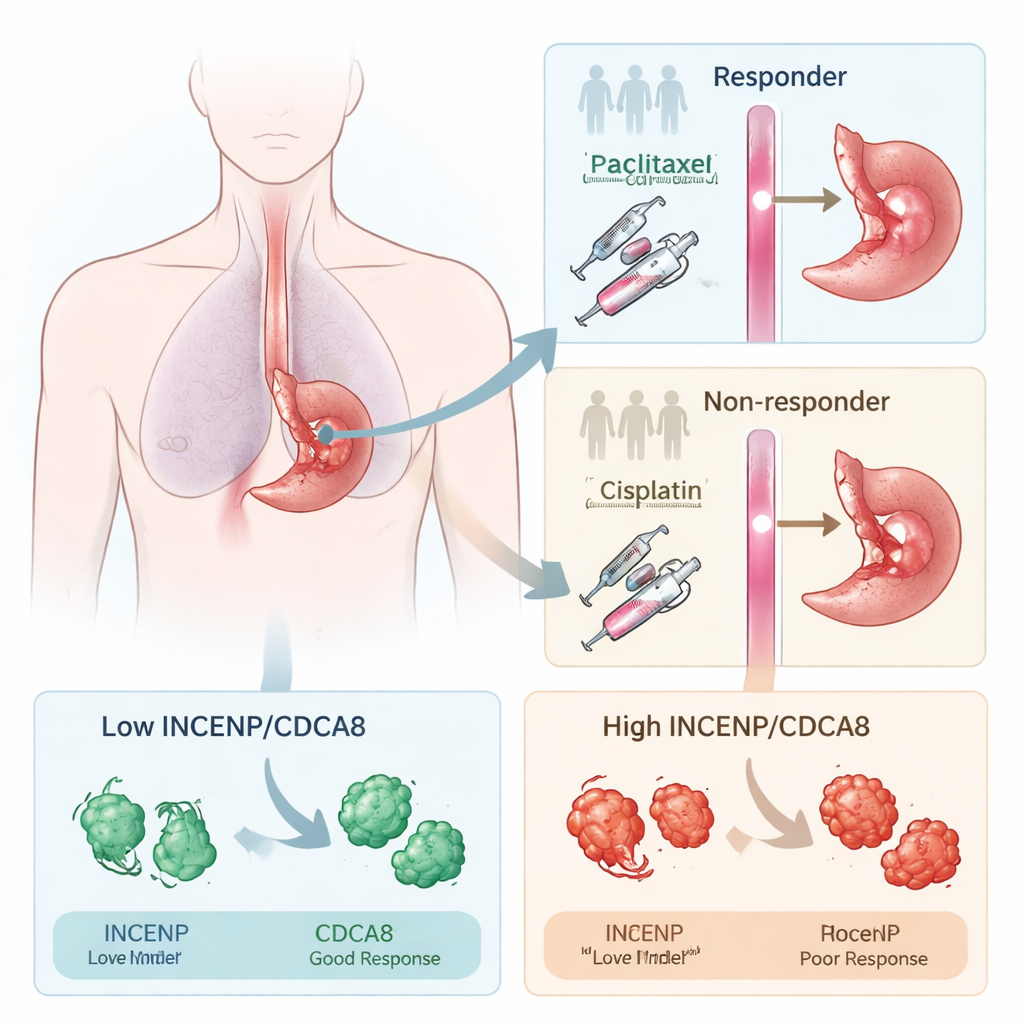
Individuare chi risponde al trattamento
I ricercatori si sono concentrati su un regime preoperatorio standard che combina paclitaxel e cisplatino, ampiamente usato in diversi tumori. Lavorando inizialmente con pazienti affetti da carcinoma squamocellulare esofageo, hanno confrontato campioni tumorali di persone i cui tumori si sono ridotti notevolmente dopo la terapia (responder) con campioni di chi ha avuto scarsa risposta (non-responder). Analizzando quali geni erano attivati o soppressi, hanno rilevato che molte differenze riguardavano la divisione cellulare, un processo che la chemioterapia mira a interrompere. Due proteine che contribuiscono al controllo della separazione dei cromosomi durante la divisione cellulare, INCENP e CDCA8, sono emerse ripetutamente come molto più elevate nei tumori resistenti al trattamento.
Due proteine che segnalano probabilità di resistenza
Per verificare se INCENP e CDCA8 fossero meri osservatori o fattori attivi della resistenza, il team ha modificato i loro livelli in cellule di cancro esofageo coltivate in laboratorio. Riducendo ciascuna delle due proteine, le cellule tumorali sono diventate molto più sensibili a paclitaxel e cisplatino, formando meno colonie e richiedendo dosi di farmaco molto inferiori per essere uccise. Forzando invece l’espressione aumentata di INCENP o CDCA8, si è osservato l’effetto opposto: i farmaci diventavano meno efficaci. In topi impiantati con tumori esofagei umani, l’abbattimento di queste proteine ha reso la chemioterapia più efficace nello ridurre i tumori. Anche nei pazienti i tumori con alti livelli di INCENP e CDCA8 prima del trattamento erano associati a progressione di malattia e sopravvivenza più breve, rafforzando il loro valore come segnali di allarme.
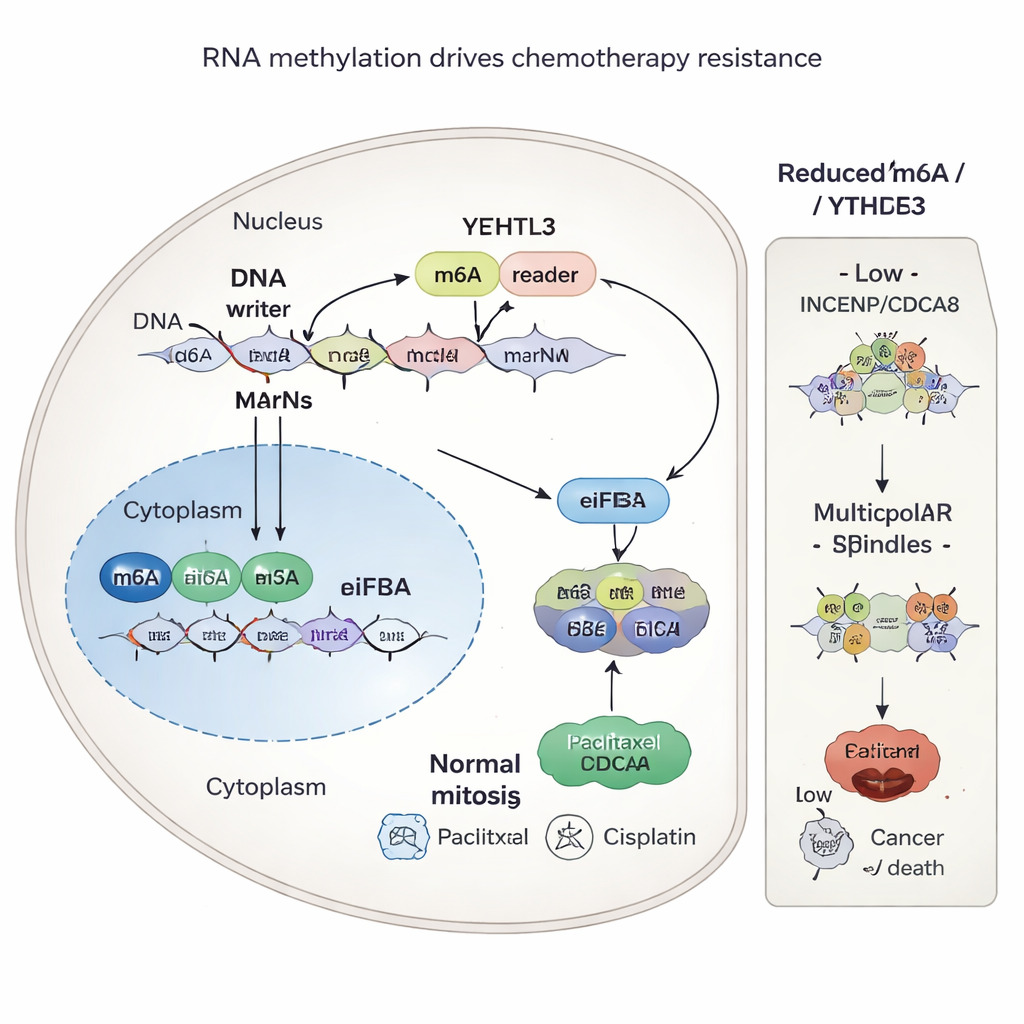
Un marchio chimico sull’RNA che alimenta la resistenza
Lo studio ha poi cercato di capire perché INCENP e CDCA8 fossero così abbondanti nei tumori resistenti. La risposta risaliva a un sottile segno chimico sull’RNA chiamato m6A, che funziona come una manopola per regolare l’efficienza con cui i messaggi genetici vengono tradotti in proteina. Un enzima, METTL3, aggiunge questi marchi m6A in punti specifici sui trascritti di INCENP e CDCA8. Un’altra proteina, YTHDF3, riconosce i marchi e contribuisce a reclutare la macchina proteica della cellula, aumentando la produzione delle due proteine. Quando gli scienziati hanno ridotto METTL3 o YTHDF3, o bloccato YTHDF3 con una piccola molecola chiamata Ebselen, i marchi m6A venivano persi o ignorati, i livelli proteici di INCENP e CDCA8 calavano e le cellule tumorali diventavano più vulnerabili alla chemioterapia.
Interferire con la divisione cellulare per aiutare la chemioterapia
INCENP e CDCA8 fanno parte di un complesso più ampio, il chromosomal passenger complex, che assicura la corretta distribuzione dei cromosomi alle cellule figlie. Nelle cellule resistenti, livelli elevati di queste proteine aiutano a mantenere fusi mitotici ordinati e bipolari durante la divisione, consentendo al tumore di sopravvivere al danno provocato da paclitaxel e cisplatino. Quando INCENP e CDCA8 vengono soppressi, le cellule spesso formano fusi difettosi a più poli. Questo caos nella segregazione dei cromosomi spinge le cellule tumorali verso la morte, amplificando il potere letale della chemioterapia. Fondamentale è che la capacità di INCENP e CDCA8 di proteggere le cellule dipendeva da specifici siti m6A nei loro RNA; mutare questi siti aboliva la resistenza.
Oltre un singolo tipo di tumore
Poiché la combinazione paclitaxel più cisplatino è usata anche per tumori polmonari e mammari, il gruppo ha esaminato anche campioni bioptici di pazienti con questi tumori. In tutti e tre i tipi di cancro, le persone i cui tumori presentavano livelli bassi di INCENP, CDCA8 e YTHDF3 prima della terapia avevano molte più probabilità di rispondere bene al trattamento. Analisi statistiche hanno mostrato che la combinazione di questi tre marcatori offre una buona capacità di distinguere i probabili responder dai non-responder, suggerendo un pannello di test pratico utilizzabile in più tipi di tumore.
Cosa significa per pazienti e medici
In termini concreti, questo lavoro identifica un “impronta” molecolare che aiuta a spiegare perché alcuni tumori resistono a chemioterapie potenti. Elevati livelli di INCENP e CDCA8, guidati da un sistema di controllo basato su m6A che coinvolge METTL3 e YTHDF3, mantengono le cellule tumorali in grado di dividersi correttamente anche sotto attacco farmacologico. Misurare queste proteine in una biopsia potrebbe aiutare i medici a prevedere se la combinazione paclitaxel più cisplatino è probabile che giovi a un paziente, risparmiando ad altri trattamenti inefficaci. Allo stesso tempo, farmaci che bloccano questa via potrebbero essere combinati con la chemioterapia standard per spingere i tumori resistenti verso errori letali nella divisione, potenzialmente migliorando la sopravvivenza per persone affette da diversi tumori rilevanti.
Citazione: Wang, X., Wang, T., Wang, K. et al. INCENP and CDCA8 predict neoadjuvant chemotherapy response and outcomes in esophageal squamous cell carcinoma. Nat Commun 17, 1672 (2026). https://doi.org/10.1038/s41467-026-68371-x
Parole chiave: chemioterapia neoadiuvante, carcinoma squamocellulare esofageo, resistenza alla chemioterapia, biomarcatori INCENP e CDCA8, metilazione RNA m6A