Clear Sky Science · it
Proteasi dipendenti da K48-ubiquitina tagliano le proteine post-RER
Come le cellule decidono quali proteine distruggere
Le nostre cellule rimuovono costantemente proteine usurate o danneggiate, in particolare quelle inserite nelle membrane che fungono da porte e sensori. Questo articolo rivela che le cellule usano un piccolo tag chiamato ubiquitina non semplicemente come un’etichetta generica di “rifiuto”, ma come un codice che indica alle proteine di membrana esattamente come verranno degradate. Capire questo codice aiuta a spiegare come le cellule mantengano l’omeostasi e può orientare future terapie che mirano a eliminare deliberatamente proteine causa di malattie.
Un codice a barre cellulare per lo smaltimento delle proteine
Le cellule decorano le proteine indesiderate con catene di una piccola proteina chiamata ubiquitina. Queste catene possono essere collegate in modi diversi, un po’ come perle infilate in fori differenti, e ogni schema può segnalare un esito diverso. Gli autori si sono concentrati su proteine di membrana che hanno già lasciato il reticolo endoplasmatico (RE) e transitano attraverso compartimenti come il Golgi e gli endosomi. Si sono chiesti se due tipi di catene comuni, dette legate in K48 e legate in K63, siano davvero etichette intercambiabili o se indirizzino il carico verso percorsi di degradazione distinti.
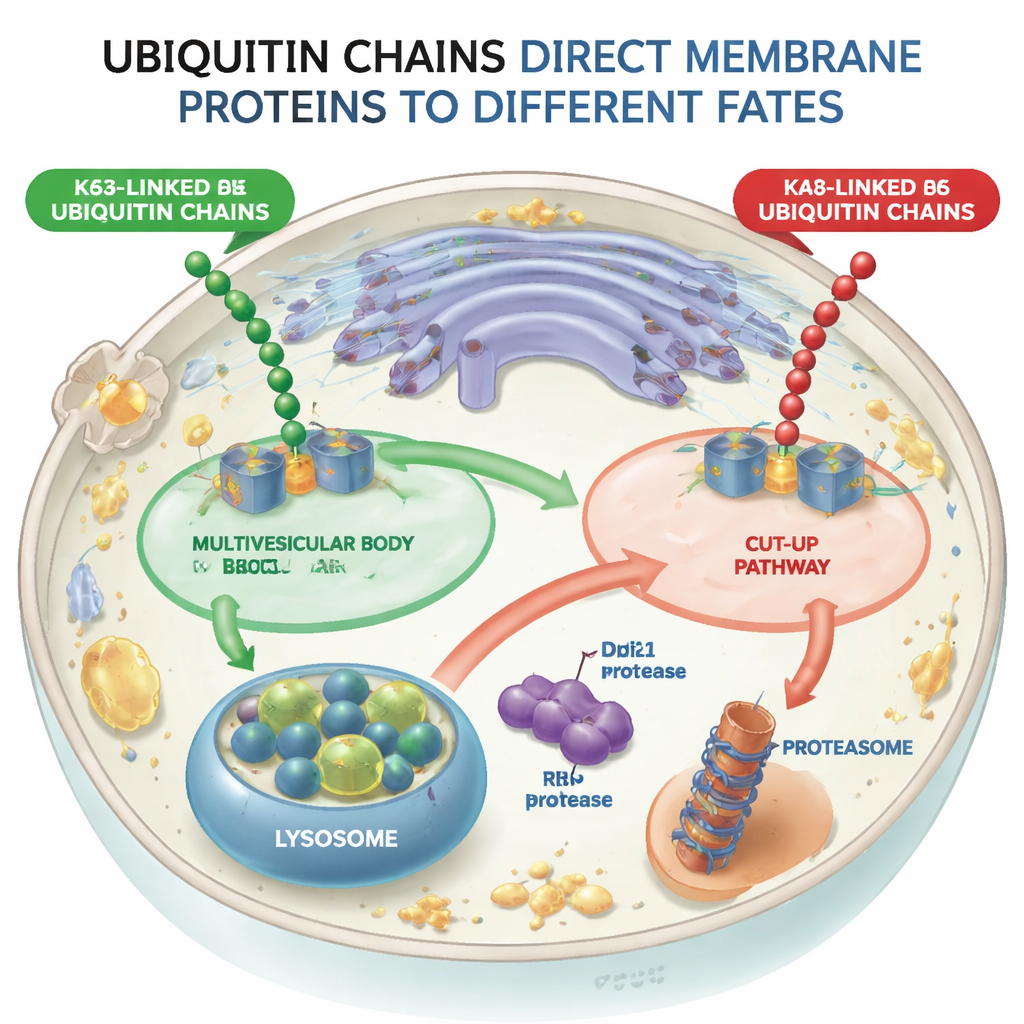
Due percorsi divergenti per le proteine taggate
Usando cellule di lievito come modello, i ricercatori hanno progettato macchine molecolari (ligasi dell’ubiquitina) in grado di attaccare o catene K48 o catene K63 alla stessa proteina di test di membrana, un recettore di smistamento chiamato Vps10. Quando Vps10 riceveva catene legate in K63, veniva inviato in vescicole interne all’interno degli endosomi — strutture note come corpi multivescicolari — che alla fine si fondono con i lisosomi, i compartimenti digestivi della cellula. Al contrario, quando Vps10 portava catene legate in K48, non seguiva questo percorso multivescicolare. Invece veniva smontato in modo completamente diverso, dimostrando che la cellula distingue tra questi due tipi di catene e che la via multivescicolare respinge efficacemente il carico marcato con K48.
Un percorso “cut-up” che taglia le proteine in due
Il gruppo ha scoperto che le catene legate in K48 attivano una via di cesoiamento delle proteine che chiamano CUT-UP, abbreviazione di Cleavage of Ubiquitinated Targets by Ubiquitin-dependent Proteases. Invece di estrarre l’intera proteina dalla membrana in una sola volta, CUT-UP la trancia in pezzi che vengono poi completati dai sistemi di smaltimento cellulare esistenti. Un enzima chiave, Ddi1, si trova nel citosol e taglia la porzione della proteina di membrana rivolta verso il citoplasma. Quel frammento viene poi digerito dal proteasoma, il principale trituratore proteico della cellula. Allo stesso tempo, un altro enzima, Rbd2, è integrato nella membrana stessa e tronca la parte della proteina rivolta verso il lume del compartimento, rilasciandola nello spazio che alla fine si collega al lisosoma. L’inibizione simultanea di Ddi1, Rbd2, del proteasoma e degli enzimi lisosomiali è risultata necessaria per proteggere completamente Vps10 marcato con K48 dalla degradazione, confermando che tutti questi componenti cooperano nella via CUT-UP.
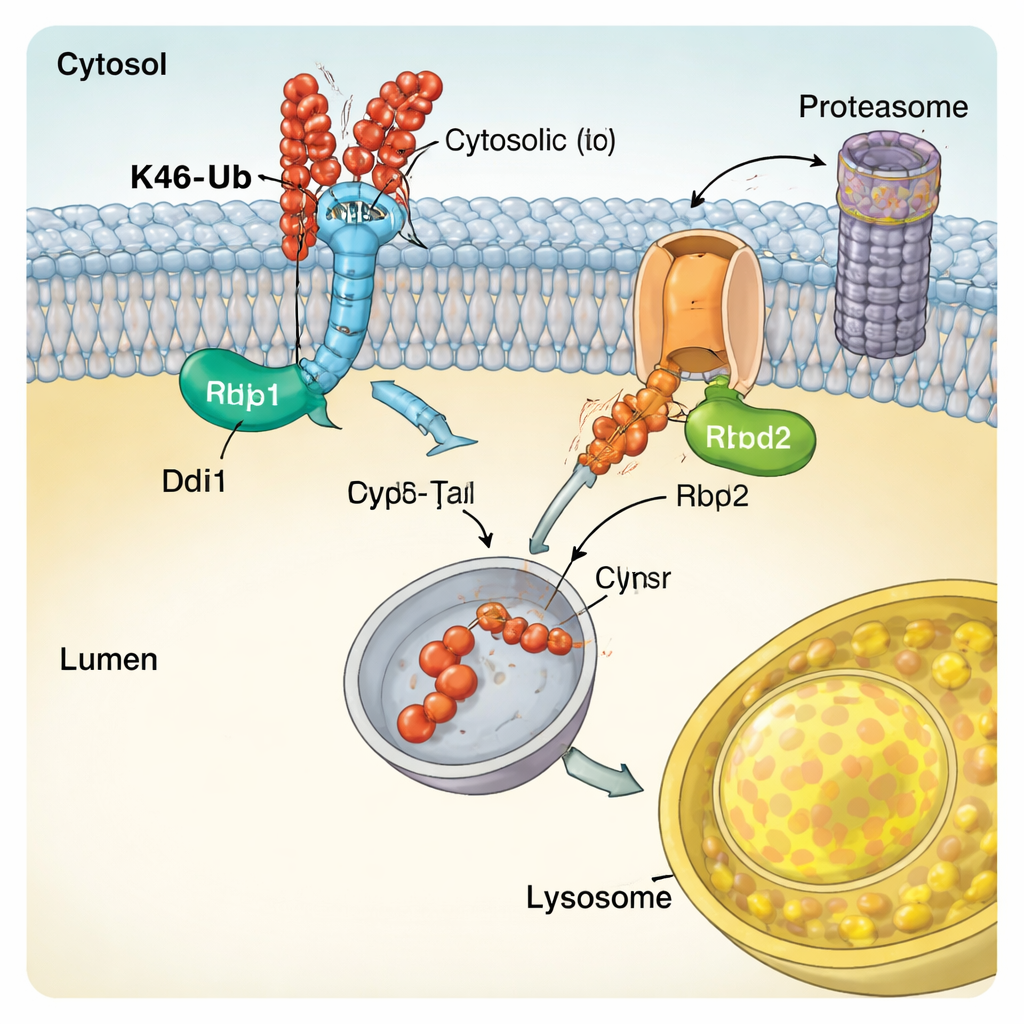
Enzimi specializzati che leggono il codice dell’ubiquitina
Per capire come CUT-UP riconosce i suoi bersagli, gli autori hanno esaminato le caratteristiche molecolari di Ddi1. Hanno mostrato che il nucleo catalitico centrale di Ddi1 non soltanto taglia le proteine, ma può anche legare direttamente l’ubiquitina, e che la sua attività è modulata da regioni aggiuntive che si agganciano alle catene di ubiquitina. Ddi1 ha mostrato una particolare dipendenza dalle catene legate in K48, coerente con il suo ruolo in CUT-UP. Rbd2, invece, è una proteasi romboide che attraversa la membrana. Lo studio ha rilevato che il sito attivo di Rbd2 è essenziale per tagliare le porzioni di Vps10 rivolte al lume e che l’enzima transita attraverso diversi compartimenti della via secretoria, permettendogli di agire in più localizzazioni cellulari. Enzimi simili esistono nelle cellule umane e sono stati implicati in condizioni che spaziano dalla neurodegenerazione al cancro, suggerendo che meccanismi simili a CUT-UP potrebbero avere una rilevanza estesa.
Perché questo conta per la salute e la terapia
Dimostrando che diversi tipi di catene di ubiquitina mandano la stessa proteina di membrana verso destini nettamente diversi — o lo smistamento nei corpi multivescicolari o il sezionamento mediato da CUT-UP — questo lavoro fornisce forti evidenze che le cellule usano un vero “codice dell’ubiquitina” per modulare con precisione lo smaltimento delle proteine. La scoperta di CUT-UP chiarisce come proteine di membrana ostinate possano essere smantellate pezzo per pezzo e mette in luce Ddi1 e Rbd2 come attori chiave che leggono e applicano questo codice. Per i non specialisti, il punto essenziale è che le cellule non si limitano a etichettare le proteine come immondizia; specificano come quella immondizia verrà rimossa. Quando gli sviluppatori di farmaci progettano strumenti che marcano le proteine dannose con ubiquitina per eliminarle, comprendere percorsi come CUT-UP sarà fondamentale per prevedere quali frammenti verranno prodotti e come ciò potrebbe influenzare il comportamento cellulare.
Citazione: Minard, A.Y., Winistorfer, S., Yu, L. et al. K48-ubiquitin-dependent proteases cut-up post-ER proteins. Nat Commun 17, 1669 (2026). https://doi.org/10.1038/s41467-026-68367-7
Parole chiave: codice dell'ubiquitina, degradazione delle proteine, proteine di membrana, proteasoma, lisosoma