Clear Sky Science · it
La perdita del quorum sensing Fsr favorisce la formazione di biofilm e peggiora l’esito nell’endocardite infettiva da enterococco
Sabotatori silenziosi sulle valvole cardiache
L’endocardite infettiva è un’infezione potenzialmente letale delle valvole cardiache, la cui incidenza sta aumentando a livello mondiale. Questo studio si concentra su un colpevole principale, il batterio intestinale Enterococcus faecalis, e si domanda perché alcune infezioni siano particolarmente difficili da curare. Scoprendo come questi batteri comunicano tra loro e costruiscono biofilm protettivi sulle valvole cardiache, i ricercatori spiegano perché alcuni ceppi scatenano malattie più gravi e resistono agli antibiotici, e perché un sistema di comunicazione batterica, chiamato Fsr, si rivela sorprendentemente un freno piuttosto che un acceleratore del danno.
Come i batteri edificano fortezze nel cuore
Le valvole cardiache normalmente sopportano alcuni dei flussi sanguigni più rapidi del corpo, ma se la superficie valvolare è danneggiata, piastrine e proteine della coagulazione possono formare un piccolo coagulo, o vegetazione. Questo coagulo diventa un punto d’atterraggio per i batteri in circolo nel sangue. Una volta aderiti, i batteri si moltiplicano e si intrecciano in un biofilm — una comunità viscosa e strutturata che li protegge dalle cellule immunitarie e dai farmaci. Il gruppo ha usato dispositivi microfluidici per imitare il flusso sanguigno in laboratorio e un modello su ratto per ricreare l’endocardite in animali vivi, permettendo loro di osservare come E. faecalis si adatti mentre l’infezione passa da poche cellule isolate a biofilm densi e maturi. 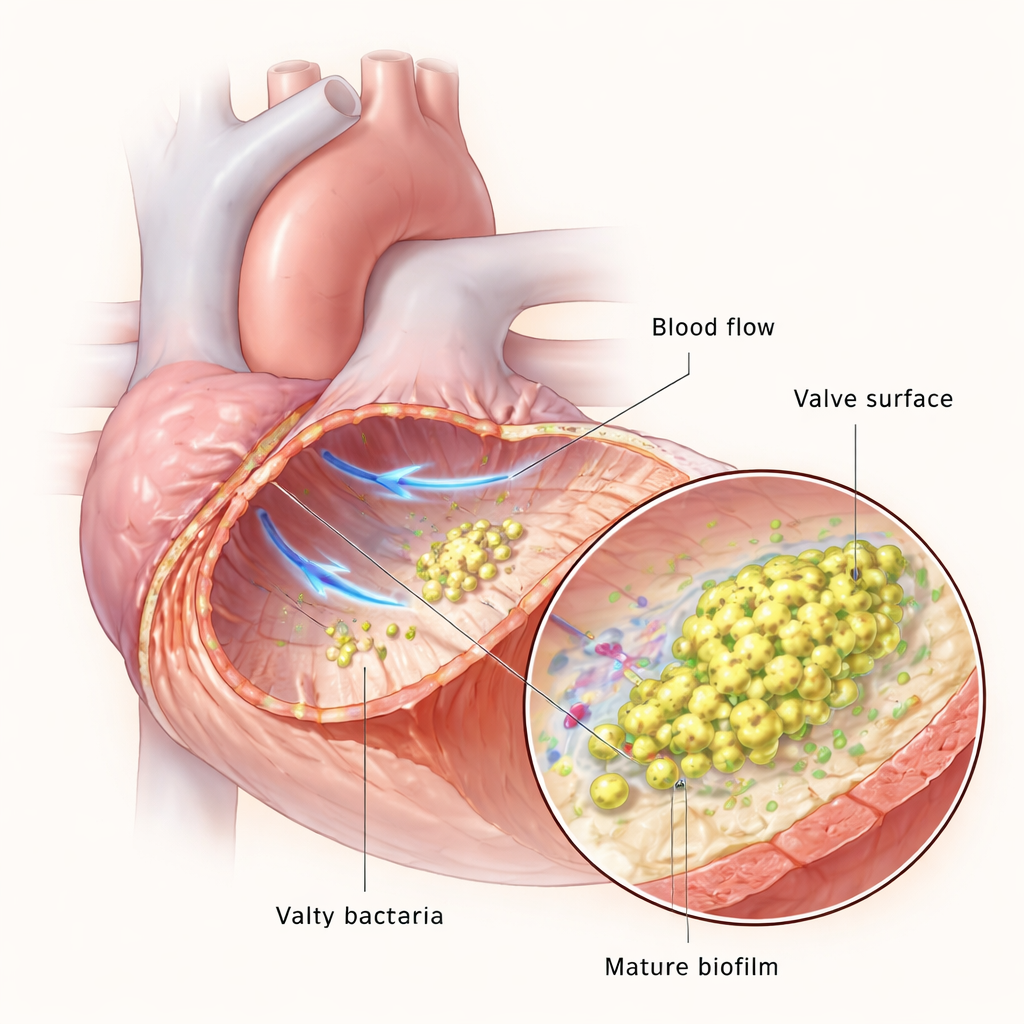
Quando il flusso sanguigno forte spegne il “chiacchiericcio” batterico
I batteri coordinano spesso il loro comportamento tramite il quorum sensing, un sistema chimico di “voto” che attiva o disattiva geni quando il numero di cellule è sufficiente. Fsr è il sistema di quorum sensing usato da E. faecalis. Sorprendentemente, i ricercatori hanno scoperto che un fluido in movimento intenso in realtà dilava le molecole segnalatrici necessarie per l’attivazione di Fsr. Nelle fasi iniziali dell’infezione, quando i batteri sono attaccati alla superficie esposta della vegetazione e sentono tutta la forza del flusso sanguigno, Fsr è in gran parte silente. Solo più tardi, quando le microcolonie crescono e si immergono più in profondità nella vegetazione — protette dal flusso — Fsr si attiva. Ciò significa che nel cuore reale il quorum sensing è governato non solo dal numero di batteri presenti, ma anche dalla loro posizione all’interno della struttura tridimensionale.
Spegnere Fsr permette il sovracrescere dei biofilm
Per verificare cosa fa concretamente Fsr nell’infezione, il gruppo ha confrontato batteri normali con mutanti privi dell’intero sistema Fsr. All’inizio, entrambe le versioni colonizzavano le valvole in modo simile. Ma dopo tre giorni, gli animali infettati con ceppi privi di Fsr presentavano vegetazioni più grandi e molti più batteri al loro interno. Imaging dettagliato ha mostrato che i loro biofilm ricoprivano una porzione maggiore della superficie del coagulo e che le microcolonie erano più grandi. La perdita di Fsr ha inoltre spento due enzimi secretati chiave, GelE e SprE, che normalmente aiutano a modellare il biofilm e possono limitare il sovracrescere. Animali infettati con mutanti privi solo di questi enzimi hanno sviluppato biofilm più voluminosi, sebbene non così estremi come nei ceppi privi di Fsr, suggerendo che altri fattori controllati da Fsr contribuiscono al fenomeno. 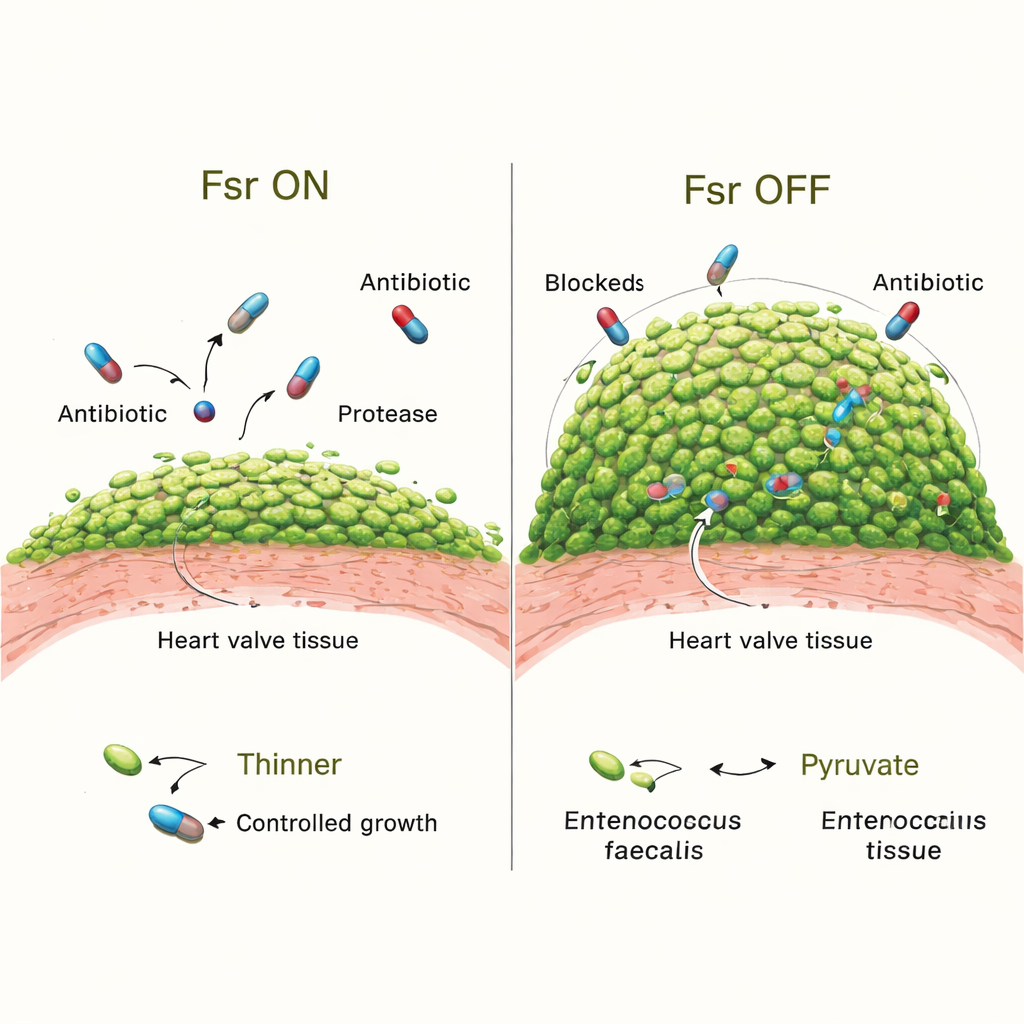
Rimodellamento metabolico e una presa più forte sugli antibiotici
Il profilo di espressione genica dei batteri all’interno delle valvole infette ha rivelato che Fsr fa più che regolare pochi enzimi. Senza Fsr centinaia di geni hanno cambiato attività, in particolare quelli coinvolti nell’assorbimento di zuccheri e nella produzione di energia. Una coppia di geni, lrgA e lrgB, è emersa come significativa: erano fortemente attivati nei batteri privi di Fsr e aiutavano le cellule a sfruttare meglio il piruvato, una piccola molecola ricca di energia presente nel sangue. Quando i ricercatori hanno cancellato lrgAB insieme a Fsr, l’eccesso di crescita del biofilm è scomparso, indicando un ruolo chiave per questa via metabolica nel sostenere l’infezione sovracresciuta. Di particolare rilievo, i biofilm privi di Fsr erano anche più difficili da curare. Nei ratti trattati con l’antibiotico gentamicina, le infezioni da batteri normali si sono ridotte e i conteggi piastrinici — un indicatore della gravità della malattia — sono migliorati. Al contrario, le infezioni prive di Fsr hanno risposto a malapena, nonostante i batteri non mostrassero maggiore resistenza nei test di laboratorio standard.
Una svolta specifica per l’uomo nell’infiammazione
Lo studio ha inoltre individuato un possibile modo con cui questi batteri possono accentuare l’infiammazione nell’uomo. L’enzima GelE può tagliare il precursore umano del segnale immunitario IL‑1β in una forma attiva che scatena risposte infiammatorie. In modo intrigante, GelE tagliava diversamente l’IL‑1β del ratto, degradandola piuttosto che attivarla, e il taglio preciso che produce l’attivazione era assente nelle proteine di ratto e di topo. Questo effetto specifico di specie suggerisce che negli esseri umani GelE possa contribuire a concentrare l’infiammazione proprio al margine del biofilm, peggiorando il danno tissutale durante l’endocardite.
Dal banco alla clinica: perché la perdita di Fsr conta per i pazienti
Per capire se questi risultati sperimentali avevano rilevanza nella pratica clinica, i ricercatori hanno analizzato isolati di E. faecalis provenienti da 81 pazienti con endocardite infettiva in Svizzera e negli Stati Uniti. Quasi metà dei ceppi mancava naturalmente del sistema Fsr. I pazienti infettati da questi ceppi Fsr‑negativi hanno presentato una batteriemia di durata maggiore — più giorni con batteri rilevabili nel sangue — e avevano più probabilità di entrare in una categoria di gravità elevata che includeva terapia intensiva, ricoveri prolungati, importanti interventi cardiaci o decesso. Altri geni di virulenza non hanno potuto spiegare questo schema, indicando direttamente la perdita di Fsr come marcatore chiave di una malattia più aggressiva.
Perché questo è importante per i trattamenti futuri
Nel complesso, questi risultati ribaltano l’idea semplice secondo cui bloccare la comunicazione batterica indebolirebbe sempre le infezioni. Nell’endocardite da E. faecalis, il sistema Fsr in realtà limita l’espansione del biofilm e rende i batteri più vulnerabili agli antibiotici. Quando Fsr manca, i batteri formano biofilm più densi, sfruttano più efficientemente i nutrienti del sangue e alimentano infezioni ostinate e prolungate. Per i pazienti, questo significa che i ceppi privi di Fsr possono prevedere una malattia più difficile da trattare, e che terapie che sopprimono indiscriminatamente il quorum sensing potrebbero avere effetti contrari in questo contesto. Al contrario, mirare con precisione a vie metaboliche come l’utilizzo del piruvato, o monitorare lo stato di Fsr e GelE come marcatori prognostici, potrebbe offrire modi migliori per gestire queste pericolose infezioni cardiache.
Citazione: Antypas, H., Schmidtchen, V., Staiger, W.I. et al. Loss of Fsr quorum sensing promotes biofilm formation and worsens outcomes in enterococcal infective endocarditis. Nat Commun 17, 1668 (2026). https://doi.org/10.1038/s41467-026-68366-8
Parole chiave: endocardite infettiva, biofilm batterici, quorum sensing, Enterococcus faecalis, tolleranza agli antibiotici