Clear Sky Science · it
saRNA VPg ingegnerizzato ottiene una traduzione cap-indipendente, a bassa immunogenicità e precisa di proteine terapeutiche in vivo
Rivoluzionare le regole per i farmaci a RNA
I vaccini basati su RNA messaggero (mRNA) hanno contribuito a cambiare le sorti della pandemia di COVID-19, ma usare molecole simili per sostituire o integrare proteine mancanti nelle malattie croniche è molto più difficile. L’organismo tende a eliminare rapidamente l’RNA estraneo e a montare forti risposte immunitarie, e molti progetti esistenti di RNA auto-amplificante fanno errori durante la copia. Questo studio descrive un nuovo tipo di RNA auto-amplificante — costruito con parti del norovirus umano — progettato per essere di lunga durata, meno infiammatorio e sorprendentemente preciso, aprendo la strada a terapie a RNA più precise e durature.
Un RNA auto-copiante più intelligente
I medicinali a mRNA convenzionali contengono una singola “ricetta” per una proteina e vengono letti una volta dalla cellula prima di essere degradati. L’RNA auto-amplificante (saRNA) include macchinario virale aggiuntivo che permette all’RNA di copiarsi all’interno delle cellule, aumentando notevolmente la produzione a partire da una piccola dose. I sistemi saRNA più studiati provengono dagli alfavirus, ma sono ingombranti, attivano forti difese antivirali e copiano le loro sequenze con precisione relativamente bassa. Gli autori si sono quindi rivolti al norovirus umano, una causa comune di gastroenterite. Hanno isolato una sezione compatta del materiale genetico del norovirus e l’hanno ricostruita come vettore per geni terapeutici. Al suo centro c’è VPg, una piccola proteina virale che è chimicamente attaccata all’estremità anteriore dell’RNA. VPg sostituisce la consueta struttura di “cap” presente negli mRNA umani e permette che l’RNA venga tradotto da un diverso insieme di fattori cellulari meno sensibili ad alcuni segnali di stress. 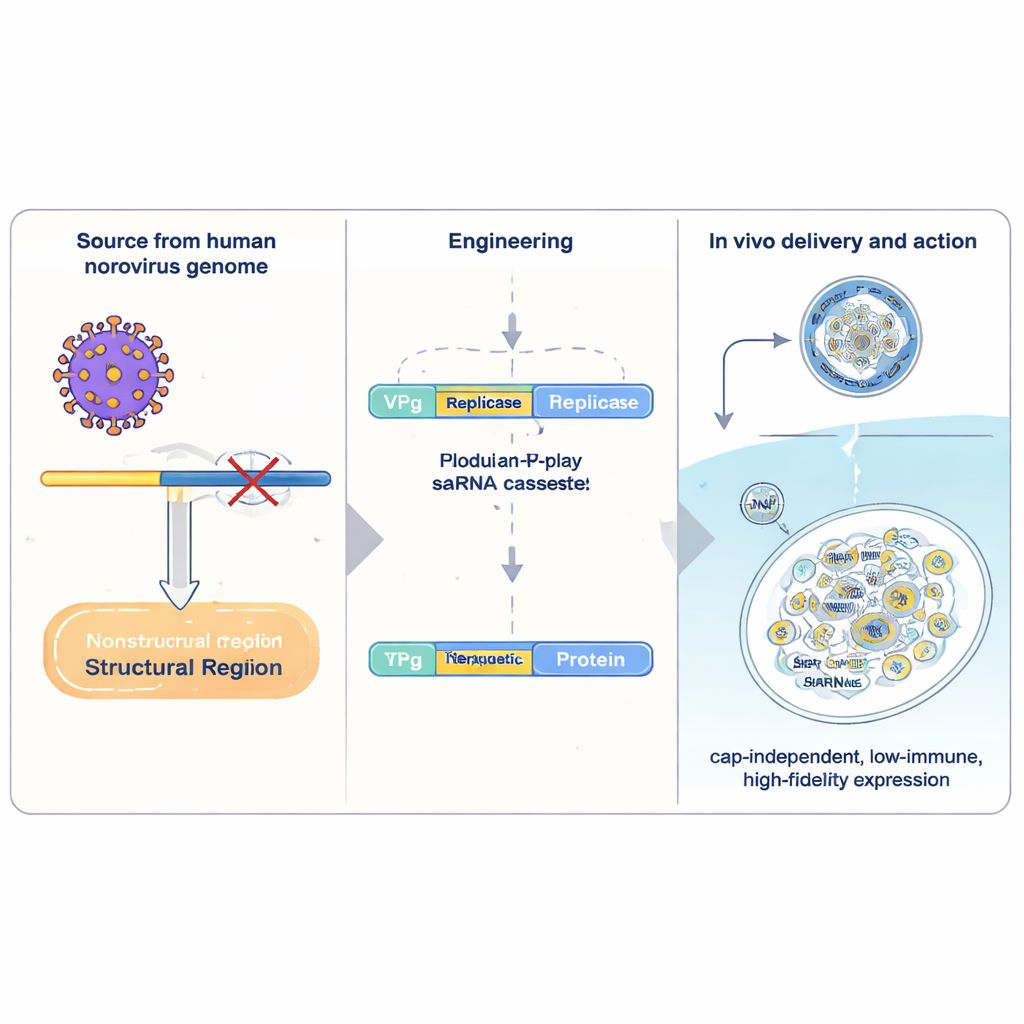
Alta precisione senza scatenare l’immunità
Per le terapie proteiche, la precisione è cruciale: anche piccoli errori di copia possono modificare il comportamento di un farmaco o creare sottoprodotti tossici. Il gruppo ha dimostrato che quando VPg del norovirus si lega all’enzima che copia l’RNA (una polimerasi), rallenta il tasso con cui vengono inseriti i blocchi costitutivi errati, riducendo nettamente il tasso di errori. Hanno individuato specifici amminoacidi in VPg che entrano in contatto con una regione di controllo chiave della polimerasi e hanno dimostrato che interrompere questa interfaccia rende la copia meno accurata. Allo stesso tempo, i progetti saRNA classici generano grandi quantità di RNA a doppio filamento, un segnale molecolare che attiva le difese antivirali e blocca la produzione proteica. Ridisegnando la polimerasi per favorire una specifica forma iniziale legata a VPg e riorganizzando il genoma in modo che venga prodotta efficientemente solo la singola elica terapeutica, gli autori hanno ridotto drasticamente la formazione di RNA a doppio filamento. Hanno inoltre ottimizzato una regione terminale dell’RNA in modo che VPg si attacchi al sito corretto, evitando frammenti corti non intenzionati che potrebbero tradursi in peptidi indesiderati.
Funziona dove l’mRNA standard fallisce
Il nuovo saRNA basato su VPg è stato poi testato in contesti patologici impegnativi dove l’mRNA cappato convenzionale arranca. Nella cachessia associata al cancro — una sindrome di deperimento in cui muscoli e grasso si riducono drasticamente — fattori chiave della traduzione che riconoscono il cap mRNA standard vengono inattivati, rendendo inefficienti gli mRNA cap-dipendenti. Poiché VPg usa un punto di accesso alternativo alla macchina di traduzione cellulare, ha continuato a sostenere la produzione dell’ormone grelina, che regola appetito e metabolismo, in un modello murino di tumore pancreatic. Iniezioni mensili a basso dosaggio hanno aiutato a preservare muscolo e tessuto adiposo, migliorato l’assunzione di cibo e il metabolismo e prolungato modestamente la sopravvivenza, senza tossicità evidente o segni di attivazione immunitaria cronica.
Attacco tumorale preciso e autoimmunità più calma
Per verificare se la copia ad alta fedeltà fosse davvero importante, i ricercatori hanno caricato il vettore VPg con un costrutto oncolitico complesso, GSDMDENG, progettato per perforare i mitocondri delle cellule tumorali e stimolare risposte immunitarie specifiche contro il tumore. Quando lo stesso costrutto è stato inserito in un saRNA convenzionale derivato da alfavirus, si sono accumulate mutazioni dopo ripetuti cicli di copia che hanno indebolito le sue funzioni selettive di uccisione tumorale e di priming immunitario. Al contrario, il sistema VPg ha preservato la sequenza prevista, ha prodotto una potente eliminazione delle cellule tumorali e ha scatenato risposte durature dei linfociti T che hanno rallentato o impedito il progresso del tumore pancreatico nei modelli murini. Infine, hanno applicato il saRNA VPg a una sfida diversa: la malattia cronica da trapianto contro l’ospite, in cui cellule immunitarie attaccano i polmoni dopo trapianto di midollo osseo. Un saRNA VPg che codifica la proteina C attivata ha ridotto la formazione di anticorpi dannosi, prevenuto la fibrosi polmonare e migliorato la respirazione nei topi, mentre un costrutto comparabile basato su alfavirus ha provocato una risposta innata più forte e peggiorato gli esiti.
Perché è importante per i futuri farmaci a RNA
Nel complesso, il lavoro delinea una piattaforma RNA compatta e “plug-and-play” che combina tre caratteristiche desiderabili: si auto-copia con precisione, è progettata per minimizzare gli allarmi immunitari e aggira alcuni dei colli di bottiglia che limitano la traduzione dell’mRNA standard. Poiché il gene terapeutico viene semplicemente inserito in uno scheletro fisso basato sul norovirus, molti proteine diverse — da ormoni a regolatori della coagulazione fino ad agenti oncolitici — possono essere testate sullo stesso telaio. Sebbene rimangano molti passi da compiere prima dell’uso clinico, questo approccio saRNA VPg suggerisce una strada verso farmaci a RNA che funzionano più come infusioni proteiche stabili: a basso dosaggio, più duraturi e progettati per operare anche in tessuti malati dove i messaggi mRNA ordinari non possono essere letti in modo affidabile. 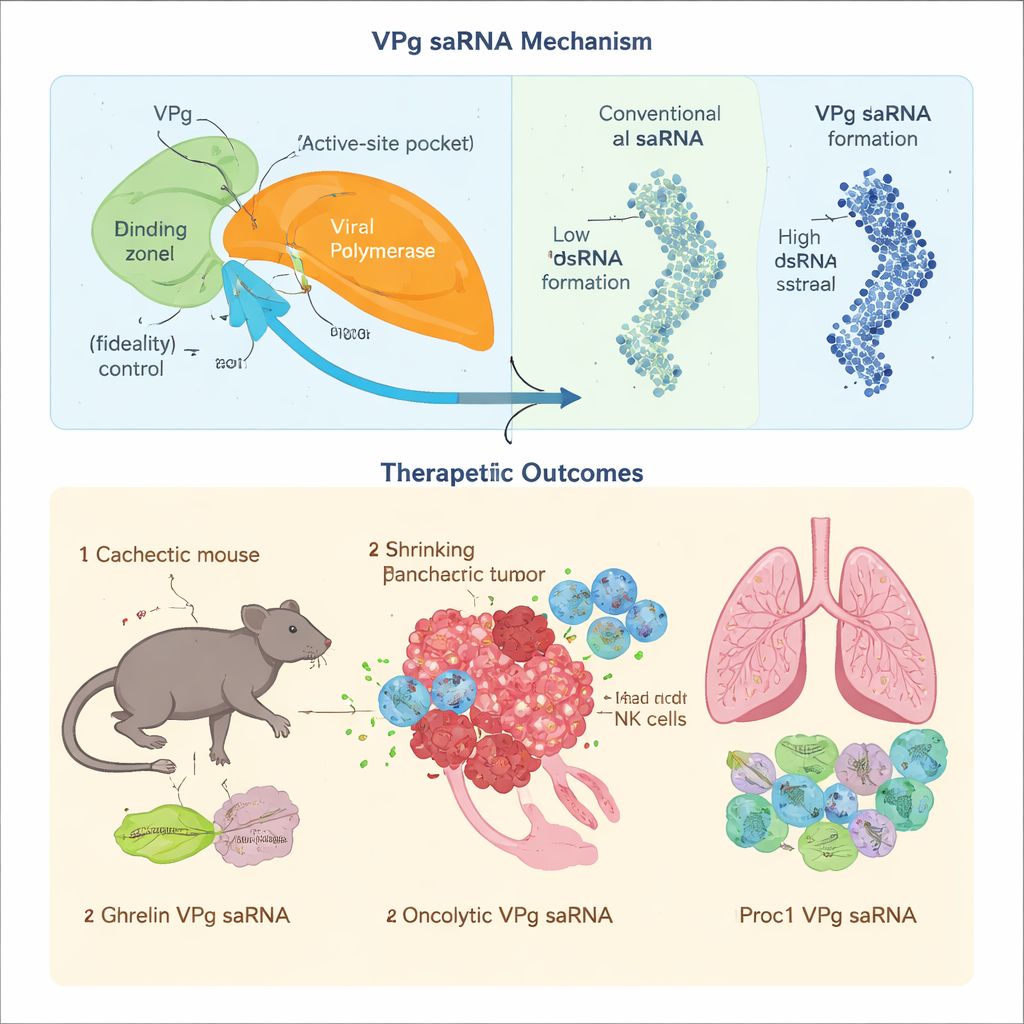
Citazione: Feng, Z., Chu, L., Li, Q. et al. Engineered VPg saRNA achieves cap-independent, low-immunogenic and precise encoding of therapeutic proteins in vivo. Nat Commun 17, 1666 (2026). https://doi.org/10.1038/s41467-026-68364-w
Parole chiave: RNA auto-amplificante, terapeutici a mRNA, VPg del norovirus, cachexia da cancro, malattia da trapianto contro l’ospite