Clear Sky Science · it
Deplezione guidata dalla firma trascrittomica delle cellule epiteliali alveolari intermedie migliora la fibrosi polmonare nei topi
Perché i polmoni cicatrizzati contano
La fibrosi polmonare è una grave malattia polmonare in cui i delicati alveoli si trasformano progressivamente in tessuto cicatriziale rigido, rendendo ogni respiro faticoso. I medici sanno che questa cicatrizzazione inizia quando i normali processi di riparazione vanno fuori strada, ma non era chiaro quali cellule specifiche fossero responsabili e come rimuoverle senza danneggiare il tessuto polmonare sano. Questo studio esplora un nuovo modo di “leggere” i messaggi molecolari all’interno delle cellule polmonari, usare queste informazioni per identificare cellule transitorie dannose e eliminarle selettivamente per ridurre la cicatrizzazione nei topi.
Cellule colte mentre riparano in modo difettoso
Dopo un danno polmonare, cellule speciali produttrici di surfattante chiamate cellule di tipo II normalmente si moltiplicano e poi maturano in sottili cellule di tipo I che rivestono gli alveoli e consentono il passaggio dell’ossigeno nel sangue. Nella fibrosi, molte di queste cellule rimangono bloccate in uno stato intermedio o transitorio invece di completare questa trasformazione. Studi precedenti con sequenziamento a singola cellula avevano individuato queste cellule intermedie sia nei topi sia negli esseri umani, ma non era chiaro se fossero semplici spettatori o attori chiave della malattia. Gli autori si sono concentrati su un tipo transitorio murino chiamato Krt8+ alveolar differentiation intermediates e sui loro corrispettivi umani noti come cellule basaloidi aberranti, che compaiono in grande numero nei polmoni cicatrizzati.
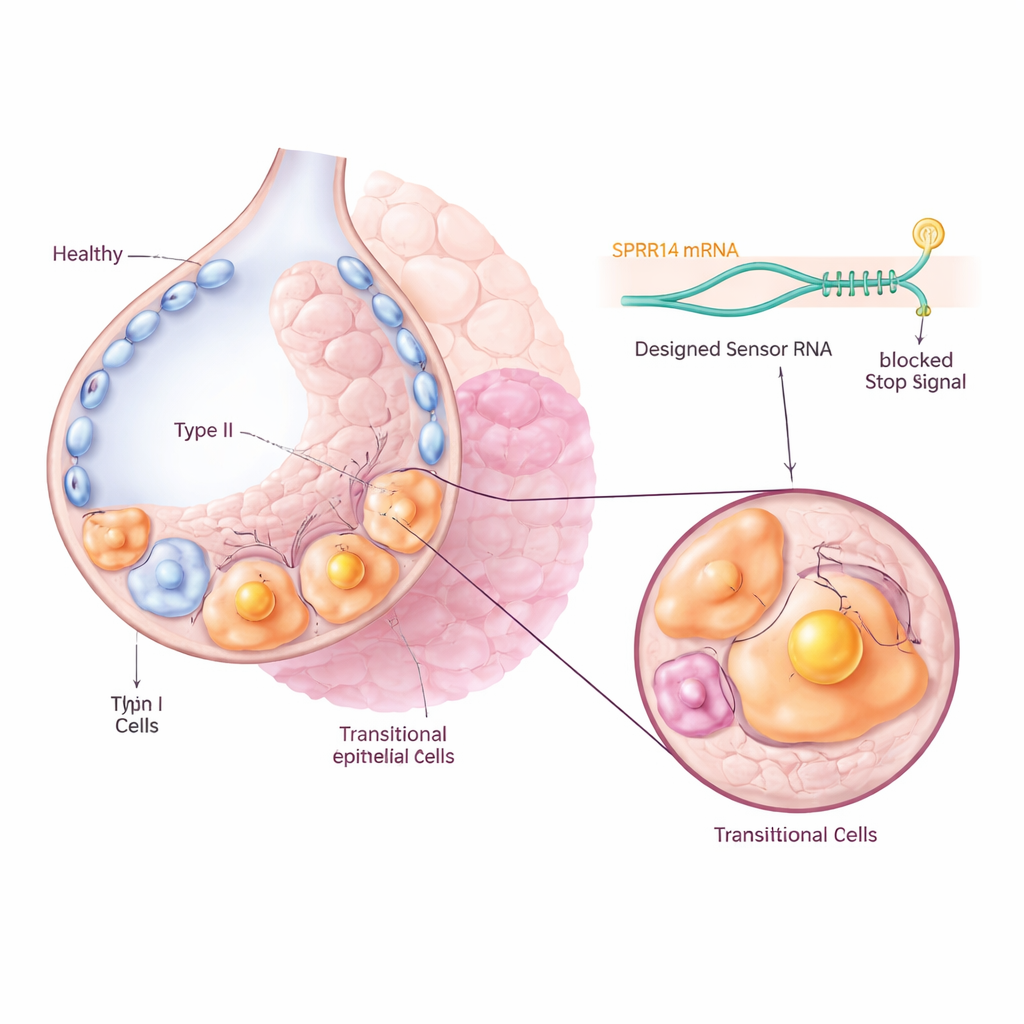
Trovare un distintivo molecolare unico
Per mirare a queste cellule problematiche senza coinvolgere le vicine sane, il gruppo ha inizialmente cercato nei grandi dataset di espressione genica un marcatore fortemente e specificamente attivato nella popolazione transitoria. Hanno identificato una molecola chiamata SPRR1A come distintivo particolarmente significativo: era fortemente arricchita nelle cellule intermedie Krt8+ nei polmoni fibrotici dei topi e nelle cellule basaloidi aberranti KRT5-/KRT17+ dei pazienti con fibrosi polmonare idiopatica, ma era in gran parte assente nelle cellule polmonari normali. L’osservazione microscopica di tessuto polmonare murino e umano ha confermato che SPRR1A compariva principalmente nelle aree danneggiate e rimodellate e non negli alveoli sani, suggerendo che potesse servire come maniglia precisa per identificare le cellule colpevoli.
Programmare le cellule con un sensore RNA
I ricercatori hanno poi utilizzato una tecnologia recentemente sviluppata chiamata CellREADR, che funziona come un sensore molecolare interno. Hanno progettato brevi sequenze di RNA in grado di appaiarsi con l’RNA di SPRR1A all’interno della cellula. Quando il sensore rileva SPRR1A, attiva la produzione di una proteina “effettrice” collegata, come una targhetta fluorescente o un recettore che rende la cellula sensibile a un farmaco. Nei topi, sono stati usati virus per consegnare questi costrutti sensore–effettore alle cellule polmonari. Solo le cellule che producevano attivamente SPRR1A accendevano il segnale fluorescente, permettendo al gruppo di tracciare e isolare le cellule transitorie direttamente dai polmoni fibrotici. Il sequenziamento a singola cellula ha mostrato che le cellule etichettate corrispondevano strettamente alla firma genica transitoria nota, confermando che il sensore RNA individuava con precisione la popolazione prevista.
Spegnere gli intermedi dannosi
Successivamente, l’effettore è stato sostituito con il recettore per la tossina difterica, in modo che le cellule positive per SPRR1A potessero essere uccise selettivamente mediante somministrazione di tossina difterica. Sincronizzando il trattamento con il picco di abbondanza delle cellule transitorie dopo un danno chimico ai polmoni, gli autori sono riusciti a rimuovere circa un terzo di questa popolazione. Questa deplezione mirata ha portato a una riduzione marcata della cicatrizzazione polmonare: si è riscontrata minore accumulo di collagene, livelli più bassi di proteine fibrotiche e strutture alveolari dall’aspetto più normale. Analisi dettagliate hanno mostrato che la maggior parte delle cellule positive per SPRR1A presentava segnali di uno stato di stress simile all’invecchiamento, con un piccolo sottogruppo capace di elevata proliferazione, suggerendo che questi intermedi non solo falliscono nel riparare correttamente il tessuto, ma contribuiscono anche a mantenere il processo fibrotico.
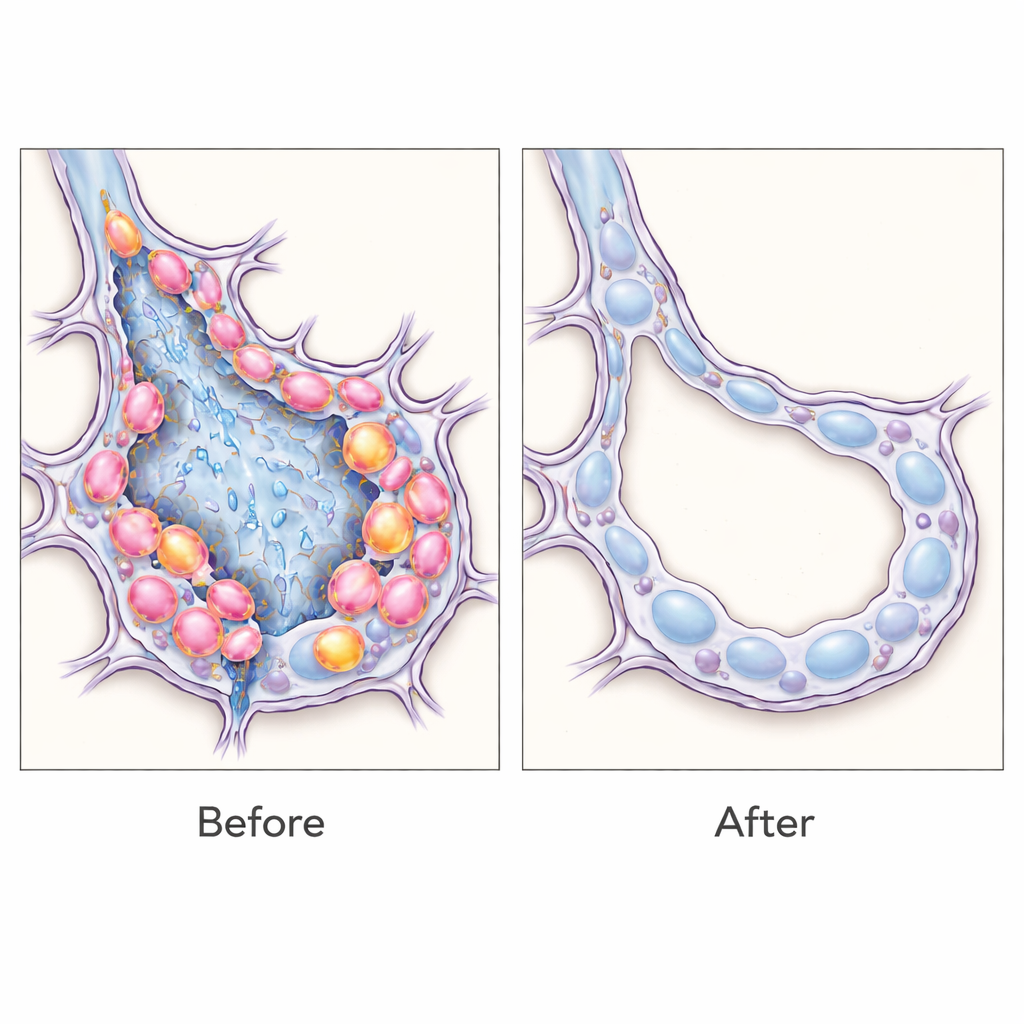
Cosa significa per i trattamenti futuri
Questi risultati sostengono l’idea che le cellule epiteliali transitorie non siano soltanto marcatori ma effettive promotrici della fibrosi polmonare, e che la loro rimozione selettiva possa riportare l’equilibrio verso un’architettura polmonare più sana nei topi. Più in generale, il lavoro dimostra una strategia flessibile: “leggendo” le firme di RNA specifiche delle cellule, i ricercatori possono etichettare, studiare e persino eliminare popolazioni cellulari definite con precisione nei tessuti viventi senza dover creare ogni volta linee animali personalizzate. Sebbene rimanga molto lavoro prima che strumenti di rilevamento RNA simili possano essere adattati in sicurezza per l’uomo, questo approccio apre la strada a terapie di precisione che colpiscono i tipi cellulari esatti che compromettono la guarigione nella cicatrizzazione polmonare cronica e, potenzialmente, in altre malattie fibrotiche.
Citazione: Peng, F., Jiang, Cs., Zheng, Z. et al. Transcriptomic signature-guided depletion of intermediate alveolar epithelial cells ameliorates pulmonary fibrosis in mice. Nat Commun 17, 1636 (2026). https://doi.org/10.1038/s41467-026-68354-y
Parole chiave: fibrosi polmonare, cellule epiteliali alveolari, sequenziamento RNA a singola cellula, tecnologia di rilevamento RNA, senescenza cellulare