Clear Sky Science · it
Atlante a singolo nucleo dell’amigdala centrale rivela dinamiche della cromatina e della trascrizione genica nel disturbo da uso di alcol umano
Perché questa ricerca conta nella vita di tutti i giorni
Il disturbo da uso di alcol (AUD) colpisce milioni di persone e le loro famiglie, eppure sappiamo sorprendentemente poco di quello che il consumo eccessivo prolungato fa al cervello umano a livello delle singole cellule. Questo studio si concentra su una piccola ma critica regione — l’amigdala centrale, un nodo per paura, stress e motivazione — per mappare come l’alcol rimodella le cellule cerebrali e i loro sistemi di controllo genetico. Associando l’avanzata tecnologia di sequenziamento “a singola cellula” con studi genetici sul rischio di dipendenza, gli autori iniziano a spiegare perché alcune persone sono più vulnerabili all’AUD e come l’alcol lasci cicatrici molecolari persistenti nel cervello.
Uno sguardo ravvicinato a un minuscolo centro cerebrale
L’amigdala centrale è una stazione di uscita chiave nella rete cerebrale delle emozioni e dello stress ed è fortemente collegata all’alleviamento dell’ansia, alla voglia e all’uso compulsivo di alcol. In questo lavoro i ricercatori hanno analizzato circa 175.000 singoli nuclei cellulari prelevati postmortem dall’amigdala centrale di 50 persone — 22 con storia di disturbo da uso di alcol e 28 senza AUD. Utilizzando una tecnologia che legge sia l’attività genica (RNA) sia l’accessibilità della cromatina (quanto il DNA è “aperto” o “chiuso”) nella stessa cellula, hanno costruito un atlante dettagliato di tutti i principali tipi cellulari di questa regione, includendo diversi tipi di neuroni e cellule di supporto come astrociti e microglia. Hanno scoperto che i neuroni inibitori — che attenuano o modellano l’attività cerebrale — sono particolarmente abbondanti nell’amigdala centrale e sembrano particolarmente colpiti nelle persone con AUD. 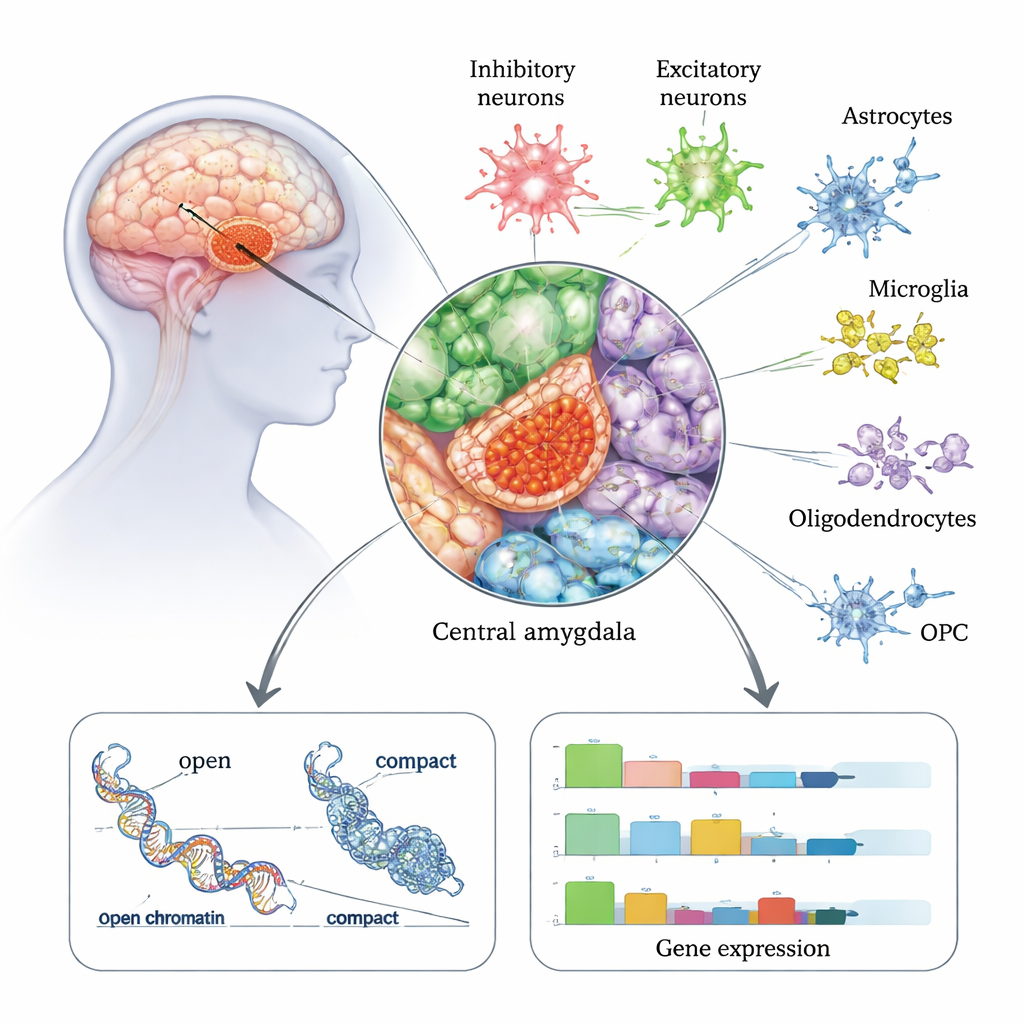
Quali cellule e geni cambiano nel disturbo da uso di alcol?
Il gruppo ha confrontato sistematicamente l’attività genica tra persone con e senza AUD, cellula per cellula. Hanno identificato oltre 1.800 geni la cui attività era alterata in popolazioni cellulari specifiche, con i maggiori spostamenti nei neuroni inibitori, seguiti da neuroni eccitatori e astrociti. Un sottotipo di neurone inibitore marcato dal peptide proenkephalina (PENK) ha mostrato cambiamenti particolarmente pronunciati. Molti dei geni interessati sono coinvolti nella comunicazione tra cellule cerebrali, in particolare nell’equilibrio tra il segnale eccitatorio glutammato e il segnale inibitorio GABA. Ad esempio, il gene GABRA2, che contribuisce alla formazione di un importante tipo di recettore GABA, risultava aumentato in certi neuroni inibitori, mentre GRM8, un recettore del glutammato, e NCAM1, una molecola di adesione cellulare importante per le sinapsi, cambiavano in direzioni opposte tra i sottotipi neuronali. Questi schemi suggeriscono che la messa a punto dell’eccitazione e dell’inibizione nell’amigdala centrale è alterata nell’AUD.
Gli interruttori di controllo del cervello: cromatina ed elementi regolatori
I geni non agiscono da soli; sono controllati da tratti di DNA che funzionano come interruttori e dimmer. Analizzando la cromatina — il modo in cui il DNA è impacchettato — i ricercatori hanno identificato oltre mezzo milione di elementi regolatori candidati e li hanno collegati a geni vicini in modo specifico per tipo cellulare. Quasi la metà di questi elementi era unica per un singolo tipo cellulare, evidenziando quanto siano specializzate le diverse cellule cerebrali. Molti elementi regolatori che cambiavano nell’AUD erano connessi a geni coinvolti nella gestione del calcio e nella segnalazione del glutammato, come CALN1, un gene che lega il calcio fortemente attivo nei neuroni. Nei neuroni inibitori CALN1 mostrava sia un’espressione aumentata sia densi ammassi di anelli regolatori, implicando che l’esposizione all’alcol rimodella l’architettura locale del DNA che controlla questo gene. 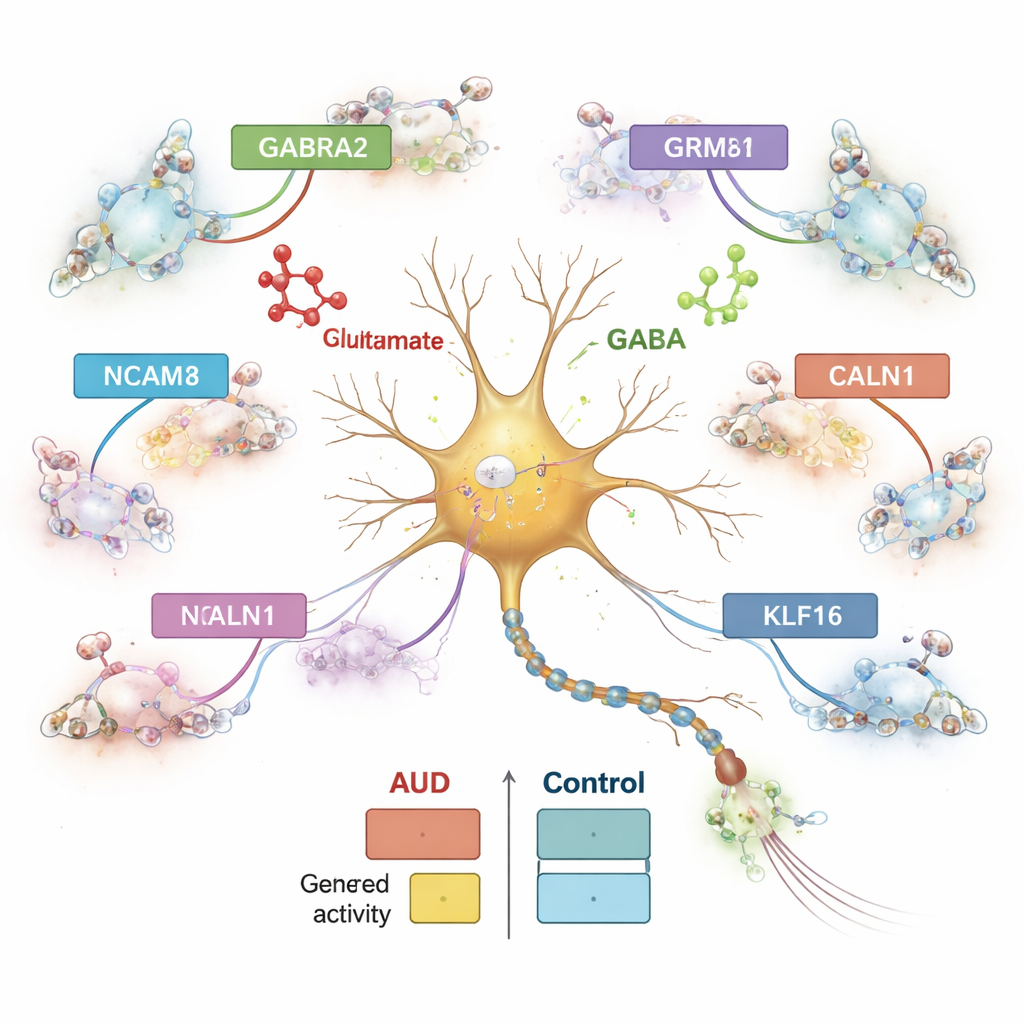
Dai geni del rischio ai cambiamenti reali nel cervello
Studi genetici hanno identificato molte varianti del DNA che aumentano il rischio di sviluppare problemi legati all’alcol, ma dove e come agiscano nel cervello era rimasto poco chiaro. Sovrapponendo le loro mappe a singola cellula con grandi studi di associazione genome-wide sul consumo problematico di alcol, gli autori hanno scoperto che i geni di rischio sono sproporzionatamente attivi e dysregolati nei neuroni dell’amigdala centrale, in particolare in quelli inibitori. Hanno individuato oltre 200 varianti di rischio probabilmente causali che si trovano all’interno di elementi regolatori aperti in tipi cellulari specifici. Alcune ricadevano in o vicino a geni già legati alla dipendenza, come CACNA1C e DRD2, che aiutano a controllare l’eccitabilità neuronale e la segnalazione della dopamina. Altre, tra cui SEMA6D e NF1, sono emerse come nuove candidate. Il team ha anche identificato una famiglia di fattori di trascrizione chiamata Kruppel-like factors (in particolare KLF16) che sembrano coordinare ampie modifiche nei geni legati al calcio e al glutammato, e ha confermato parti di questa rete regolatoria in un modello murino di esposizione acuta all’alcol.
Cosa significa per comprendere e trattare l’AUD
In termini semplici, questo studio mostra che il disturbo da uso di alcol non è solo un problema cerebrale diffuso, ma una perturbazione altamente organizzata concentrata in tipi cellulari e percorsi molecolari particolari all’interno di un hub emotivo critico. I neuroni inibitori dell’amigdala centrale, insieme a astrociti e altre cellule di supporto, mostrano cambiamenti coordinati nell’attività genica e negli interruttori del DNA che regolano quei geni — specialmente nei sistemi che gestiscono i segnali di glutammato, GABA e calcio. Collegando questi cambiamenti cellulari alle varianti genetiche di rischio, il lavoro offre una mappa che collega la vulnerabilità ereditata a eventi molecolari concreti nel cervello. Nel tempo, mappe cellula‑specifiche di questo tipo potrebbero guidare lo sviluppo di trattamenti più precisi che ristabiliscano l’equilibrio tra eccitazione e inibizione, invece di agire in modo generalizzato su tutto il cervello.
Citazione: Lee, C.Y., Hwang, A., McRiley, D. et al. Central amygdala single-nucleus atlas reveals chromatin and gene transcription dynamics in human alcohol use disorder. Nat Commun 17, 1634 (2026). https://doi.org/10.1038/s41467-026-68351-1
Parole chiave: disturbo da uso di alcol, amigdala centrale, genomica a singola cellula, neuroni inibitori, regolazione genica