Clear Sky Science · it
Dalla formazione del complesso TDP-43/RNA all’aggregazione patologica di TDP-43: un approccio strutturale e cellulare
Perché questa proteina cerebrale è importante
Le malattie neurodegenerative, come la sclerosi laterale amiotrofica (SLA) e la demenza frontotemporale, spesso presentano aggregati di proteine mal ripiegate all’interno dei neuroni. Uno dei colpevoli più ricorrenti è la proteina TDP-43, che normalmente contribuisce all’elaborazione dell’RNA — la copia operativa dei nostri geni. Questo studio affronta una domanda cruciale: cosa fa TDP-43 nelle cellule sane e cosa va storto perché un utile fattore dell’RNA diventi una proteina che forma aggregati tossici?
Come funziona TDP-43 nei neuroni sani
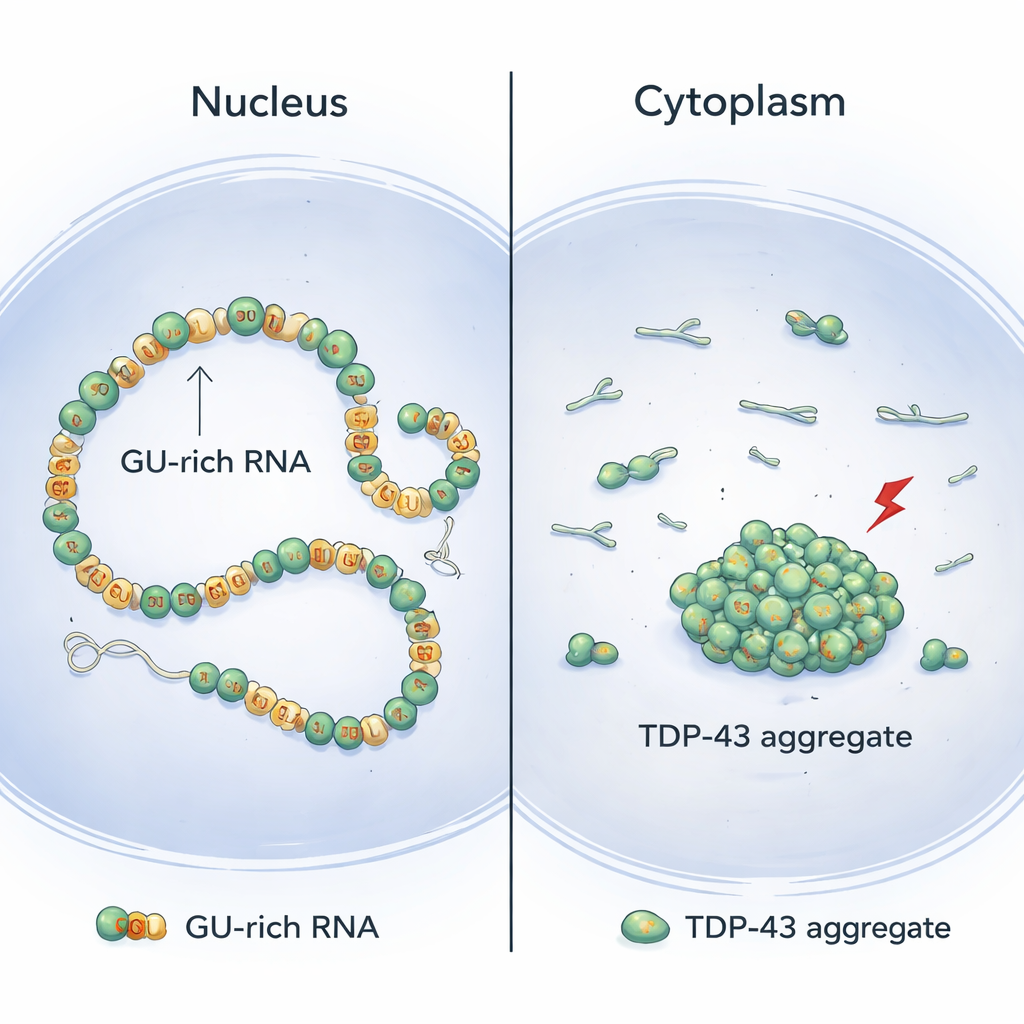
TDP-43 si trova di solito nel nucleo cellulare, dove si lega a lunghi tratti di RNA ricchi di ripetuti mattoni “GU”. Usando una combinazione di biologia strutturale ed esperimenti cellulari, gli autori mostrano che le molecole di TDP-43 si allineano in modo cooperativo lungo queste regioni ricche di GU, formando catene lisce e continue sull’RNA. In questa disposizione, l’estremità anteriore della proteina — il dominio N-terminale — rimane fisicamente separata tra molecole adiacenti. Di conseguenza, questi segmenti N-terminali restano disponibili per raggiungere e collegare porzioni distanti ricche di GU dello stesso RNA, creando delicati anelli e compattando lunghi introni (le regioni non codificanti all’interno dei geni) senza aggregarsi.
Una lotta interna alla proteina
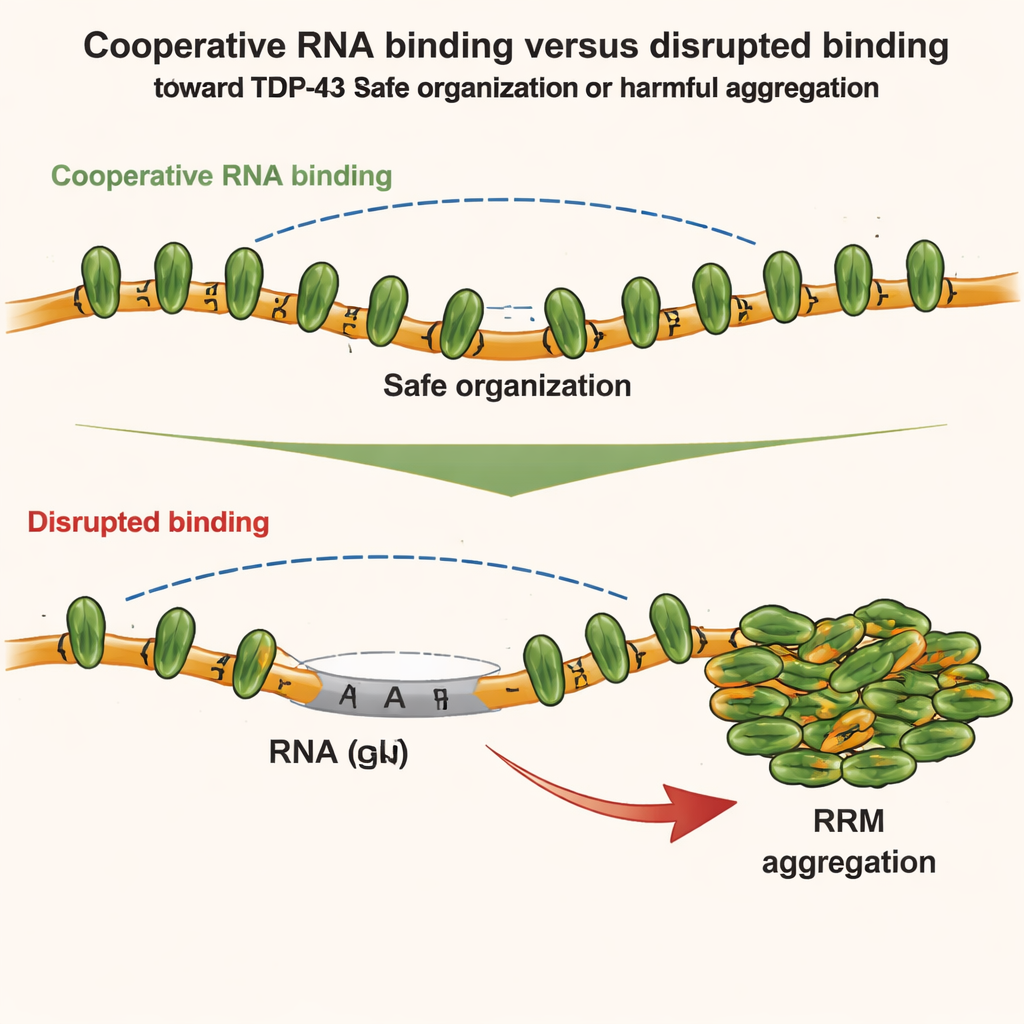
Il gruppo ha poi esplorato come le diverse parti di TDP-43 competano o cooperino tra loro. Si sono concentrati su due regioni: il dominio N-terminale, che può aderire ad altri domini N-terminali, e i moduli centrali leganti l’RNA, che guidano il legame cooperativo lungo l’RNA ricco di GU. Usando tecniche sensibili come la spettroscopia NMR, la calorimetria e la diffrazione a basso angolo (SAXS), hanno osservato che quando TDP-43 si lega all’RNA in modo cooperativo, la geometria della catena indebolisce in realtà i contatti diretti N-terminale–N-terminale tra molecole adiacenti. In altre parole, il forte legame cooperativo all’RNA tiene sotto controllo le interazioni locali tra N-terminali. Ma quando questa cooperatività viene rotta — per esempio inserendo tratti non GU nell’RNA o mutando TDP-43 — i domini N-terminali di proteine vicine si avvicinano e possono ora agganciarsi l’uno all’altro.
Dalla compattazione utile al raggruppamento dannoso
Queste intuizioni strutturali sono state testate in cellule vive. Gli autori hanno usato sistemi cellulari ingegnerizzati per seguire come diversi mutanti di TDP-43 si mescolano o si separano all’interno di compartimenti artificiali ricchi di RNA. Hanno rilevato che sia il legame cooperativo all’RNA sia le interazioni N-terminali contribuiscono a organizzare TDP-43 in assemblaggi di ordine superiore, ma in modi differenti. Il legame cooperativo dispone le proteine lungo l’RNA ricco di GU, mentre i contatti N-terminali collegano tra loro ammassi distanti. Tuttavia, sotto uno stress ossidativo lieve, il quadro cambia. Un agente chimico stressante (arsenito) induce modifiche chimiche specifiche — acetilazione — sui motivi centrali leganti l’RNA, rendendoli inclini ad aderire. Se il legame cooperativo all’RNA è intatto, TDP-43 resta per lo più solubile. Se la cooperatività è indebolita, i legami N-terminali tra molecole TDP-43 vicine agiscono come un’impalcatura che avvicina i core acetilati, favorendo l’aggregazione irreversibile.
Perché TDP-43 forma più aggregati nel citoplasma
Il modello emerso da questo lavoro aiuta a spiegare perché gli aggregati di TDP-43 si trovano spesso nel citoplasma dei neuroni malati anziché nel nucleo. Nel nucleo sono comuni lunghi introni con molte ripetizioni GU, che favoriscono un legame continuo e cooperativo che mantiene basse le interazioni N-terminali pericolose tra vicini e permette invece un sicuro avvolgimento a lunga distanza. Nel citoplasma, invece, gli RNA maturi hanno molte meno regioni ricche di GU. Questo rende il legame di TDP-43 più a macchia di leopardo e meno cooperativo, aumentando la probabilità che domini N-terminali adiacenti interagiscano e predisponendo all’aggregazione una volta che avvengono modifiche chimiche indotte dallo stress. A sostegno di questa ipotesi, la fornitura artificiale di introni ricchi di GU nel nucleo riduce l’aggregazione di TDP-43 sotto stress.
Cosa significa per terapie future
In sintesi, lo studio ritrae TDP-43 come una proteina in equilibrio tra l’organizzazione utile dell’RNA e il raggruppamento dannoso, con il legame cooperativo all’RNA ricco di GU che funge da meccanismo di sicurezza. Quando quella rete di sicurezza viene meno — a causa di sequenze di RNA alterate, mutazioni proteiche o stress cellulare — gli stessi domini che normalmente compattano i lunghi segmenti di RNA possono invece promuovere la formazione di aggregati tossici. Per i non specialisti, la conclusione principale è che mantenere il giusto tipo di interazioni tra TDP-43 e l’RNA potrebbe essere una strategia promettente per prevenire o rallentare la formazione di aggregati proteici osservata nella SLA e in malattie cerebrali correlate.
Citazione: Feng, Y., Joshi, V., Pankivskyi, S. et al. From TDP-43/RNA complex formation to disease-linked TDP-43 aggregation through a structural and cellular approach. Nat Commun 17, 1631 (2026). https://doi.org/10.1038/s41467-026-68346-y
Parole chiave: Aggregazione di TDP-43, Proteine leganti l’RNA, SLA, Interazioni proteina–RNA, Neurodegenerazione