Clear Sky Science · it
Ingegneria ligando atomica di precisione di nanoparticelle d'oro tramite trasferimento di massa interfaciale
Perché le particelle d'oro minuscole contano per la salute
La diagnostica medica fa sempre più affidamento su nanoparticelle—particelle minuscole migliaia di volte più piccole di un capello umano—per illuminare organi e tumori in profondità nel corpo. Questo studio mostra come gli scienziati possano ora perfezionare il rivestimento esterno di particelle d'oro ultrasottili quasi atomo per atomo, in modo che lo stesso nucleo luminoso possa essere indirizzato verso organi diversi, in particolare spostandone l'accumulo dal fegato e dalla milza verso i reni. Tale controllo potrebbe aiutare a progettare agenti di imaging e vettori farmaceutici più sicuri che vadano esattamente dove i medici desiderano e vengano eliminati dall'organismo in modo più pulito.
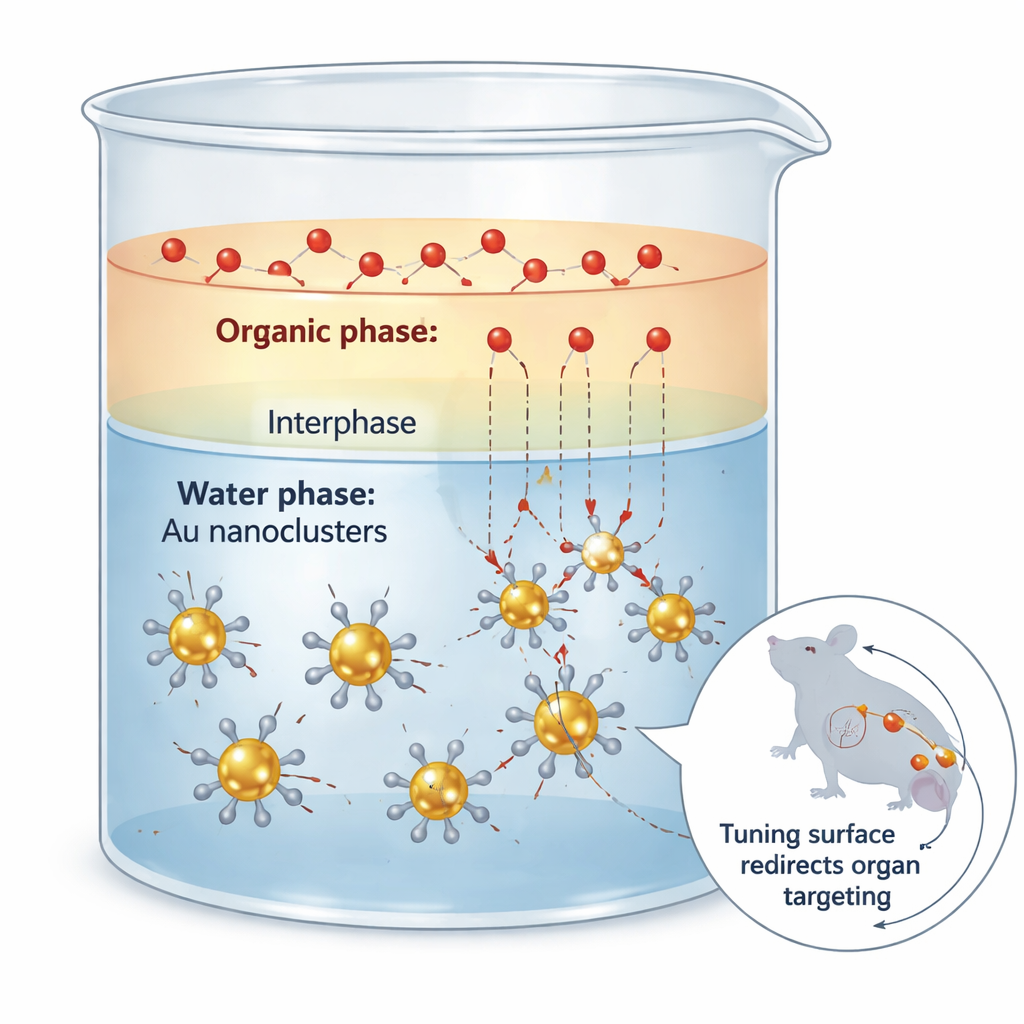
La sfida di vestire i nanocluster d'oro
I nanocluster d'oro sono particelle di dimensioni ultra-piccole che si comportano più come grandi molecole che come grani metallici. Possono emettere luce nella finestra del vicino infrarosso II, che penetra profondamente nel tessuto e fornisce immagini nitide con basso rumore di fondo. Tuttavia, quasi tutto il comportamento di questi cluster nell'organismo—dove si dirigono, quanto a lungo circolano e come vengono eliminati—dipende non dall'oro in sé, ma dai ligandi organici, o molecole di “guscio”, legati alla loro superficie. I metodi tradizionali per cambiare questo guscio spesso funzionano come un intervento grossolano: la reazione procede troppo rapidamente, il rivestimento risulta irregolare e il nucleo d'oro può essere parzialmente consumato, rovinando sia la struttura sia le proprietà ottiche.
Rallentare il traffico tra due liquidi
I ricercatori hanno affrontato questo problema sfruttando un'idea fisica semplice: la resistenza al trasferimento di massa al confine tra due liquidi che non si mescolano completamente. Hanno posto i nanocluster d'oro in acqua e i ligandi entranti a base di zolfo in un solvente organico come l'acetato di etile. Nella sottile regione dove i due liquidi si mescolano parzialmente, i ligandi diffondono lentamente verso i cluster e si scambiano con il guscio originale. Misure cinetiche accurate hanno mostrato che l’indesiderato “etching” del nucleo d'oro è estremamente sensibile alla concentrazione di ligando libero, mentre lo scambio desiderato lo è molto meno. Utilizzando il sistema a due fasi per mantenere bassi ma continuamente riforniti i livelli di ligando libero, il team ha ridotto l'etching di circa sessanta volte pur preservando la maggior parte della velocità di scambio utile.
Costruire un kit molecolare di precisione
Con questo metodo assistito dall'interfase, gli autori sono stati in grado di sostituire i ligandi superficiali su un modello di cluster d'oro, Au25, in modo altamente controllato. Sono partiti da cluster protetti da un ligando acido solfonico carico negativamente e hanno inserito una varietà di nuovi tioli portatori di gruppi carbossilici, amminici, ossidrilici, nitro e anelli aromatici idrofobici. La spettrometria di massa ha rivelato miscele pulite e ben definite, come cluster Au25 che presentano numeri specifici di ciascun tipo di ligando, piuttosto che distribuzioni ampie e disordinate. Il metodo ha funzionato anche per altre dimensioni di cluster e famiglie di ligandi, suggerendo che si tratta di una strategia generale per creare nanocluster d'oro robusti e su misura per diverse applicazioni.
Guidare le nanoparticelle dal fegato ai reni
La prova più significativa di questa precisione è venuta da esperimenti di imaging in vivo su topi. Introducendo gradualmente un ligando carico positivamente, p-aminotiolofenolo, nello strato altrimenti carico negativamente, il team ha creato una serie di cluster il cui carico superficiale complessivo variava da fortemente negativo a quasi zwitterionico (gruppi positivi e negativi bilanciati). Tutte le versioni brillavano in modo simile nei test di laboratorio, ma la loro biodistribuzione nei topi differiva in modo drammatico. I cluster puramente negativi si accumulavano principalmente in fegato e milza. Aggiungendo più ligandi positivi, il segnale in questi organi diminuiva e aumentava quello nei reni e nella vescica, indicando un miglioramento della clearance renale. Quando è stato usato un ligando neutro con gruppo ossidrilico al posto dell'ammina, questo spostamento non si è verificato, sottolineando il ruolo particolare delle cariche positive nel reindirizzare le particelle.
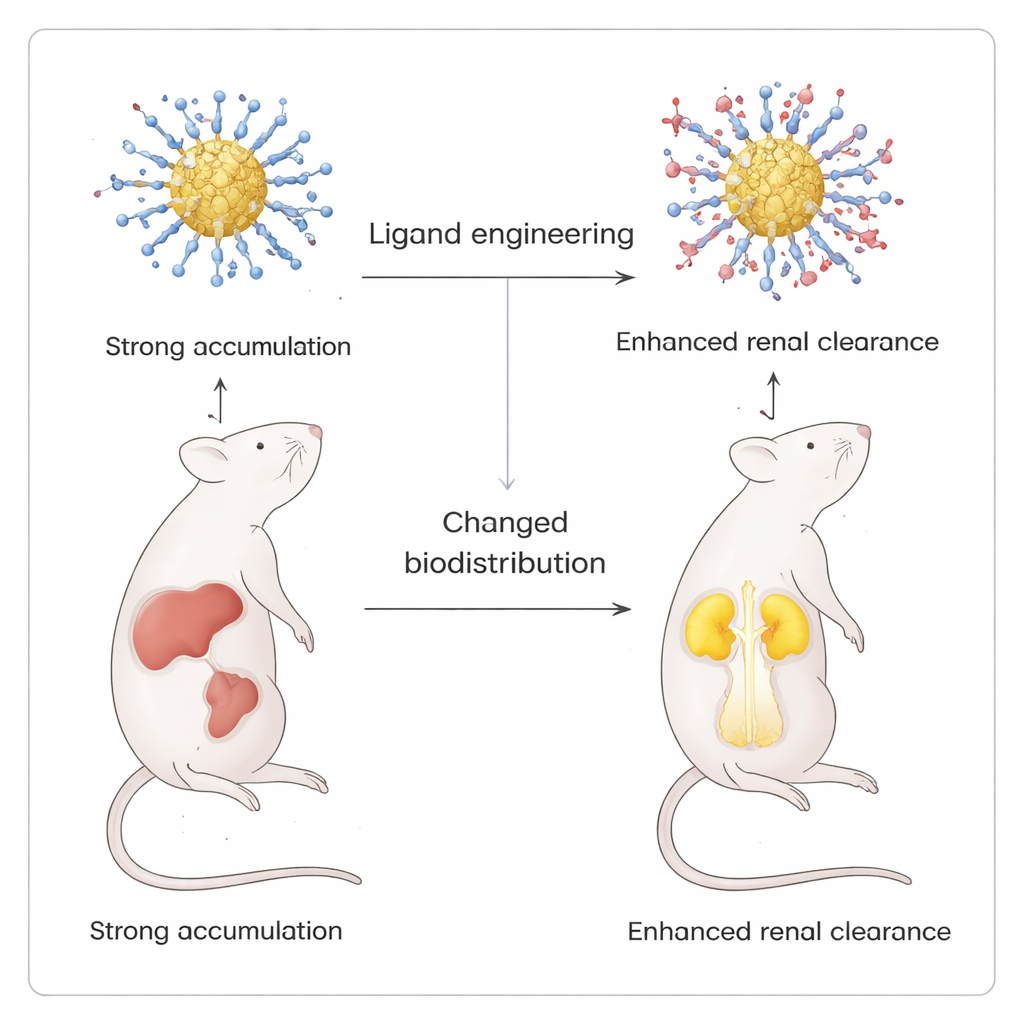
Cosa significa per le medicine del futuro
Per i non specialisti, il punto chiave è che gli scienziati hanno trovato un modo per “vestire” i nanocluster d'oro luminosi con rivestimenti molecolari che possono essere sintonizzati quasi una molecola alla volta, senza danneggiare la particella sottostante. Usando un sistema delicato a due liquidi, possono controllare sia la chimica sia il destino finale di queste particelle all'interno del corpo. Questo livello di controllo rende possibile progettare agenti di imaging e potenziali vettori farmaceutici che illuminano organi specifici e poi lasciano il corpo attraverso i reni anziché permanere nel fegato e nella milza, aprendo la strada a una nanomedicina più sicura e prevedibile.
Citazione: Zhang, B., Xiao, F., Song, X. et al. Atomically precise ligand engineering of gold nanoparticles via interphase mass transfer. Nat Commun 17, 1630 (2026). https://doi.org/10.1038/s41467-026-68345-z
Parole chiave: nanocluster d'oro, ingegneria dei ligandi, bioimaging, nanomedicina, biodistribuzione