Clear Sky Science · it
L'attività di DOT1L limita la velocità di allungamento della trascrizione e favorisce la pausa della RNAPII per facilitare la mutagenesi da parte di AID
Come le nostre cellule immunitarie regolano con precisione modifiche rischiose del DNA
Il nostro sistema immunitario crea anticorpi potenti mutando deliberatamente il proprio DNA, una strategia rischiosa che talvolta può favorire il cancro. Questo studio affronta una domanda apparentemente semplice ma dalle grandi implicazioni: che cosa controlla dove e con quale efficienza avvengono queste mutazioni intenzionali? La risposta ruota attorno a una proteina chiamata DOT1L, che regola la velocità di lettura dei geni nei linfociti B e, così facendo, aiuta a indirizzare la macchina delle mutazioni nei punti giusti.
Attivare la mutazione per affinare gli anticorpi
Quando i linfociti B incontrano un’infezione, migliorano gli anticorpi in due modi. Introducono piccole modifiche nella regione di legame dell’anticorpo per aumentare l’affinità per i patogeni e sostituiscono la porzione Fc dell’anticorpo per modificare la risposta immunitaria. Entrambi gli aggiornamenti iniziano con un enzima chiamato AID, che incide e altera il DNA nei geni attivamente trascritti. Pur essendo essenziale per una buona immunità, AID può anche colpire altri geni, creando rotture pericolose che guidano i tumori ematologici. Lavori precedenti avevano mostrato che AID predilige geni fortemente trascritti e regolati da potenti interruttori genetici chiamati super-enhancer, ma questo non spiegava completamente perché solo un sottoinsieme selezionato di geni sia realmente vulnerabile.
Un marcatore cromatinico che segnala i geni sensibili ad AID
Gli autori si sono concentrati sulle proteine che si trovano in prossimità di AID nel nucleo. Utilizzando una tecnica di marcatura per prossimità in cellule umane, hanno scoperto che AID si aggrega vicino a DOT1L, un enzima che aggiunge un segno chimico su un punto specifico delle proteine istoniche intorno al DNA. Questa marcatura, un tag chimico sull'istone H3 nella posizione K79, è comune nei geni attivi. Nei linfociti B di topo, i geni che AID muta frequentemente — inclusi i geni degli anticorpi e gli off-target legati al cancro — presentano livelli particolarmente alti di questi segni prodotti da DOT1L. Quando i ricercatori hanno disattivato DOT1L in linee di cellule B o ne hanno bloccato l'attività con un farmaco, lo “switch” di classe degli anticorpi è diminuito, così come le rotture del DNA guidate da AID e le fusioni tra geni degli anticorpi e il gene di crescita cMyc, favorevoli al cancro. È importante che fosse richiesta la funzione catalitica di DOT1L, non soltanto la sua presenza: versioni mutate incapaci di collocare il marcatore istonico non sono riuscite a ripristinare lo switch degli anticorpi.
Rallentare il lettore di geni per dare tempo ad AID
A prima vista questo sembra paradossale perché DOT1L è associato a geni attivi, eppure la sua rimozione non ha semplicemente spento quei geni. Usando un metodo che cattura istantanee dell’RNA neo-sintetizzato, il gruppo ha scoperto che i linfociti B privi di DOT1L producevano in realtà più trascritti nascenti in molti geni marcati da DOT1L — anche se c’era leggermente meno dell’enzima principale di lettura genica, l’RNA polimerasi II, posato su quei geni. Combinando questa misura dell’RNA nascituro con mappe di occupazione della polimerasi, hanno dedotto che, in condizioni normali, i segni istonici di DOT1L funzionano come lievi dossi rallentatori. Rallentano la polimerasi mentre avanza lungo il gene ed estendono brevi pause vicino all’inizio e all’interno del corpo dei geni marcati da DOT1L. Senza DOT1L, la polimerasi corre più veloce e le pause sono più brevi. Poiché AID ha bisogno di finestre temporanee in cui il DNA è esposto e la polimerasi indugia, questa accelerazione riduce paradossalmente la capacità di AID di agganciarsi e svolgere la sua funzione, anche se complessivamente la trascrizione aumenta.
Scollare l’attività genica dal rischio di mutazione
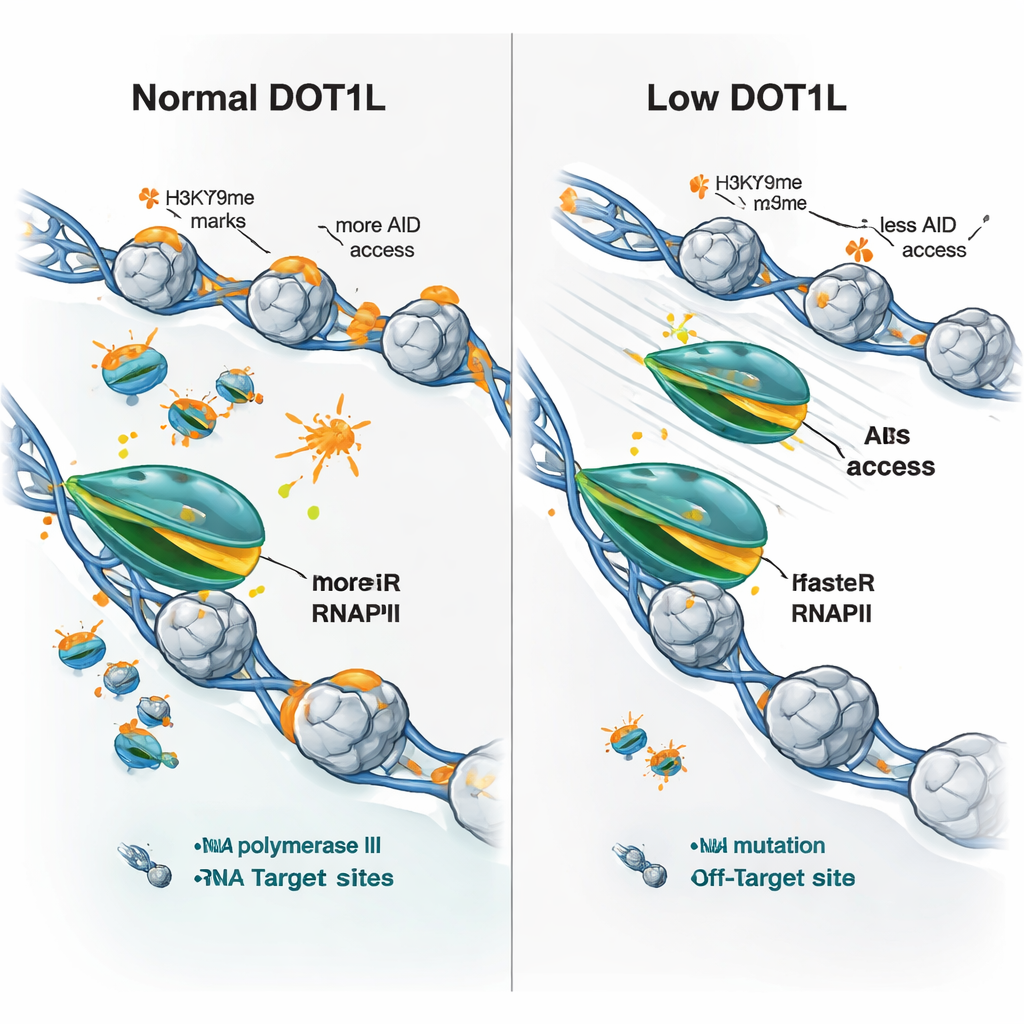
I ricercatori hanno poi chiesto se questi cambiamenti di velocità potessero spiegare il quadro misto di espressione genica osservato quando DOT1L viene perso — alcuni geni aumentano, altri diminuiscono. Hanno scoperto che praticamente tutti i geni marcati da DOT1L condividevano una caratteristica nelle cellule knockout: un allungamento più rapido da parte dell'RNA polimerasi II. Ma l’esito dipendeva dallo stato iniziale. I geni lenti e debolmente espressi tendevano a produrre più RNA quando la polimerasi accelerava, mentre i geni altamente attivi e lunghi con polimerasi già veloci a volte producevano meno, probabilmente perché un transito troppo rapido compromette il processamento o il completamento efficiente. Fondamentale, sia nei geni degli anticorpi sia nei classici off-target di AID, la perdita di DOT1L portava a un movimento più rapido della polimerasi, a meno evidenza di “intasamento” della polimerasi e a una riduzione significativa dell’occupazione di AID, anche quando i livelli di espressione genica non diminuivano.
Perché questo conta per l’immunità e il cancro
Nel complesso, il lavoro dipinge DOT1L come un sottile controllore del traffico per la macchina che legge i geni nei linfociti B. Installando specifici segni istonici, DOT1L rallenta leggermente l’RNA polimerasi II e allunga le sue pause, creando un ambiente trascrizionale in cui AID può interagire produttivamente con i geni degli anticorpi — e, sfortunatamente, con un limitato insieme di altri geni vulnerabili — per introdurre mutazioni. Quando DOT1L manca o è inibito, la polimerasi attraversa i geni più rapidamente, lasciando ad AID meno opportunità di agire, il che attenua la diversificazione degli anticorpi e riduce simultaneamente il rischio di alcuni riarrangiamenti dannosi. Questa intuizione meccanicistica spiega perché la perdita di DOT1L può sia aumentare sia diminuire l’espressione genica, e collega il controllo fine della velocità di trascrizione al luogo in cui il nostro sistema immunitario si permette di riscrivere il proprio DNA.
Citazione: Subramani, P.G., Seija, N., Ridani, J. et al. DOT1L activity limits transcription elongation velocity and favors RNAPII pausing to facilitate mutagenesis by AID. Nat Commun 17, 1623 (2026). https://doi.org/10.1038/s41467-026-68332-4
Parole chiave: diversificazione degli anticorpi, enzima AID, DOT1L, trascrizione genica, linfociti B