Clear Sky Science · it
Progettazione computazionale di ciclopropanasi generaliste con selettività stereodivergente
Perché piccole strutture a tre anelli contano per i farmaci
I ciclopropani—anelli carboniosi a tre atomi—sono blocchi costitutivi piccoli e tesi che possono modificare in modo drastico il comportamento di un farmaco nell’organismo. L’esatta disposizione tridimensionale degli atomi (la stereochimica) può determinare se una molecola diventi un medicinale efficace oppure un analogo inattivo o addirittura dannoso. Questo articolo descrive una strategia computazionale per progettare enzimi in grado di sintetizzare in modo affidabile tutte e quattro le possibili forme 3D di questi anelli a partire dagli stessi reagenti, aprendo la porta a un’esplorazione più rapida e pulita dei candidati farmacologici.
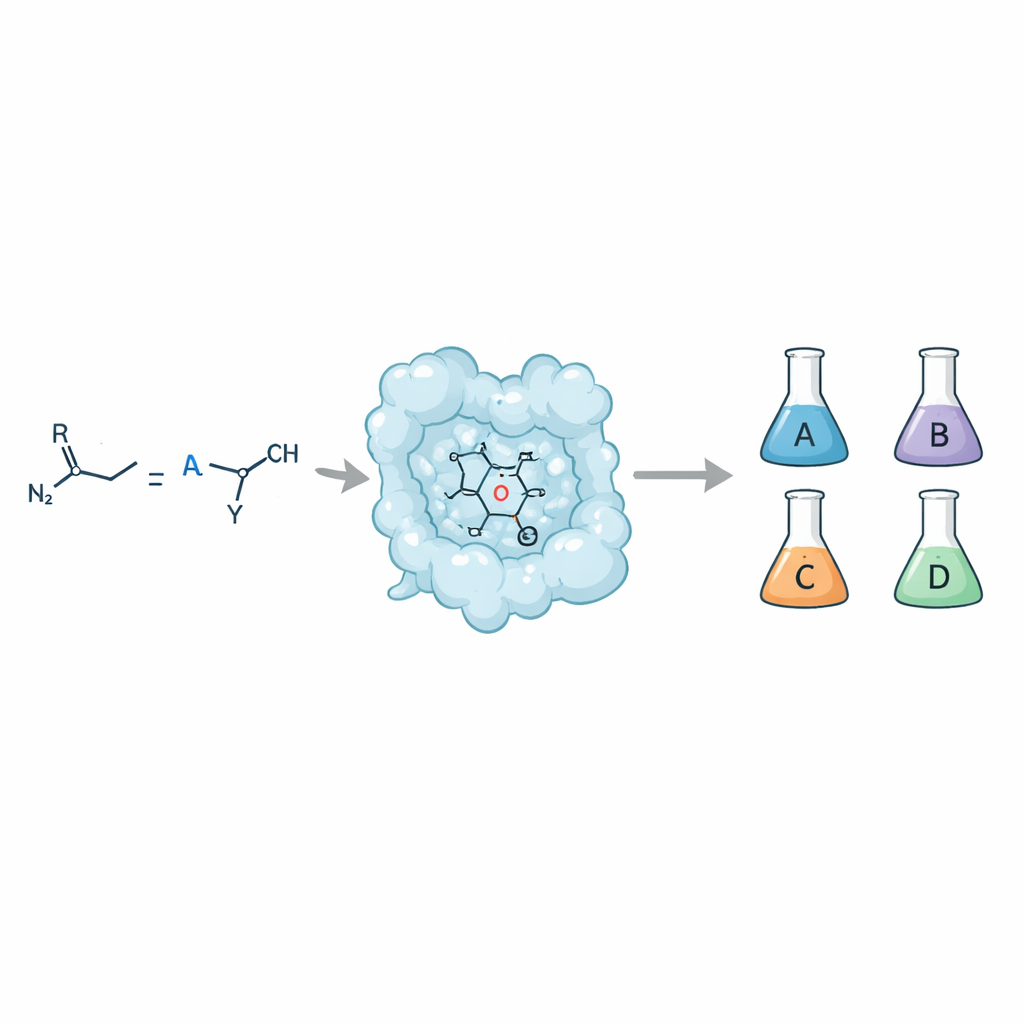
Da una ricetta a quattro risultati diversi
Quando un semplice doppio legame (un olefina) reagisce con un donatore di carbene come un composto diazo, il risultato può essere un anello ciclopropanico. Ma quell’anello può assumere quattro differenti forme stereoisomeriche, tutte con gli stessi atomi ma disposte diversamente nello spazio. I chimici vogliono poter accedere a ciascuna di queste forme perché possono interagire in modo molto diverso con bersagli biologici e influenzare proprietà chiave dei farmaci come assorbimento, metabolismo e sicurezza. I catalizzatori organici tradizionali talvolta offrono questo controllo, ma ottenerlo con enzimi—i catalizzatori della natura—è stato difficile, soprattutto quando si mira a elevata selettività con ampia tolleranza verso substrati diversi.
Progettare enzimi sullo schermo del computer
Gli autori hanno sviluppato un flusso di lavoro computazionale multi‑stato basato sul meccanismo per risolvere questo problema. Hanno prima utilizzato calcoli quantitativi della chimica quantistica per modellare gli effimeri stati di transizione—le strutture ad alta energia lungo il percorso di reazione—for la formazione di ciascuno dei quattro stereoisomeri del ciclopropano. Questi modelli sono stati poi inseriti nei siti attivi di diverse proteine contenenti eme, e il software di progettazione proteica Rosetta è stato usato per valutare quanto ciascuna proteina stabilizzasse o destabilizzasse ogni stato di transizione. In modo cruciale, il punteggio di progettazione premia mutazioni che favoriscono lo stato di transizione desiderato (progettazione positiva) e sfavoriscono quelli concorrenti (progettazione negativa), insegnando efficacemente all’enzima a “preferire” un prodotto 3D rispetto agli altri.
Costruire una cassetta di strumenti enzimatica completa
Con questo approccio, il team ha creato una famiglia di enzimi ciclopropanasi “generalisti”. Partendo dalla mioglobina, hanno riprogettato il suo sito attivo per ottenere varianti che producono il ciclopropano trans-(1R,2R) con selettività molto elevata e buona attività su più di 20 olefine diverse, inclusi substrati poco reattivi e poveri di elettroni. Una mioglobina precedentemente ingegnerizzata forniva già il prodotto complementare trans-(1S,2S). Per raggiungere i due prodotti cis, gli autori si sono rivolti ad altre proteine eme. Hanno rimodellato l’enzima batterico P450cam per ottenere varianti che danno selettivamente il prodotto cis-(1S,2R), e hanno riconvertito la indolamina 2,3‑diossigenasi‑1 umana (IDO1)—non impiegata in precedenza per la chimica dei carbene—per favorire il prodotto cis-(1R,2S). Insieme, questi quattro biocatalizzatori possono fornire ogni stereoisomero dello stesso set di prodotti ciclopropanici, spesso con fino al 99% di controllo sia su diastereoisomeri sia su enantiomeri.
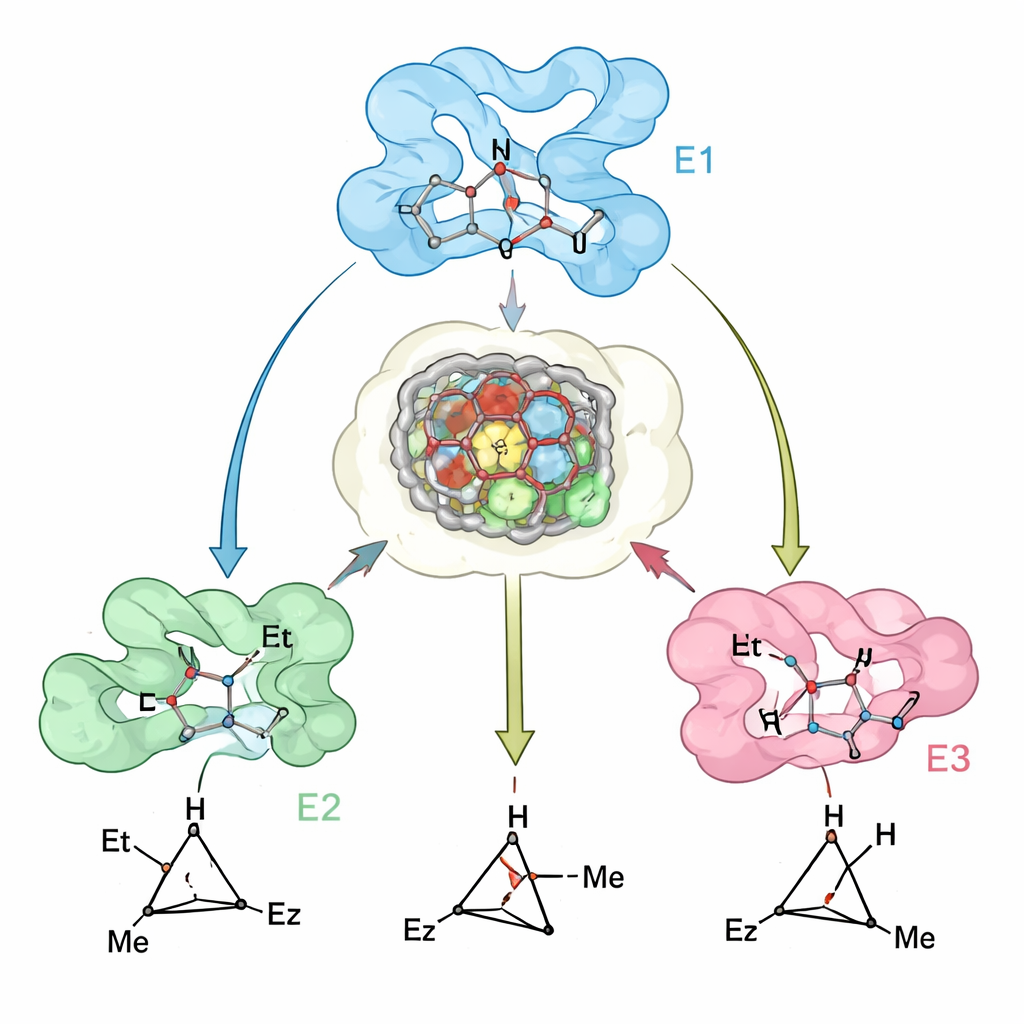
Verificare come la progettazione corrisponde alla realtà
Per testare quanto i loro modelli computazionali rispecchiassero gli enzimi reali, i ricercatori hanno risolto le strutture cristalline di una variante chiave di mioglobina e le hanno confrontate con le strutture previste. L’accordo è stato stretto, e i dati sperimentali hanno evidenziato una caratteristica sottile ma importante: il sito attivo della proteina è pre‑organizzato per accogliere lo stato di transizione preferito, mentre piccoli spostamenti in loop e eliche vicine rendono il legame dello stato di transizione “sbagliato” energeticamente svantaggioso. Dove le previsioni sono state meno accurate—come per alcuni substrati ingombranti—le discrepanze sono state ricondotte a movimenti della catena principale non completamente catturati nella modellizzazione, suggerendo percorsi chiari per migliorare i metodi di progettazione futuri.
Cosa significa questo per i futuri farmaci e catalizzatori
Combinando la modellizzazione degli stati di transizione basata sulla fisica con una riprogettazione proteica intelligente, questo lavoro dimostra che gli esiti stereochimici di reazioni catalizzate da enzimi possono essere programmati in anticipo, invece di essere scoperti solo attraverso evoluzione per prove ed errori. La suite risultante di ciclopropanasi offre ai chimici un modo pratico per ottenere set completi di stereoisomeri del ciclopropano a partire da un’ampia gamma di olefine di partenza, semplificando notevolmente gli studi struttura‑attività nella scoperta di farmaci e nella sintesi di prodotti naturali. La stessa strategia dovrebbe essere adattabile ad altri tipi di enzimi e classi di reazione, accelerando la creazione di biocatalizzatori che forniscono controllo 3D preciso su molecole complesse.
Citazione: Shen, Z., Siriboe, M.G., Ren, X. et al. Computational design of generalist cyclopropanases with stereodivergent selectivity. Nat Commun 17, 1620 (2026). https://doi.org/10.1038/s41467-026-68327-1
Parole chiave: biocatalisi, ciclopropanazione, progettazione di enzimi, stereochimica, proteine eme