Clear Sky Science · it
La glicerolo 3‑fosfato aciltransferasi aggrava la tossicità indotta da α‑sinucleina aumentando la perossidazione lipidica
Perché i grassi nel cervello contano nel Parkinson
La malattia di Parkinson è solitamente descritta come un problema dovuto a una proteina chiamata alpha‑sinucleina che si aggrega e danneggia le cellule cerebrali che controllano il movimento. Questo studio mostra che i grassi cerebrali — in particolare il modo in cui vengono sintetizzati e danneggiati — giocano un ruolo sorprendentemente potente nella tossicità dell’alpha‑sinucleina. Identificando un enzima della sintesi lipidica che peggiora il danno neuronale, il lavoro indica una nuova via farmacologicamente aggredibile che potrebbe integrare gli sforzi esistenti per affrontare il Parkinson alla radice.
Una proteina che si comporta male nel Parkinson
Le persone con Parkinson perdono progressivamente i neuroni produttori di dopamina in una regione profonda del cervello che coordina il movimento. All’interno di queste cellule che muoiono, gli scienziati spesso trovano depositi densi chiamati corpi di Lewy, pieni della proteina alpha‑sinucleina. In famiglie rare, mutazioni o copie extra del gene dell’alpha‑sinucleina causano direttamente il Parkinson, ma le varianti genetiche comuni in quel gene aumentano il rischio solo modestamente. Ciò suggerisce che altri geni e percorsi modulano quanto l’alpha‑sinucleina diventi dannosa. Sempre più prove indicano i lipidi — grassi e molecole simili ai grassi che formano le membrane cellulari e le riserve energetiche — come partner chiave sia nell’aggregazione dell’alpha‑sinucleina sia nella morte neuronale.
Scoprire un enzima lipidico potente nei modelli di moscerino
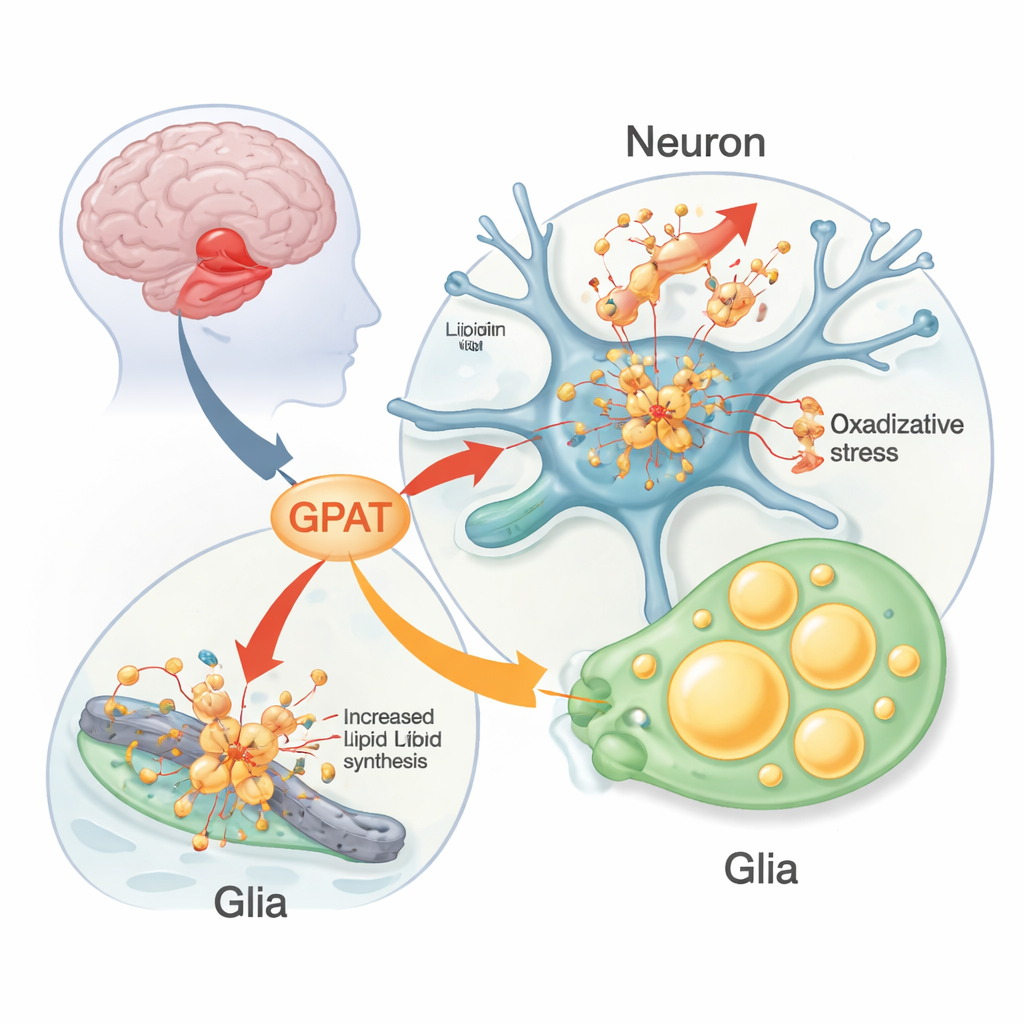
I ricercatori hanno utilizzato moscerini della frutta ingegnerizzati per esprimere l’alpha‑sinucleina umana nel loro sistema nervoso come banco di prova vivo. Questi moscerini sviluppano problemi simili al Parkinson: perdita dei neuroni dopaminergici, difficoltà a salire e ritmi di attività giornaliera alterati. Il team ha alterato sistematicamente le versioni moscerine dei geni di rischio umani per il Parkinson per vedere quali modificavano l’impatto dell’alpha‑sinucleina. Uno è emerso in modo netto: un gene chiamato mino, che codifica una forma mitocondriale dell’enzima glicerolo 3‑fosfato aciltransferasi (GPAT). GPAT si trova al punto di ingresso della sintesi di fosfolipidi e trigliceridi — i lipidi che formano le membrane e le goccioline lipidiche. Quando il team ha ridotto l’attività di mino nei neuroni, i moscerini con alpha‑sinucleina mantenevano più neuroni dopaminergici e si muovevano meglio più a lungo; aumentare l’espressione di mino produceva l’effetto opposto e dannoso.
Grassi danneggiati, mitocondri stressati e goccioline lipidiche nelle cellule gliali
Approfondendo, gli scienziati hanno scoperto che GPAT influenzava la quantità di danno ossidativo accumulato nei lipidi cerebrali. Nei moscerini con alpha‑sinucleina tenuti a temperature più alte (che peggiorano i tratti della malattia), la perossidazione lipidica — la «ruggine» chimica dei grassi — aumentava nelle membrane cerebrali. Ridurre mino diminuiva questo danno, mentre la sua sovraespressione lo aumentava; in assenza di alpha‑sinucleina, modificare mino aveva poco effetto. I marcatori di morte cellulare nella regione cerebrale visiva rispecchiavano questo andamento. Il team ha anche osservato un’impressionante accumulazione di goccioline lipidiche — piccole sfere di stoccaggio di grasso — non nei neuroni stessi ma nelle cellule gliali vicine. Queste goccioline aumentavano con l’età nei moscerini con alpha‑sinucleina e venivano modulati dagli enzimi che sintetizzano o degradano i trigliceridi, evidenziando una partnership metabolica attiva tra neuroni e glia sotto stress.
Rimodellamento metabolico e aggregazione dell’alpha‑sinucleina
Le misurazioni dei metaboliti nei cervelli dei moscerini hanno rivelato che l’espressione di alpha‑sinucleina era collegata a un collo di bottiglia nel ciclo energetico cellulare: citrato e isocitrato, due intermedi del ciclo degli acidi tricarbossilici (TCA), si accumulavano fortemente, mentre i passaggi a valle variavano in misura più modesta. Anche i livelli di lattato aumentavano, coerentemente con una glicolisi potenziata. Allo stesso tempo, un profilo lipidico dettagliato mostrava cambiamenti nell’equilibrio dei fosfolipidi di membrana e nella composizione degli acidi grassi, favorendo specie più suscettibili al danno ossidativo. Quando il team riduceva diversi enzimi GPAT — mino nei mitocondri e enzimi correlati nel reticolo endoplasmatico — l’alpha‑sinucleina continuava ad accumularsi, ma la sua tendenza a formare oligomeri di ordine superiore (complessi multi‑proteici) diminuiva, e i mitocondri mostravano meno segni di stress ossidativo e «invecchiamento».
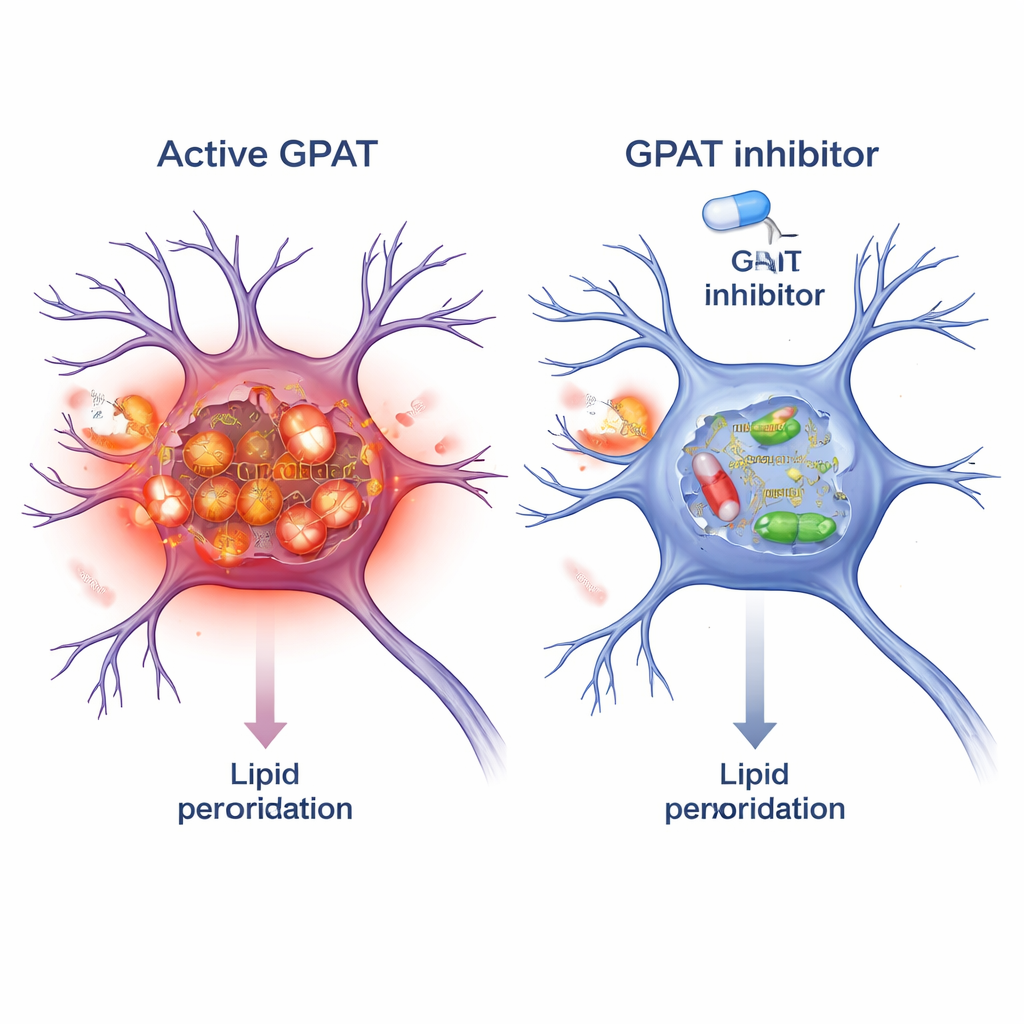
Bloccare GPAT come strategia protettiva
Poiché GPAT è un enzima, può essere preso di mira da piccole molecole. I ricercatori hanno testato FSG67, un inibitore di GPAT esistente sviluppato originariamente per obesità e diabete. Nei moscerini con alpha‑sinucleina, aggiungere FSG67 al cibo ha riprodotto i benefici dell’abbassamento genetico di GPAT: miglioramento del movimento, maggiore sopravvivenza dei neuroni dopaminergici, meno oligomeri dannosi di alpha‑sinucleina e riduzione dello stress ossidativo mitocondriale. Per valutare se il concetto valesse anche nei mammiferi, hanno trattato neuroni cerebrali murini in coltura con fibrille preformate di alpha‑sinucleina, che favoriscono la formazione di aggregati tossici. Il trattamento combinato con FSG67 ha ridotto l’accumulo di alpha‑sinucleina fosforilata e abbassato diversi marcatori indipendenti di perossidazione lipidica all’interno di questi neuroni.
Cosa significa per le persone con Parkinson
In termini semplici, questo lavoro mostra che il modo in cui il cervello gestisce i grassi può modulare la tossicità dell’alpha‑sinucleina. Quando GPAT è molto attivo, nei membrane e nelle goccioline di stoccaggio vengono incorporate più specie lipidiche vulnerabili, che diventano più facili da ossidare; questo ambiente di grassi danneggiati sembra favorire forme dannose di alpha‑sinucleina e mettere sotto stress i mitocondri, le centrali energetiche della cellula. Ridurre l’attività di GPAT — sia geneticamente sia con un farmaco — sposta l’equilibrio verso meno «ruggine» lipidica, meno assemblaggi proteici tossici e neuroni più sani. Pur essendo risultati preliminari ottenuti in moscerini e in cellule murine coltivate, questi dati mettono in luce il metabolismo lipidico, e in particolare GPAT, come un promettente nuovo indirizzo per terapie del Parkinson che potrebbero integrare le strategie che mirano direttamente all’alpha‑sinucleina.
Citazione: Ren, M., Lim, G.G.Y., Tang, W. et al. Glycerol 3-phosphate acyltransferase exacerbates α-synuclein-induced toxicity by increasing lipid peroxidation. Nat Commun 17, 1618 (2026). https://doi.org/10.1038/s41467-026-68325-3
Parole chiave: Malattia di Parkinson, alpha-sinucleina, perossidazione lipidica, inibitore GPAT, neurodegenerazione