Clear Sky Science · it
Vaccino per KRAS mutante con doppio blocco dei checkpoint nel cancro del pancreas asportato: uno studio di fase I
Nuove speranze contro un cancro mortale
Il cancro del pancreas è tra i tumori più letali, in gran parte perché si diffonde precocemente e spesso ritorna anche dopo intervento chirurgico e chemioterapia. Questo studio esplora un nuovo tipo di “programma di addestramento” per il sistema immunitario: un vaccino progettato per riconoscere le mutazioni comuni in un gene oncogenico chiamato KRAS, combinato con due farmaci immunoterapici moderni. Per le persone a cui sono già stati rimossi i tumori pancreatici, questo approccio mira a eliminare i semi invisibili di cancro prima che ricrescano.
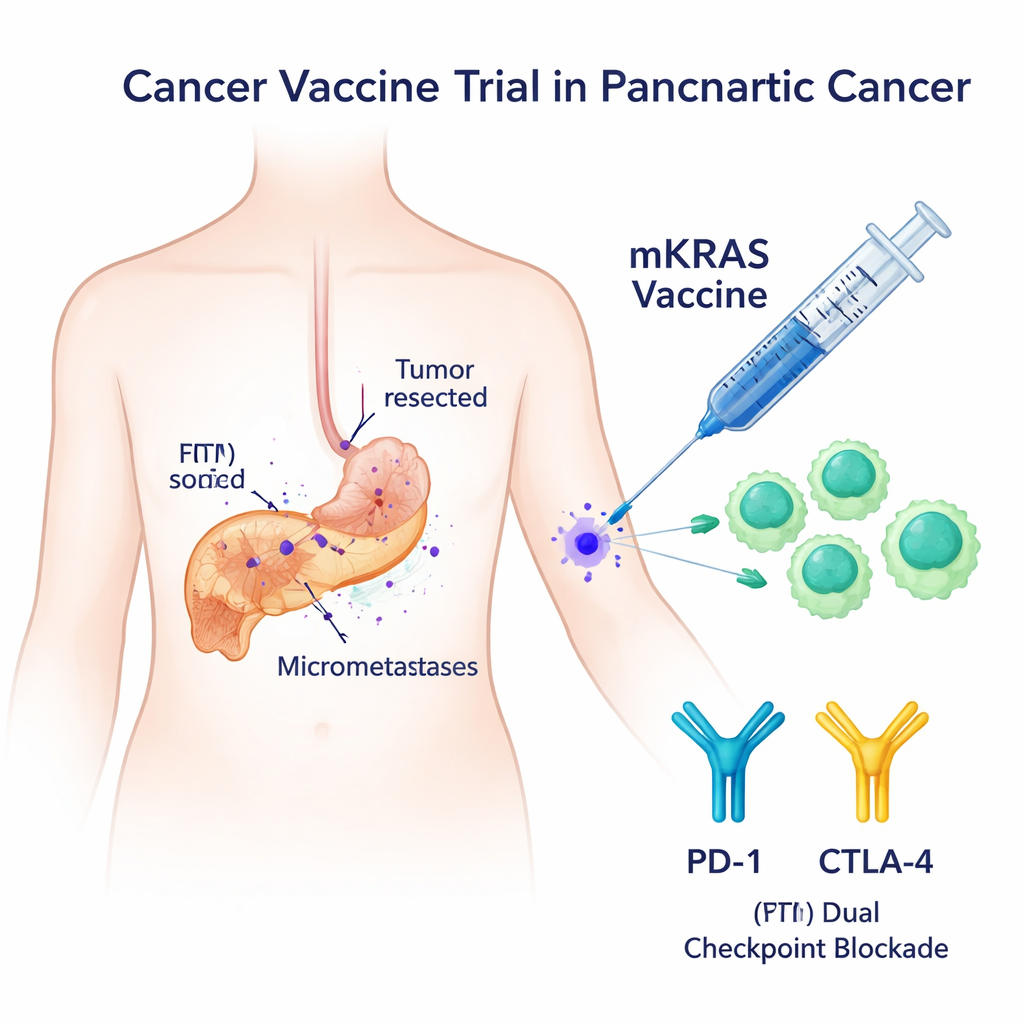
Un bersaglio preciso: KRAS mutante
La maggior parte dei tumori pancreatici presenta alterazioni nel gene KRAS che funzionano come un accelleratore bloccato per la crescita cellulare. Queste versioni mutate — come G12V, G12D, G12R, G12C, G12A e G13D — sono quasi assenti nei tessuti sani, rendendole bersagli molto attraenti per il sistema immunitario. Tentativi precedenti di vaccini mirati a KRAS hanno mostrato risposte immunitarie solo modeste e si sono generalmente concentrati su una o due mutazioni. In questo studio di fase I, i ricercatori hanno testato un vaccino più ampio, chiamato mKRAS-VAX, che combina sei lunghi peptidi rappresentativi delle mutazioni KRAS più comuni e li associa a due farmaci “checkpoint”, nivolumab e ipilimumab, che aiutano a liberare le cellule T che altrimenti potrebbero essere trattenute.
Progettare e somministrare la strategia vaccinale
Lo studio ha arruolato 12 persone i cui tumori pancreatici erano stati rimossi chirurgicamente e che avevano completato la chemioterapia standard, ma che comunque avevano un alto rischio di recidiva. Il tumore di ciascun partecipante presentava una delle sei mutazioni KRAS incluse nel vaccino. Durante una fase iniziale di “priming”, i pazienti hanno ricevuto quattro cicli del cocktail peptidico mescolato con un adiuvante stimolante il sistema immunitario, insieme ai due farmaci checkpoint. A questo è seguito un programma di richiami, e alcuni pazienti rimasti liberi da malattia dopo un anno hanno continuato con richiami vaccinali da soli. Le domande principali erano se questa combinazione fosse sicura e se aumentasse in modo rilevabile le cellule T dirette contro KRAS nel sangue.
Addestrare e monitorare le cellule immunitarie
Campioni di sangue prelevati prima e dopo la vaccinazione sono stati esposti a ciascun peptide KRAS per valutare quante cellule T producevano interferone-gamma, un mediatore chiave dell’attività immunitaria. I risultati sono stati notevoli per uno studio di piccole dimensioni: 11 dei 12 pazienti hanno mostrato un aumento significativo delle cellule T che riconoscevano complessivamente i peptidi KRAS mutanti, e 10 dei 12 hanno montato una forte risposta contro la specifica mutazione KRAS del proprio tumore. Molti pazienti hanno risposto a diverse delle sei varianti KRAS, e alcune cellule T potevano riconoscere più di una mutazione, suggerendo un grado di cross-reattività utile. Il profilo dettagliato ha mostrato che la maggior parte di queste cellule indotte dal vaccino erano cellule T CD4 “helper” con caratteristiche di memoria, supportate da un gruppo più piccolo ma importante di cellule T citotossiche CD8 capaci di uccidere. Il team ha inoltre mappato e clonato centinaia di recettori di cellule T specifici per KRAS, inclusi alcuni recettori “pubblici” condivisi tra pazienti diversi, che potrebbero essere preziosi per future terapie cellulari.
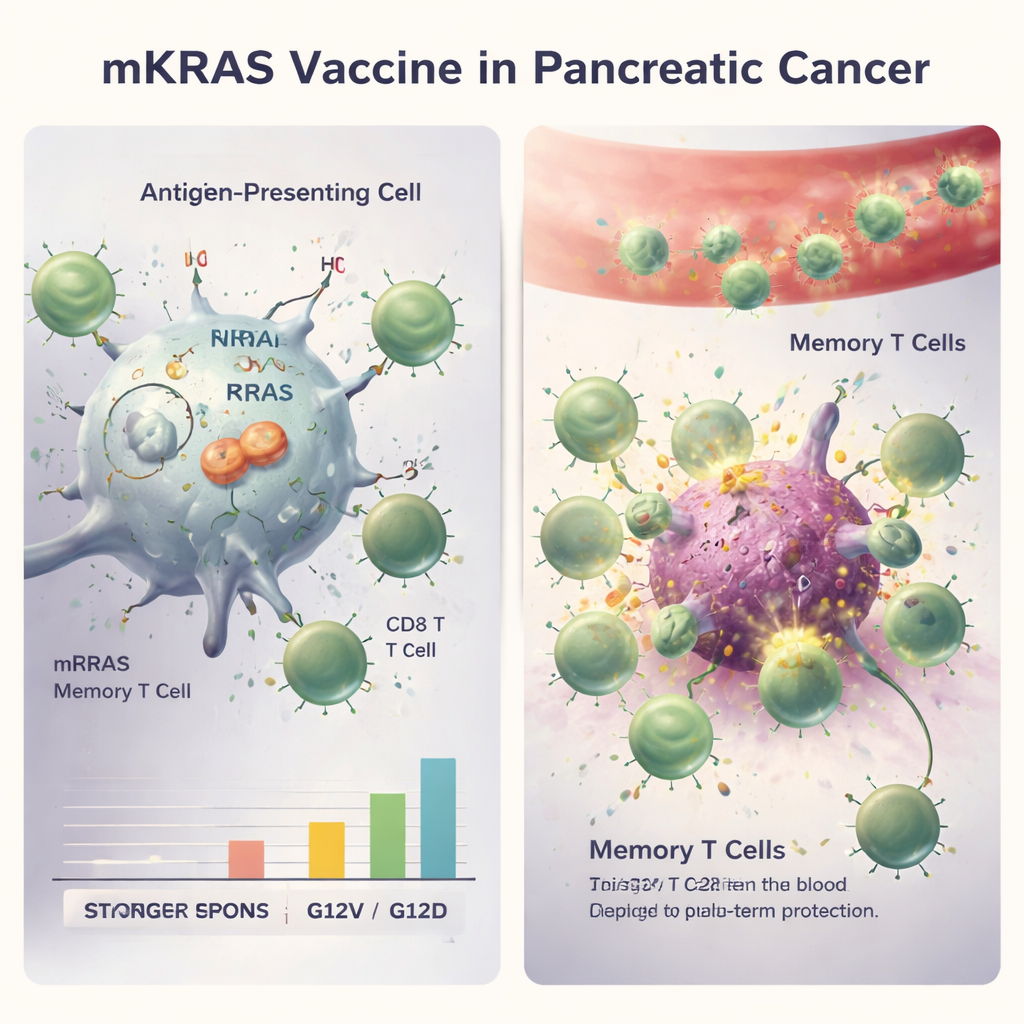
Primi segnali clinici e differenze tra mutazioni
Pur non essendo lo studio sufficientemente ampio per dimostrare un beneficio di sopravvivenza, ci sono stati segnali incoraggianti. I pazienti le cui risposte delle cellule T mirate a KRAS rientravano nel 75% superiore tendevano a rimanere liberi da malattia rilevabile più a lungo rispetto a quelli con risposte più deboli. Dopo circa tre anni di follow-up, un terzo dei partecipanti risultava ancora libero da malattia. Tutti e quattro i pazienti ancora liberi da cancro all’ultimo controllo avevano tumori KRAS G12V o G12R, e le loro cellule T specifiche per KRAS sono persistite per più di un anno, in particolare le cellule CD4 di memoria. Al contrario, i tumori con la mutazione G12D non solo hanno risposto meno a livello immunitario ma erano anche più propensi a recidivare, in linea con altri studi che collegano G12D a una malattia più aggressiva. È importante notare che gli effetti collaterali legati al vaccino sono stati lievi (principalmente dolore locale, affaticamento e febbre), mentre le complicanze immunitarie più gravi derivavano dai farmaci checkpoint piuttosto che dal vaccino stesso.
Cosa potrebbe significare per i pazienti futuri
In termini semplici, questo trial mostra che un vaccino “pronto all’uso” mirato a più bersagli KRAS mutati, quando combinato con i moderni farmaci checkpoint, può risvegliare in sicurezza una risposta ampia e duratura delle cellule T nella maggior parte delle persone con cancro del pancreas ad alto rischio. Sebbene molti pazienti abbiano comunque visto la malattia ricomparire, coloro che hanno sviluppato risposte immunitarie più forti focalizzate su KRAS tendevano ad avere esiti migliori, suggerendo che potenziare ulteriormente queste risposte — o iniziare la vaccinazione prima — potrebbe migliorare i risultati. Il ricco catalogo di recettori di cellule T specifici per KRAS scoperto qui apre anche la strada a terapie con cellule ingegnerizzate. Nel complesso, questi risultati suggeriscono che trasformare KRAS, da noto driver tumorale, in una bandiera riconoscibile dal sistema immunitario potrebbe diventare una strategia chiave per prevenire la recidiva del cancro del pancreas.
Citazione: Huff, A.L., Haldar, S.D., Gergis, A.A. et al. Mutant KRAS vaccine with dual checkpoint blockade in resected pancreatic cancer: a phase I trial. Nat Commun 17, 1538 (2026). https://doi.org/10.1038/s41467-026-68324-4
Parole chiave: vaccino per il cancro del pancreas, KRAS mutante, immunoterapia, risposta delle cellule T, blocco dei checkpoint