Clear Sky Science · it
La struttura del complesso SHOC2-KRAS-PP1C rivela determinanti specifici per le isoforme RAS e indicazioni per mirare l’assemblaggio del complesso con inibitori di RAS
Come le cellule decidono quando crescere
Le nostre cellule si affidano a un sistema di cablaggio interno per decidere quando crescere, dividersi o rimanere inattive. Al centro di questo sistema ci sono le proteine RAS, piccoli interruttori molecolari che spesso si guastano nel cancro. Questo studio esplora in profondità come un particolare gruppo di proteine—SHOC2, RAS e PP1C—si unisce per azionare un importante interruttore di crescita e come i farmaci oncologici moderni possano essere tarati per bloccare più efficacemente questo processo e impedire ai tumori di eludere il trattamento.
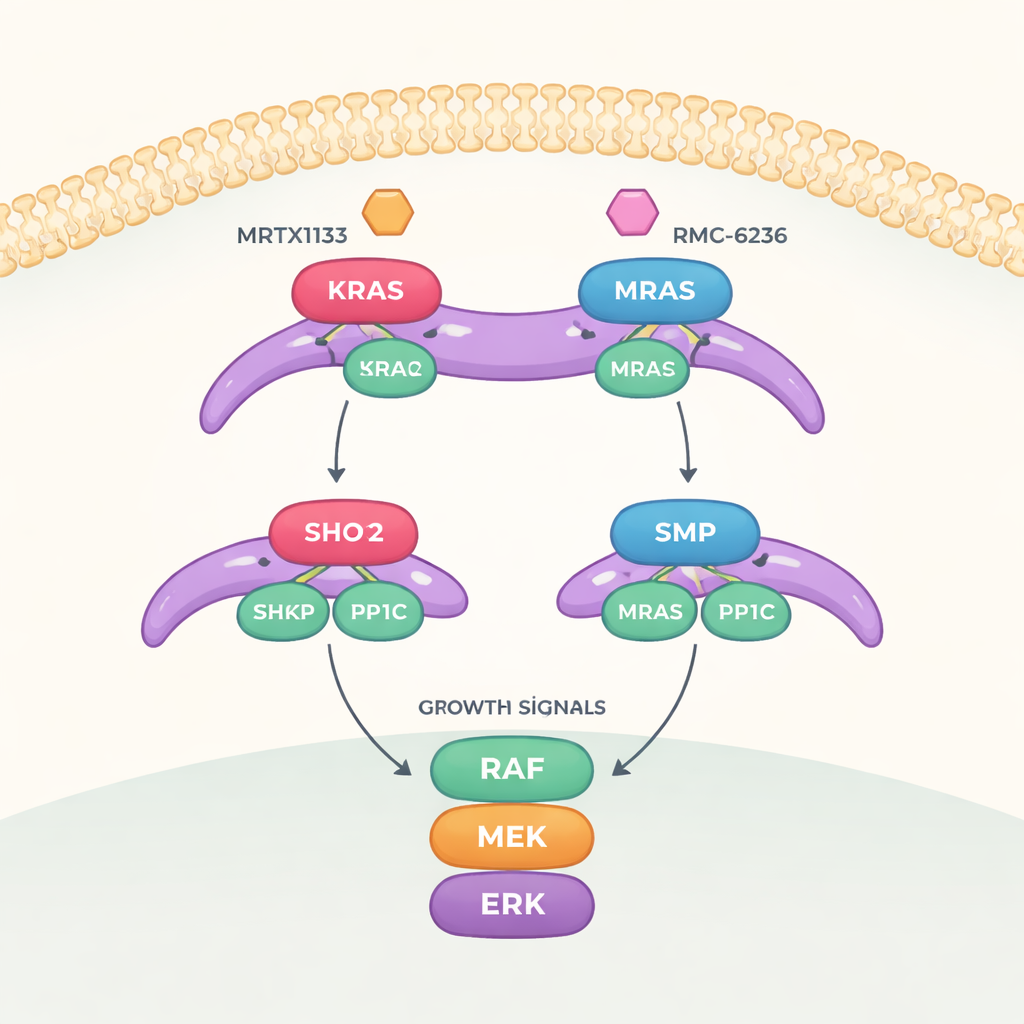
Un interruttore di crescita con tre parti critiche
Il lavoro si concentra su una via di segnalazione chiamata MAPK, che trasmette i segnali di crescita dalla superficie cellulare fino al nucleo. Per attivare completamente questa via, un’altra proteina chiamata RAF deve essere commutata dallo stato “spento” a quello “acceso”. Questo interruttore è controllato da un complesso a tre componenti formato da SHOC2 (uno scaffold che tiene insieme i componenti), PP1C (un enzima che rimuove un gruppo fosfato) e una proteina RAS attiva. Quando si assemblano, queste tre componenti rimuovono un marcatore fosfato specifico da RAF, liberandola per attivare la cascata di crescita a valle.
Perché un partner a bassa affinità conta comunque nel cancro
Esistono diversi tipi di proteine RAS. MRAS forma un complesso molto stabile con SHOC2 e PP1C, mentre i più noti driver oncogenici KRAS, HRAS e NRAS generano versioni più deboli dello stesso complesso. Sorprendentemente, le cellule tumorali guidate da KRAS, HRAS o NRAS mutati risultano fortemente dipendenti da SHOC2, nonostante i loro complessi siano meno stabili. Grandi dataset di screening genetici mostrano che molti tumori con certe mutazioni di RAS—in particolare quelle che colpiscono posizioni chiave come Q61 e G13—sono altamente sensibili alla perdita di SHOC2, il che indica che questo assemblaggio è essenziale per la loro sopravvivenza.
Rivelare la forma del complesso con KRAS
Finora gli scienziati avevano osservato solo la struttura ad alta risoluzione del complesso basato su MRAS, molto stabile. La versione più debole con KRAS si dissociava troppo facilmente per essere catturata. In questo studio, gli autori hanno utilizzato mutazioni legate a malattie che rafforzano lievemente i contatti tra i componenti per stabilizzare il complesso SHOC2–KRAS–PP1C abbastanza a lungo da poterlo visualizzare con crio-microscopia elettronica. Hanno scoperto che l’architettura generale corrisponde strettamente a quella del complesso con MRAS, ma KRAS manca di alcune piccole caratteristiche strutturali che MRAS usa per aggrapparsi più saldamente a SHOC2 e PP1C. Di conseguenza, l’assemblaggio con KRAS espone un’area di contatto minore e forma meno legami, il che spiega la sua intrinseca minore stabilità, pur restando estremamente importante nei tumori in cui KRAS è iperattivo.
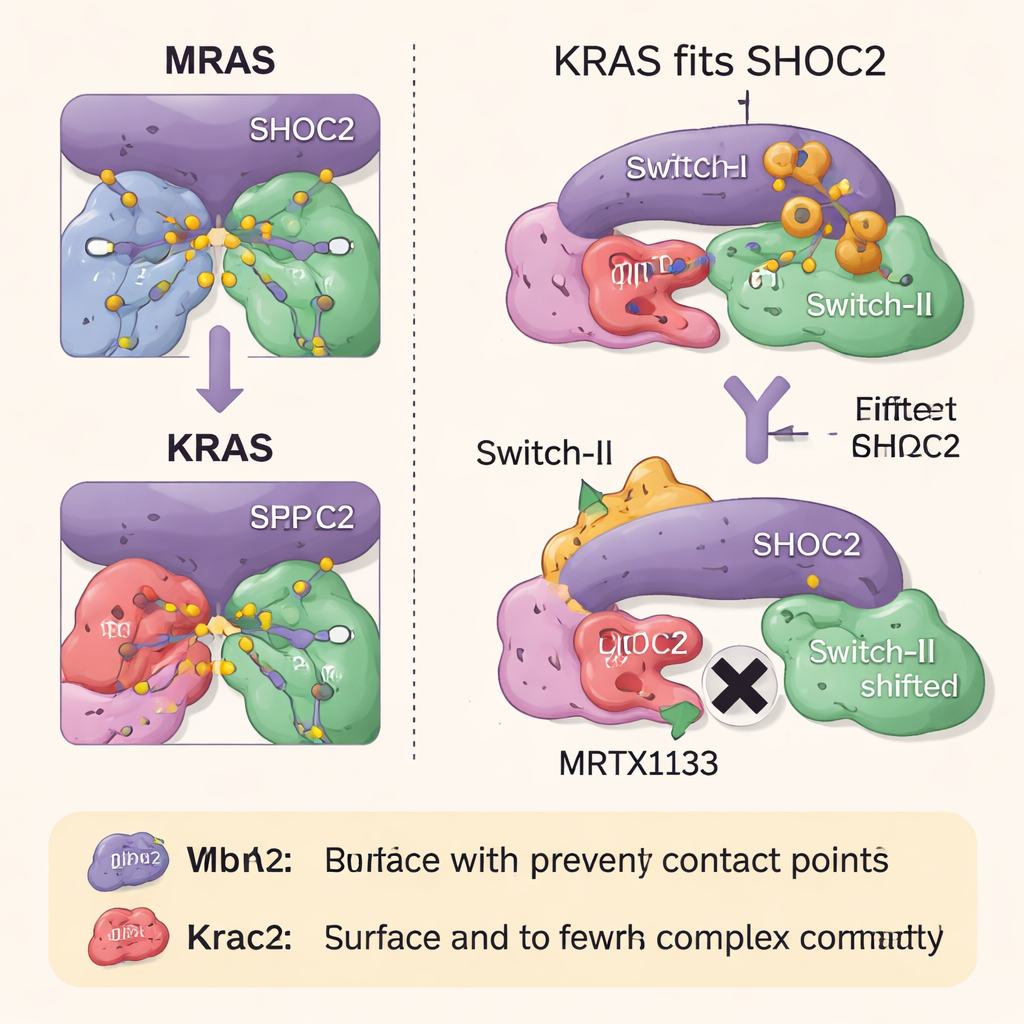
Come i farmaci contro RAS bloccano l’assemblaggio del complesso
Il gruppo ha quindi esplorato come due classi di farmaci mirati a RAS influenzino questo complesso a tre componenti. MRTX1133, progettato per legare una tasca vicino a una regione flessibile di KRAS nota come Switch-II, blocca questa regione in una conformazione che entra in conflitto con la superficie di SHOC2. Questo impedisce fortemente la formazione di nuovi complessi SHOC2–KRAS–PP1C, anche se è meno efficace nello spezzare quelli già esistenti. Un secondo farmaco, RMC-6236, agisce insieme a una proteina helper (ciclophilina A) e blocca anch’esso le stesse superfici di KRAS necessarie per il legame con SHOC2. Tuttavia, nessuno dei due farmaci si lega naturalmente a MRAS, quindi il complesso ad alta affinità con MRAS resta intatto e può contribuire a riattivare la via di crescita quando KRAS è inibito.
Verso un doppio bersaglio per prevenire la resistenza
Per verificare se il doppio targeting fosse possibile, i ricercatori hanno ingegnerizzato una variante di MRAS la cui tasca Switch-II è stata modificata in modo che MRTX1133 potesse legarsi. Questo mutante formava ancora un complesso forte con SHOC2 e PP1C, ma il farmaco ora bloccava il suo assemblaggio e riduceva la sua capacità di attivare RAF in saggi in provetta. Uniti ai dati su composti che interferiscono con il legame a SHOC2, questi risultati mostrano che è realistico progettare farmaci che spengano sia i complessi basati su KRAS sia quelli basati su MRAS. Per un lettore non specialistico, il messaggio chiave è che le cellule tumorali usano più interruttori strettamente correlati per mantenere il flusso dei segnali di crescita, soprattutto quando un interruttore viene bersagliato dal farmaco. Capendo le forme precise e i contatti all’interno di questi assemblaggi proteici, i ricercatori possono ora pianificare terapie che colpiscano entrambe le vie di riserva contemporaneamente, rendendo più difficile per i tumori guidati da RAS adattarsi e sviluppare resistenza al trattamento.
Citazione: Bonsor, D.A., Finci, L.I., Potter, J.R. et al. Structure of SHOC2-KRAS-PP1C complex reveals RAS isoform-specific determinants and insights into targeting complex assembly by RAS inhibitors. Nat Commun 17, 1614 (2026). https://doi.org/10.1038/s41467-026-68319-1
Parole chiave: segnalazione RAS, inibitori di KRAS, via MAPK, complessi proteici, resistenza ai farmaci