Clear Sky Science · it
Regolazione del pH reversibile mediata da lipidi di connexin-46/50 mediante crio-EM
Perché i minuscoli canali cellulari sono importanti per la salute e la malattia
Ogni secondo, le nostre cellule scambiano segnali elettrici e piccole molecole attraverso tunnel microscopici chiamati giunzioni comunicanti. Questi canali aiutano il cuore a battere all’unisono, il cervello a eliminare sottoprodotti tossici e il cristallino a rimanere trasparente. Quando le condizioni interne delle cellule diventano acide, come avviene durante ictus, infarto o nella formazione di cataratta, molti di questi canali si chiudono: come percepiscano e rispondano all’acidità è stato a lungo un mistero. Questo studio utilizza la criomicroscopia elettronica ad alta risoluzione per rivelare, quasi atomo per atomo, come specifici canali del cristallino si chiudano in risposta all’acido e come questo processo possa essere completamente reversibile.
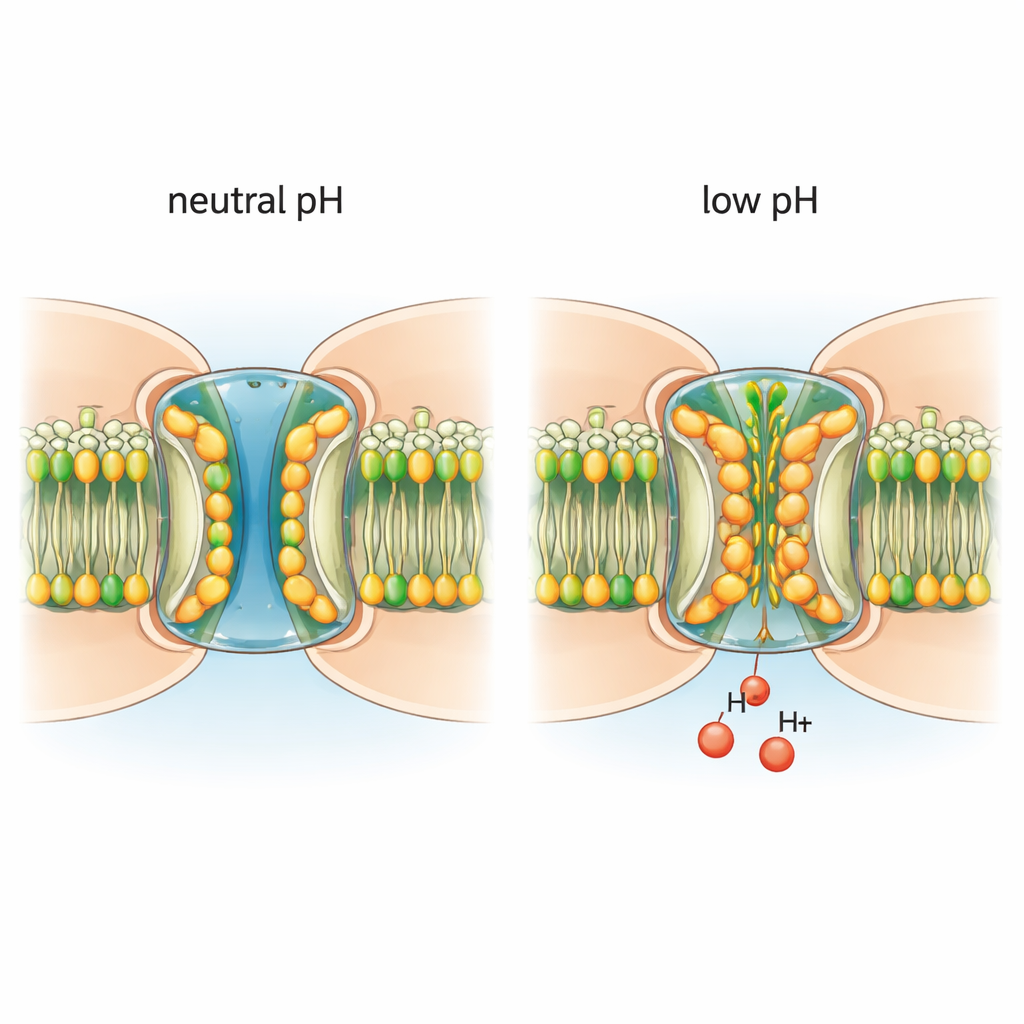
Tunnel cellulari che mantengono i tessuti sincronizzati
Le giunzioni comunicanti sono costituite da proteine chiamate connexine, che si assemblano in canali ad anello che attraversano le membrane di due cellule vicine. Questo lavoro si concentra su una coppia di connexine strettamente correlate, connexin-46 e connexin-50, che formano canali nel cristallino dell’occhio. Questi canali permettono il passaggio diretto di ioni e piccole molecole tra le cellule, aiutando a mantenere la trasparenza del cristallino e la salute del tessuto. Tuttavia, quando le cellule sono sottoposte a stress, gli stessi canali possono diventare vie di propagazione per segnali dannosi. Per proteggere i tessuti, le giunzioni comunicanti si chiudono quando l’interno della cellula diventa più acido. Comprendere il meccanismo su piccola scala di questa “regolazione dal pH” è importante per decifrare come i tessuti sopravvivono allo stress e perché alcune mutazioni portano a malattie come le cataratte.
Osservare il movimento dei canali con la crio‑EM
I ricercatori hanno purificato canali nativi di connexin-46/50 da cristallini di pecore anziane e li hanno incorporati in una membrana modello. Usando la criomicroscopia elettronica, hanno immaginato i canali a risoluzione quasi atomica in condizioni neutre, che favoriscono un poro aperto, e in condizioni leggermente acide, che innescano la chiusura. A pH neutro, i canali adottano in gran parte uno stato aperto stabile, con un tunnel centrale sufficientemente largo per ioni e piccole molecole e con un segmento flessibile, il dominio N‑terminale, che riveste l’ingresso del poro. In queste condizioni il poro è pulito: non ci sono molecole aggiuntive a ostruire il passaggio e i lipidi della membrana circostante restano organizzati in strati regolari.
L’acidità attrae i lipidi nel poro
Quando l’ambiente è stato reso leggermente acido, l’architettura del canale è cambiata in modo sorprendente. Molecole lipidiche della membrana circostante sono state attirate all’interno del poro, insinuandosi tra e sotto i segmenti N‑terminali. Questi lipidi invasori formano una “guarnizione” idrofobica a due strati che spinge i domini N‑terminali verso l’interno, restringendo il canale e contribuendo a bloccare il transito. Altri lipidi si inseriscono tra subunità proteiche adiacenti alle loro interfacce, apparentemente servendo da percorsi di ingresso dalla membrana al poro. È importante sottolineare che, quando i canali sono stati posti in un ambiente detergente privo di una vera membrana lipidica, il pH basso non ha più indotto questi cambiamenti strutturali. Ciò dimostra che i lipidi reali non sono meri spettatori: sono partner necessari nel processo di regolazione dal pH.
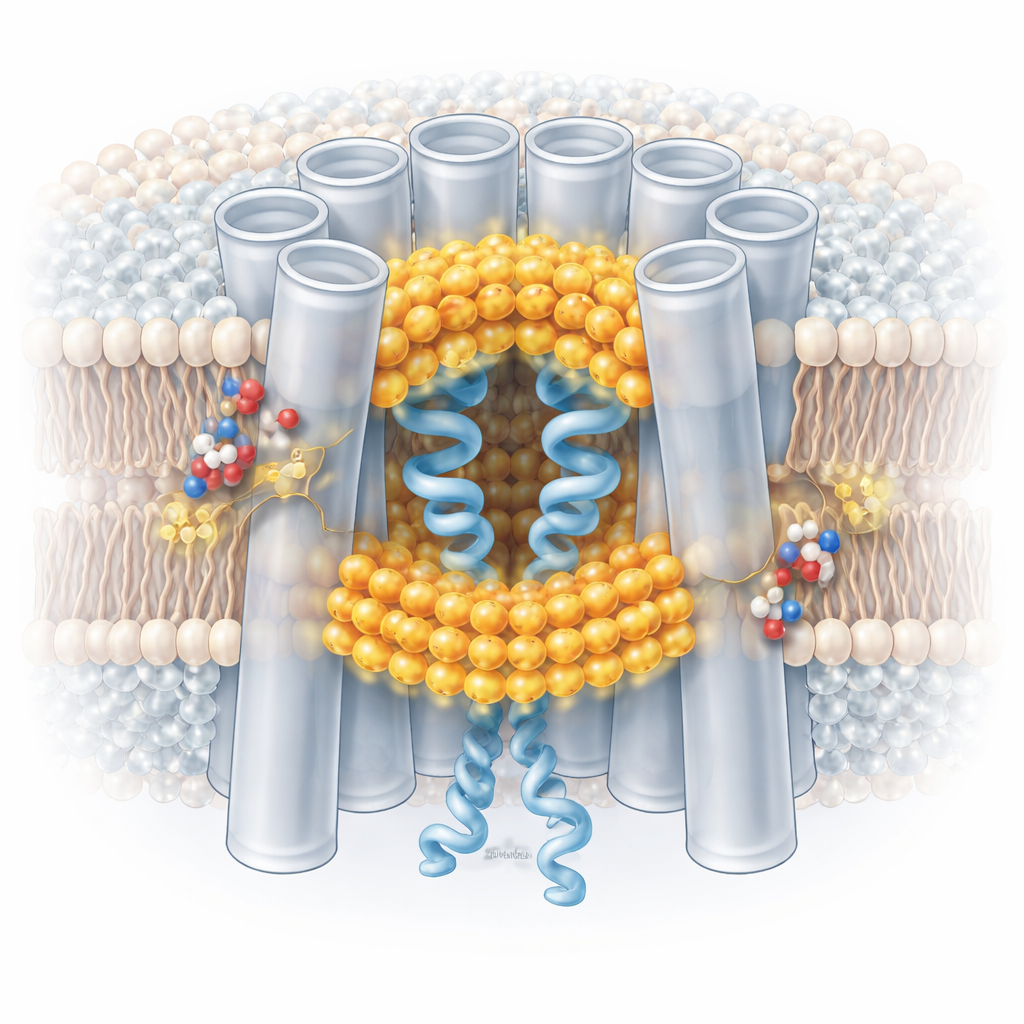
Un interruttore di sicurezza reversibile e finemente regolato
Tracciando milioni di particelle di canale individuali, gli autori hanno scoperto che il pH basso non trasforma semplicemente i canali da completamente aperti a completamente chiusi. Invece, sposta la popolazione verso una miscela di stati: alcune subunità all’interno di un canale mostrano conformazioni chiuse stabilizzate dai lipidi mentre altre restano più aperte. Il comportamento di gating è in gran parte non cooperativo: ogni elemento costitutivo del canale può rispondere in modo abbastanza indipendente. Le condizioni acide favoriscono queste conformazioni chiuse, ma quando il pH ritorna neutro, i lipidi del poro rientrano nella membrana e i canali ritornano allo stato aperto. Aminoacidi conservati chiamati istidine, che acquisiscono carica positiva a basso pH, sembrano contribuire a reclutare e stabilizzare i lipidi interfacciali che iniziano questo processo, offrendo un plausibile sensore molecolare del pH.
Implicazioni per le cataratte e la protezione dei tessuti
Questi risultati supportano un modello in cui i lipidi agiscono come tappi mobili che controllano in modo reversibile il flusso attraverso le giunzioni comunicanti in risposta all’acidità. Nel cristallino, un tale meccanismo potrebbe aiutare a isolare le cellule danneggiate e prevenire la diffusione di segnali tossici, ma un gating cronico o mal regolato potrebbe anche contribuire alla formazione di cataratta legata all’età. Poiché intrusioni lipidiche simili sono state osservate in famiglie di canali correlate, il lavoro suggerisce un principio più generale: sotto stress, le membrane cellulari stesse possono fornire componenti dinamici che aiutano ad accendere o spegnere canali vitali, offrendo nuove idee per farmaci che stabilizzino lo stato aperto o chiuso nelle malattie.
Citazione: Jarodsky, J.M., Myers, J.B. & Reichow, S.L. Reversible lipid-mediated pH-gating of connexin-46/50 by cryo-EM. Nat Commun 17, 1606 (2026). https://doi.org/10.1038/s41467-026-68311-9
Parole chiave: giunzioni comunicanti, connexin 46/50, regolazione dal pH, cataratta, crio-EM