Clear Sky Science · it
La trascrittomica single-cell dinamica rivela la formazione di reti neurali guidate da lsamp nei maschi di S. japonicum che attivano la riproduzione femminile
Perché la vita amorosa di un parassita è importante
La schistosomiasi è una malattia parassitaria che colpisce oltre 250 milioni di persone, principalmente in regioni più povere con accesso limitato alle cure mediche. La patologia non è causata dalle morsicature o dalle tossine dei vermi, ma dall’enorme quantità di uova deposte dalle femmine all’interno dell’organismo. Sorprendentemente, le femmine maturano e iniziano a deporre uova solo dopo l’accoppiamento con un maschio. Questo studio pone una domanda semplice ma cruciale: cosa fa esattamente il maschio per attivare la fertilità della femmina — e sarebbe possibile spegnere questo interruttore per fermare la malattia?
Mappare un mondo nascosto cellula per cellula
Per rispondere, i ricercatori hanno costruito un dettagliato “atlante cellulare” del trematode ematico Schistosoma japonicum durante la finestra chiave in cui maschi e femmine si accoppiano e maturano sessualmente. Utilizzando la RNA-seq a singola cellula, una tecnica che legge quali geni sono attivi in cellule individuali, hanno analizzato più di 100.000 cellule provenienti da vermi raccolti in quattro momenti dopo l’infezione nei topi. Hanno identificato 76 tipi cellulari distinti, inclusi molti tipi di neuroni, cellule staminali e cellule riproduttive. Questo ha permesso di seguire come specifiche popolazioni cellulari si espandono, si riducono o cambiano identità mentre i vermi crescono e iniziano a riprodursi.
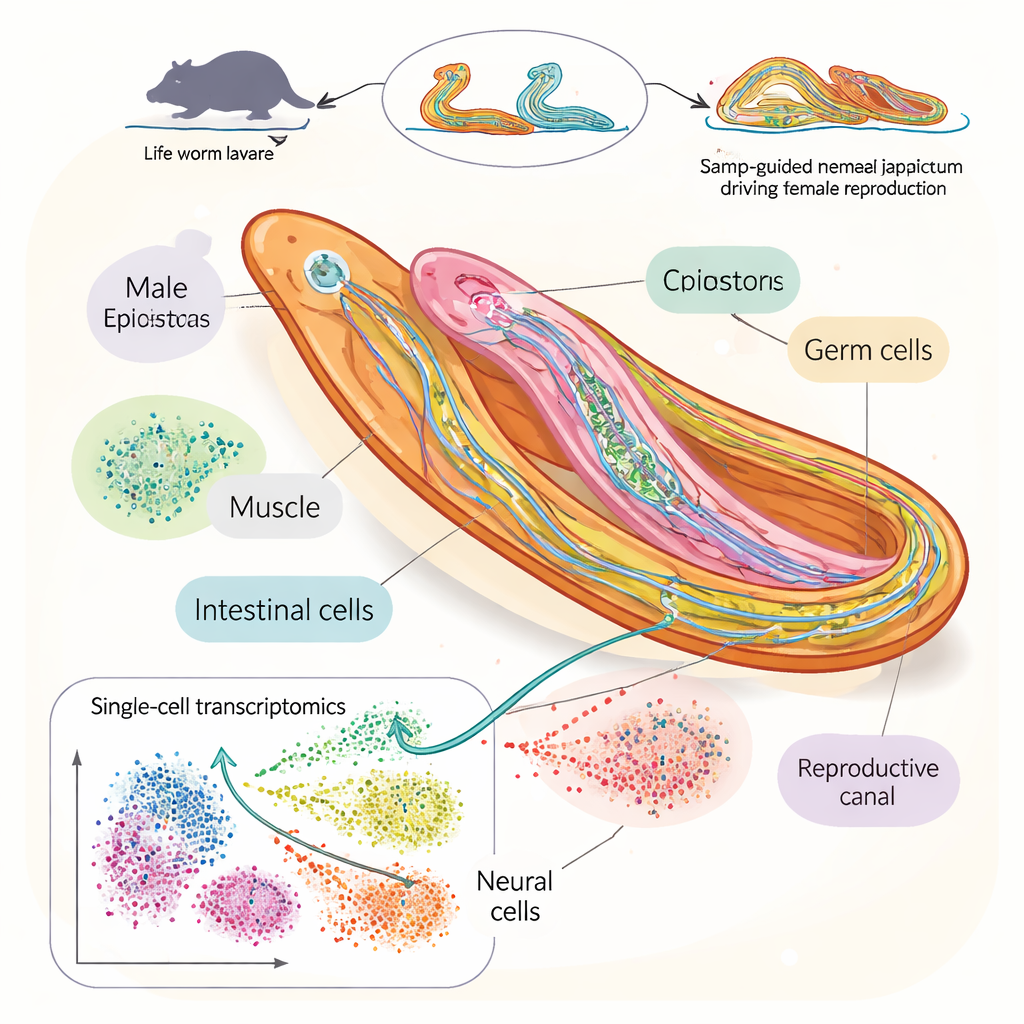
Seguire l’ascesa di uova e spermatozoi
Ingrandendo le cellule dei testicoli, delle ovaie e dei tessuti correlati, il gruppo ha ricostruito lo sviluppo graduale di spermatozoi e ovociti. Hanno mostrato come le cellule germinali staminali danno origine a cellule spermatiche e ovocitarie in stadi tardivi attraverso programmi di espressione genica distinti nei maschi e nelle femmine. Nelle femmine, i geni che supportano la crescita delle uova enfatizzano la produzione e l’imballaggio delle proteine, mentre nei maschi si concentra maggiormente su strutture come ciglia e microtubuli che aiutano il movimento degli spermatozoi. Lo studio ha anche mappato come si sviluppa il massiccio organo di supporto delle uova nelle femmine, il vitellario, attraverso stadi intermedi, e ha identificato nuovi marker genetici che rivelano il grado di maturazione di ciascun tessuto riproduttivo.
Un circuito nervoso presente solo nei maschi, in un canale di abbraccio
Una delle scoperte più sorprendenti è emersa dal sistema nervoso. L’atlante ha rivelato non una raccolta disordinata di neuroni, ma cinque linee neuronali chiaramente distinte, incluse diverse differenze tra maschi e femmine. Tre tipi neuronali — denominati N2.2, N3.2 e N4.3 — erano fortemente arricchiti nei maschi e raggruppati all’interno del canale ginecoforico, una scanalatura specializzata che il maschio usa per accogliere la femmina. Tra questi, i neuroni N4.3 hanno spiccato perché esprimevano un gene chiamato nrps, che codifica l’enzima che produce BATT, un piccolo peptide feromone precedentemente dimostrato stimolare lo sviluppo sessuale femminile. In altre parole, queste cellule N4.3 sono le “stazioni di segnalazione” del maschio per l’attivazione della fertilità femminile.
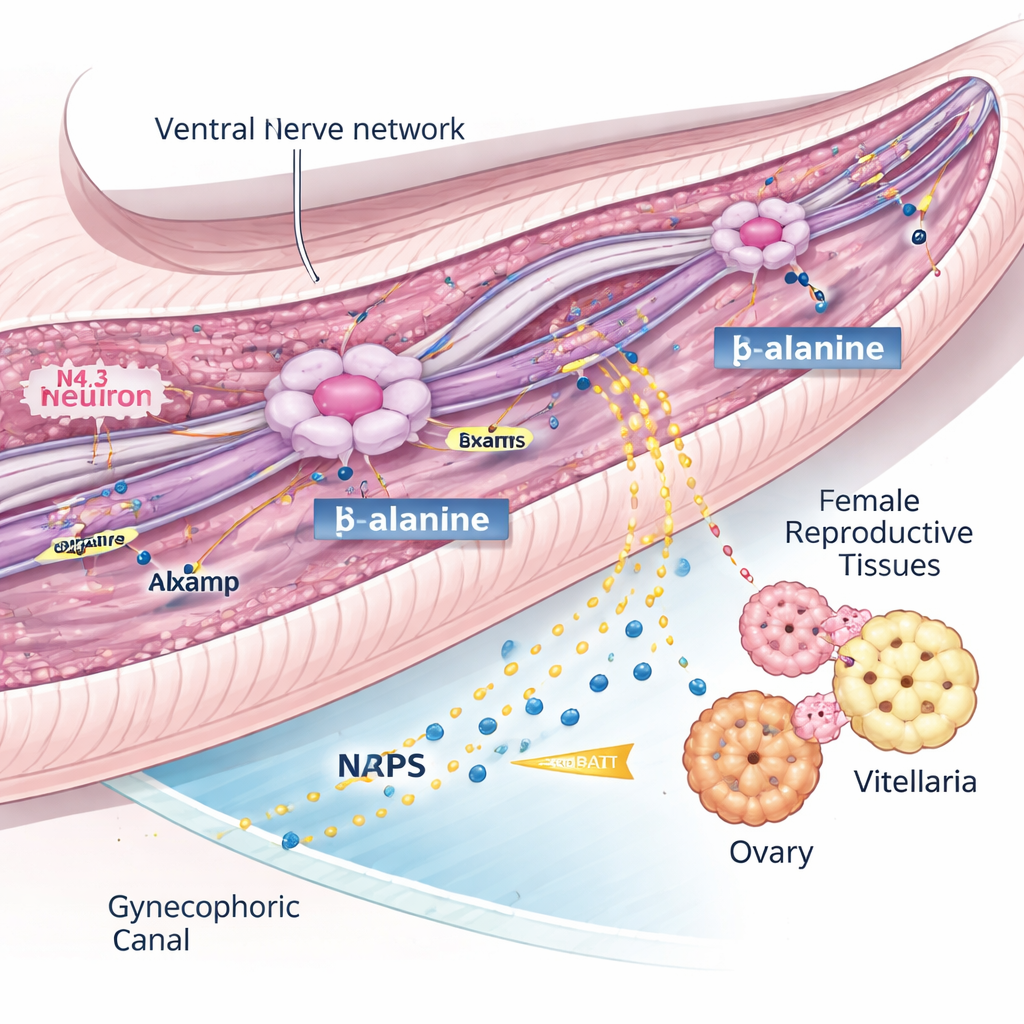
Una molecola guida che mantiene il segnale
Per comprendere come funzionano questi neuroni N4.3, i ricercatori hanno cercato geni che sembrassero dirigere il loro sviluppo e la loro funzione. Si sono concentrati su lsamp, un gene noto in altri animali per aiutare i neuroni a connettersi e a mantenere gli assoni. Nei trematodi maschi, lsamp era attivato negli stessi neuroni N4.3 che producono l’enzima BATT, e la sua attività aumentava rapidamente con la maturazione dei vermi. Riducendo lsamp nei maschi tramite interferenza a RNA, il team ha osservato che le femmine accoppiate non sono riuscite a sviluppare completamente ovaie e vitellari e hanno deposto quasi nessuna uova. Tuttavia i neuroni N4.3 erano ancora presenti, il gene nrps rimaneva attivo e i precursori chimici grezzi per BATT non risultavano alterati. I maschi carenti di lsamp mostravano invece fibre nervose danneggiate e un trasporto vescicolare compromesso lungo microtubuli stabilizzati, e producevano molto meno BATT all’interno del corpo e nell’ambiente circostante. Questo suggerisce che lsamp è fondamentale per mantenere una rete nervosa ventrale che consegna un precursore chiave, probabilmente la β-alanina, ai neuroni N4.3 in modo che possano sintetizzare abbastanza feromone da attivare la femmina.
Ridurre l’interruttore riproduttivo
Per i non specialisti, il messaggio principale è che la capacità di questo parassita di causare malattia dipende da una conversazione intima tra maschio e femmina, condotta attraverso una rete nervosa specializzata e un minuscolo feromone. Lo studio dimostra che una singola molecola guida, lsamp, contribuisce a costruire e mantenere il cablaggio nervoso ventrale del maschio; quando questo cablaggio fallisce, il maschio non riesce più a inviare un segnale chimico sufficientemente forte per far maturare completamente gli organi riproduttivi della femmina, e la produzione di uova cala drasticamente. Mappando le cellule del parassita ad alta risoluzione e scoprendo questo circuito neurale presente solo nei maschi, il lavoro indica nuove strade per bloccare la produzione di uova — offrendo una potenziale strategia per contenere la schistosomiasi dove il trattamento attuale si affida a un unico farmaco datato.
Citazione: You, Y., Cheng, S., Chen, X. et al. Dynamic single-cell transcriptomics reveals lsamp-guided neural network formation in male S. japonicum driving female reproduction. Nat Commun 17, 1602 (2026). https://doi.org/10.1038/s41467-026-68305-7
Parole chiave: schistosomiasi, trascrittomica single-cell, riproduzione del parassita, circuiti neurali, segnalazione da feromoni