Clear Sky Science · it
Meccanismo di resistenza di SARS-CoV-2 agli antivirali a base di analoghi nucleotidici
Come il virus inganna farmaci antivirali chiave
Il virus della COVID-19 appartiene a un gruppo raro di virus a RNA in grado di correggere gli errori nel proprio materiale genetico, il che lo rende insolitamente abile nel resistere ad alcuni dei nostri migliori antivirali. Questo studio esplora i dettagli a livello atomico di come SARS-CoV-2 rileva ed elimina una classe di farmaci molto usata, gli analoghi nucleotidici, spiegando perché farmaci efficaci contro altri virus spesso hanno prestazioni inferiori nelle infezioni da coronavirus.
Una lotta per l'RNA virale
SARS-CoV-2 copia il suo genoma di circa 30.000 lettere usando una grande macchina molecolare chiamata complesso di replicazione–trascrizione. Al suo centro c’è la RNA‑dipendente RNA polimerasi (RdRp), che sintetizza i nuovi filamenti di RNA, e un’unità separata, l’esonucleasi (ExoN), che controlla e rimuove gli errori. Molte pillole antivirali, compresi farmaci sviluppati per l’epatite C, imitano i normali mattoncini dell’RNA in modo sufficientemente fedele da essere incorporati dalla RdRp, ma con piccole modifiche che bloccano la copiatura o introducono errori. Purtroppo, i coronavirus posseggono ExoN, che può riconoscere questi impostori una volta inseriti nella catena di RNA e rimuoverli, permettendo così al virus di riprendere la replicazione.
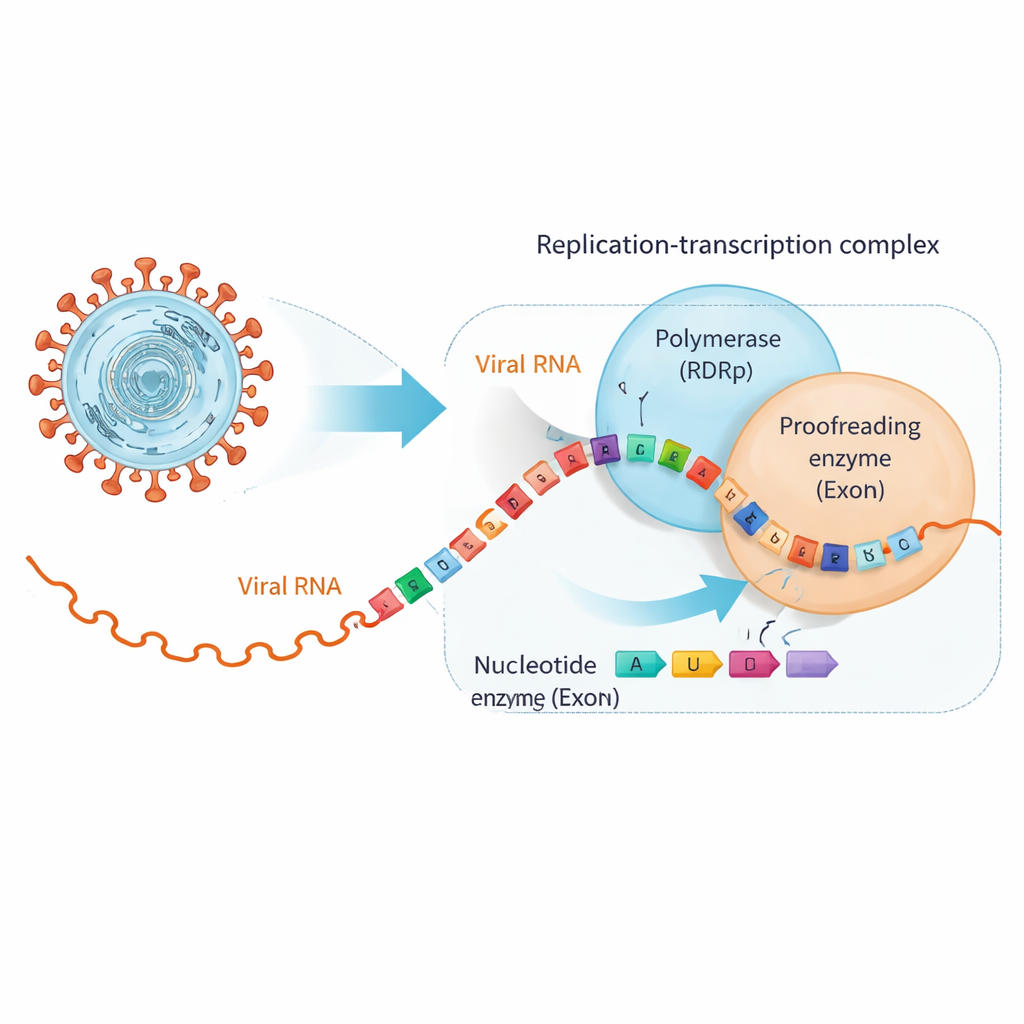
Quando i farmaci utili fanno cambiare partner all'RNA
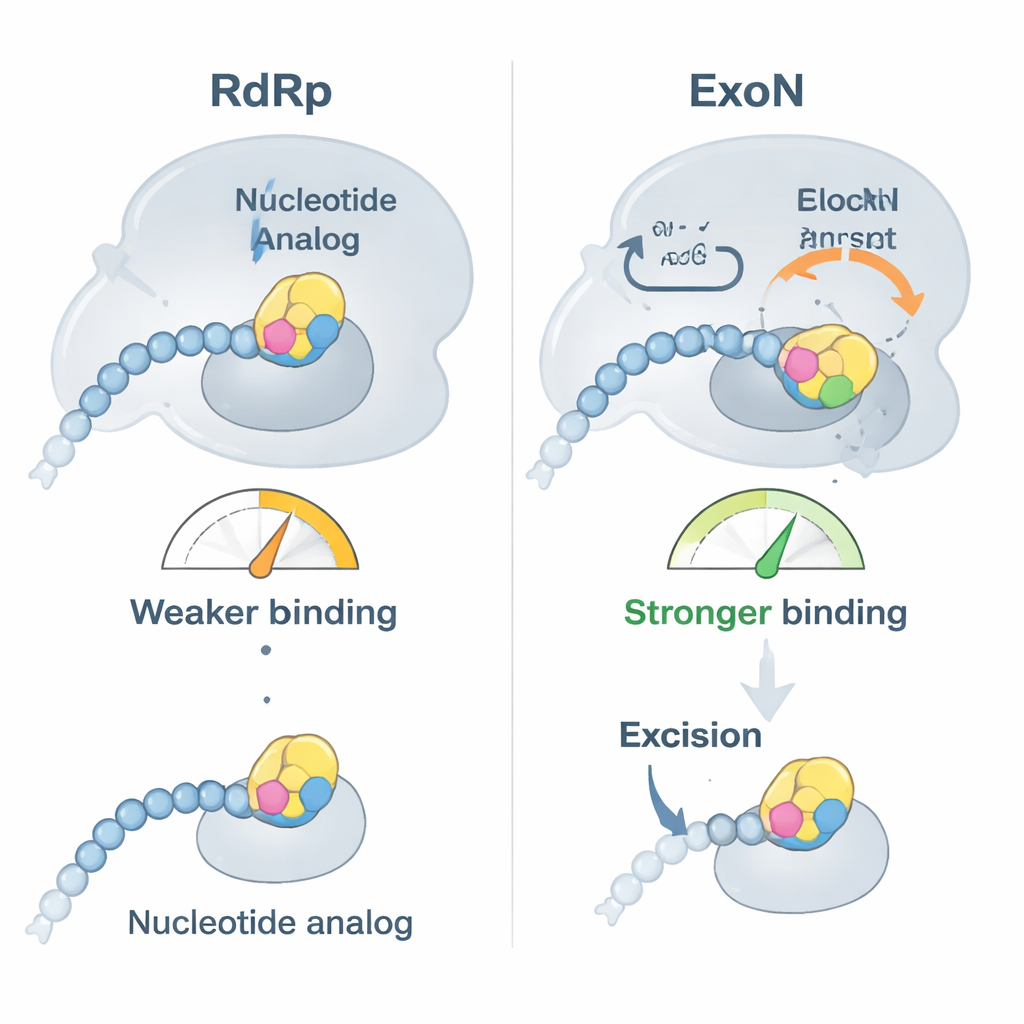
I ricercatori si sono concentrati su due antivirali clinicamente importanti, bemnifosbuvir e sofosbuvir, entrambi pensati per comportarsi come mattoni difettosi dell’RNA. Hanno prima dimostrato che la polimerasi di SARS-CoV-2 inserisce facilmente questi analoghi all'estremità di un filamento di RNA e poi per lo più smette di allungare la catena, come previsto. Tuttavia, test di legame hanno rivelato una svolta: una volta che un analogo si trova alla punta dell’RNA, il legame dell’RNA alla polimerasi si indebolisce mentre aumenta l’affinità per ExoN. Di fatto, l’RNA modificato dal farmaco viene spinto fuori dalla macchina di copia e consegnato al correttore, che ha così l’opportunità di tagliare via il nucleotide problematico e permettere alla replicazione di continuare.
Una correzione che rallenta ma non si arresta
Esperimenti biochimici nel tempo hanno mostrato che ExoN rimuove bemnifosbuvir e sofosbuvir dall’RNA, ma più lentamente rispetto ai nucleotidi normali. In reazioni in vitro prive di cellule, entrambi gli analoghi bloccavano fortemente la sintesi successiva dell’RNA—eppure quando veniva aggiunta una ExoN attiva, una frazione significativa dei filamenti RNA arrestati veniva recuperata e allungata. Una mutante inattiva di ExoN non era in grado di farlo, confermando che l’attività di proofreading è responsabile dell’annullamento di gran parte dell’effetto dei farmaci. La presenza della polimerasi insieme a ExoN accelerava in realtà la rimozione degli analoghi, suggerendo che i due enzimi virali agiscono in concerto per eliminare gli ostacoli e mantenere la replicazione in funzione.
Osservare il correttore a risoluzione atomica
Per capire come ExoN riconosce e risponde a questi farmaci, il team ha usato la crio‑microscopia elettronica ad alta risoluzione per determinare le strutture del complesso ExoN legato a filamenti di RNA terminanti con bemnifosbuvir o sofosbuvir. Queste strutture, abbastanza nitide da mostrare gruppi chimici individuali, hanno rivelato che l’anello zuccherino modificato di ciascun farmaco si inserisce in una tasca idrofobica formata da un breve loop della proteina ExoN. Questa maggiore aderenza spiega il più forte legame dell’RNA contenente il farmaco con ExoN. Ma ha anche un effetto collaterale inaspettato: tirando quel loop, i farmaci disturbano l’assetto preciso di un vicino loop catalitico che mantiene in posizione un residuo di istidina chiave. Quando questa istidina si allontana dal sito di taglio, il centro attivo di ExoN diventa parzialmente inattivato, rallentando ma non impedendo del tutto l’escissione dell’analogo.
Un interruttore integrato che calibra il proofreading virale
La mutazione di singoli amminoacidi all’interno del loop sensibile ne ha confermato l’importanza. Alterazioni di quattro residui conservati hanno notevolmente ridotto la capacità di ExoN di tagliare sia estremità di RNA standard sia estremità terminate da farmaci, e hanno anche modificato quale nucleotido finale ExoN preferisce rimuovere. Questo identifica il loop come un regolatore allosterico—un interruttore meccanico integrato che percepisce che tipo di nucleotide si trova alla punta dell’RNA e regola l’attività dell’enzima. Le strutture mostrano inoltre che ExoN riconosce basi diverse (A, U, C o G) tramite legami a idrogeno flessibili, ma ha maggiori difficoltà ad accomodare basi simili alla guanina, cosa rilevante poiché bemnifosbuvir imita la guanosina.
Cosa significa questo per le future pillole contro COVID-19
Per i non specialisti, il messaggio chiave è che SARS-CoV-2 possiede un sofisticato “correttore ortografico” capace di estrarre alcuni farmaci dal proprio genoma dopo che hanno svolto il loro compito di bloccare la replicazione. Bemnifosbuvir e sofosbuvir indeboliscono la macchina di copia del virus, ma al tempo stesso indirizzano l’RNA verso il correttore che può in parte annullarne gli effetti. Rivelando esattamente come il correttore virale afferra questi farmaci e come un piccolo loop regolatore commuta l’enzima tra stati più o meno attivi, questo lavoro offre una mappa per progettare nuovi nucleotidi antivirali che o si legano poco a ExoN, o lo bloccano in una conformazione inattiva, o sfruttano la sua difficoltà a gestire strutture simili alla guanina. Molecole di nuova generazione di questo tipo potrebbero essere molto più difficili da “cancellare” per il virus, migliorando la nostra capacità di curare COVID-19 e future epidemie da coronavirus.
Citazione: Liu, C., Li, Y., Cao, X. et al. Mechanism of SARS-CoV-2 resistance to nucleotide analog-based antivirals. Nat Commun 17, 1601 (2026). https://doi.org/10.1038/s41467-026-68304-8
Parole chiave: SARS-CoV-2, resistenza antivirale, analoghi nucleotidici, correzione dell'RNA, replicazione dei coronavirus