Clear Sky Science · it
L’attivazione di spillover degli idrossili da parte di acidi di Lewis consente l’elettroossidazione selettiva dell’urea a nitrito con produzione simultanea di idrogeno a minor consumo energetico
Trasformare i rifiuti in prodotti utili e carburante pulito
L’urea è più nota come componente delle urine e dei concimi, ma nelle acque reflue rappresenta un inquinante ostinato. Questo studio mostra come l’urea possa diventare una risorsa anziché un problema: usando un catalizzatore progettato con cura, gli autori convertono l’urea in nitrito, un composto prezioso per fertilizzanti e farmaci, producendo contemporaneamente idrogeno con un consumo elettrico inferiore rispetto alla scissione dell’acqua convenzionale. Il lavoro offre uno sguardo su impianti di trattamento futuri che depurano l’acqua, producono beni utili e generano energia pulita in un unico processo.
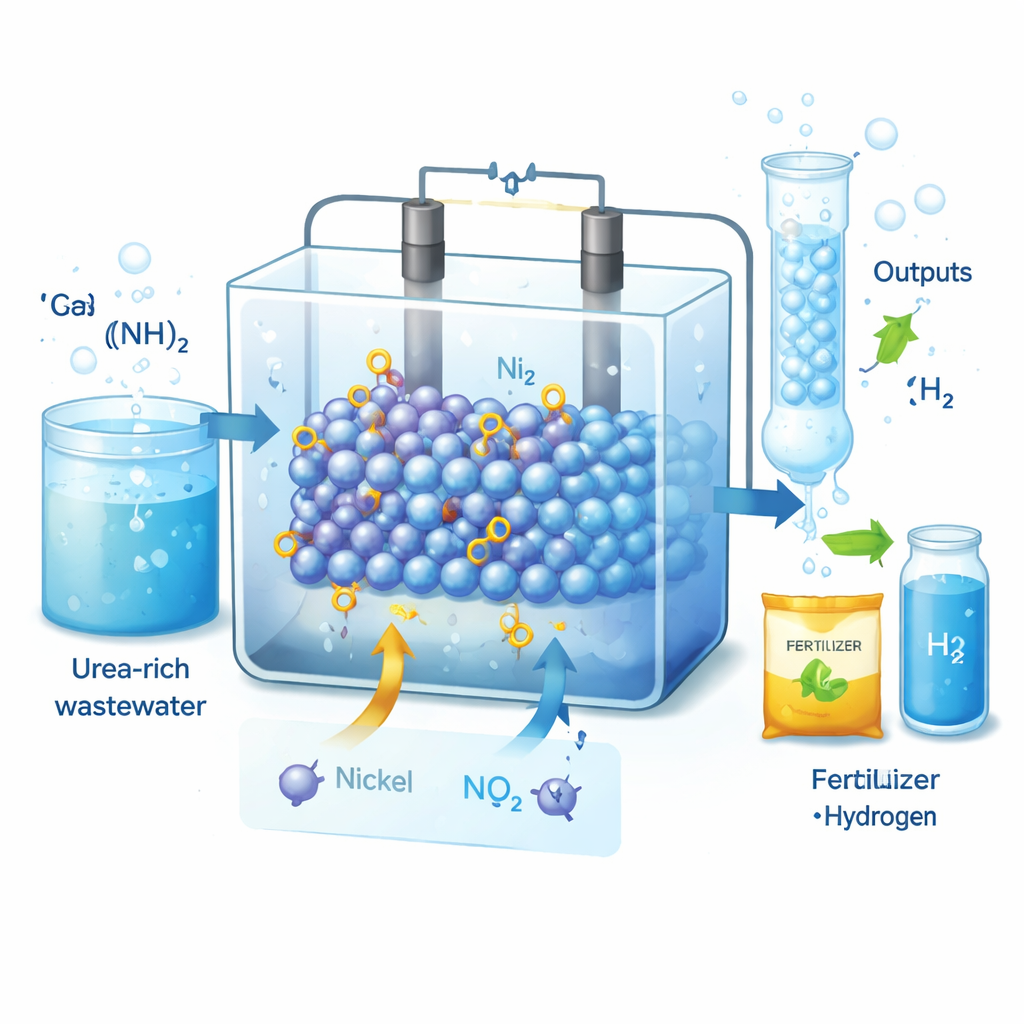
Perché nitrito e idrogeno sono importanti
Il nitrito è un ingrediente chiave in agricoltura, nella conservazione degli alimenti e nella farmaceutica, e la domanda globale si misura in milioni di tonnellate all’anno. Oggi la maggior parte del nitrito è prodotta tramite il processo Ostwald, che funziona ad alte temperature, richiede grandi quantità di energia e rilascia ossidi di azoto inquinanti. Allo stesso tempo, le acque reflue domestiche e industriali contengono elevate concentrazioni di urea, che rappresentano il 70–80% dell’azoto inquinante. Se quell’urea potesse essere elevata elettrochimicamente a nitrito producendo anche gas idrogeno, potremmo contemporaneamente depurare l’acqua e ottenere due prodotti ad alto valore—purché il processo sia sufficientemente efficiente e selettivo.
Guidare le reazioni lungo il percorso giusto
Quando l’urea viene ossidata in soluzione alcalina, può seguire due percorsi principali. Uno porta a gas inerti come l’azoto e anidride carbonica; l’altro, più desiderabile, porta a nitrito e nitrato, sostanze commerciabili. Il problema è che la maggior parte dei catalizzatori a base di nichel, i cavalli di battaglia di questa reazione, non è molto selettiva—tendono a produrre una miscela di prodotti e sprecano energia guidando la reazione di evoluzione dell’ossigeno (OER), che produce ossigeno senza valore commerciale. Gli autori hanno quindi riprogettato la superficie del catalizzatore in modo che gli ioni idrossido, la specie reattiva OH⁻ in mezzi alcalini, siano concentrati e direzionati per favorire la rottura dei legami carbonio–azoto e la formazione di nitrito piuttosto che il legame degli atomi di azoto in N₂.
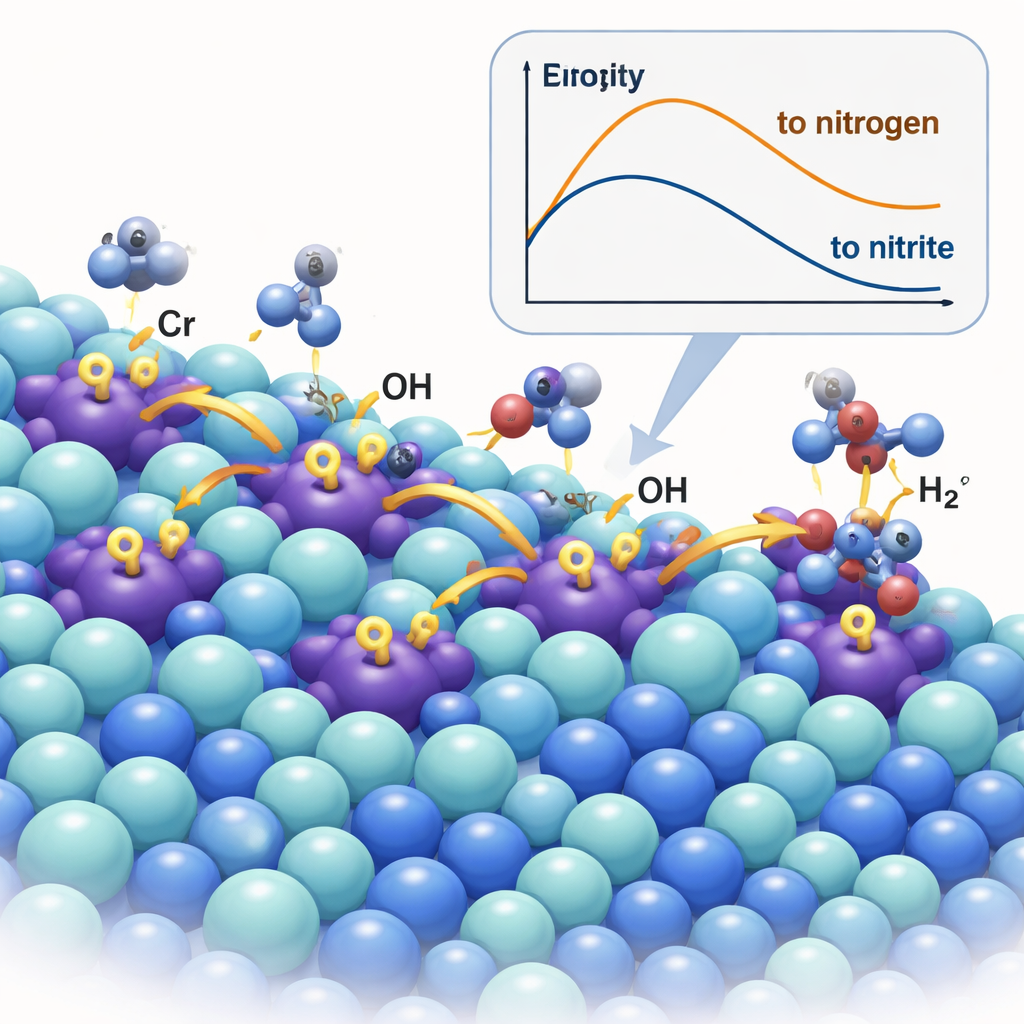
Un catalizzatore che pompa le specie reattive
Il gruppo ha creato un nuovo materiale drogando il solfuro di nichel (Ni₃S₂) con una piccola quantità di cromo, ottenendo Cr–Ni₃S₂. Gli ioni di cromo fungono da siti acidi di Lewis—centri poveri di elettroni che attirano fortemente gli ioni idrossido. Con microscopia avanzata, tecniche a raggi X e spettroscopia, i ricercatori hanno confermato che gli atomi di Cr si inseriscono nella rete del solfuro di nichel e ne contraggono e distorcono leggermente la struttura, modificando la distribuzione elettronica. In condizioni di reazione, i siti al cromo agiscono come piccole pompe: catturano OH⁻ e poi lo “spillano” verso i siti di nichel vicini, dove avviene l’effettiva ossidazione dell’urea. Misure in situ di Raman e infrarosso, insieme a esperimenti con marcatura isotopica, hanno tracciato direttamente questo spillover di idrossile da Cr a Ni e hanno mostrato che accelera la formazione dei siti attivi di ossido/idrossido di nichel (NiOOH) responsabili della chimica desiderata.
Alte rese, minore energia e solida stabilità
Poiché OH⁻ è consegnato in modo efficiente ai punti giusti, il catalizzatore Cr–Ni₃S₂ converte l’urea in nitrito con una selettività impressionante. A densità di corrente rilevanti per l’industria, raggiunge una produzione di nitrito di circa 121 milligrammi all’ora per centimetro quadrato con efficienze faradiche per il nitrito superiori all’80%, mantenendo l’evoluzione dell’ossigeno concorrente al di sotto dell’1,5%. Il catalizzatore rimane stabile per centinaia di ore di funzionamento continuo con perdite di cromo trascurabili. Lo stesso materiale riduce drasticamente anche la tensione richiesta quando è abbinato a un catodo per evoluzione di idrogeno in un dispositivo per la scissione assistita dall’urea, abbassando il costo elettrico della produzione di idrogeno a circa 3,7 kilowattora per metro cubo di H₂—meno dell’elettrolisi alcalina convenzionale. Un’analisi tecnico-economica suggerisce che, a 400 milliampere per centimetro quadrato, processare una tonnellata di urea in questo sistema potrebbe generare dell’ordine di 1.200 dollari di valore netto considerando sia il nitrito sia l’idrogeno.
Dalla cella di laboratorio ai dispositivi energetici pratici
Per dimostrare il potenziale applicativo, gli autori hanno costruito una cella a flusso per la scissione continua dell’acqua assistita da urea e una batteria Zn–urea–aria. Nella batteria, sostituire la consueta reazione di evoluzione dell’ossigeno durante la carica con l’ossidazione dell’urea ha ridotto la tensione di carica di quasi 0,3 volt mantenendo prestazioni stabili per più di 100 ore. Ciò significa che il dispositivo può sia depurare flussi contenenti urea sia fornire accumulo di energia con efficienza superiore. La stessa strategia basata sugli acidi di Lewis ha funzionato anche con altri metalli come stagno e titanio, o con un diverso ospite come il solfuro di rame, suggerendo che l’approccio è ampiamente applicabile.
Un’idea semplice dietro una reazione complessa
Per i non specialisti, l’idea chiave è che i ricercatori hanno imparato a controllare dove e come un ingrediente reattivo comune—l’idrossido—si deposita e si muove sulla superficie di un catalizzatore. Aggiungendo siti di cromo che agiscono come forti attrattori e relè per OH⁻, rendono più probabile che le molecole di urea vengano scisse in nitrito anziché ossidate completamente ad azoto molecolare. Allo stesso tempo, questa via richiede meno energia elettrica e produce naturalmente idrogeno come combustibile. In sostanza, il lavoro dimostra che un progetto attento a scala atomica dei “percorsi” sul catalizzatore può trasformare le acque reflue in fonte sia di prodotti chimici sia di energia pulita.
Citazione: Fan, C., Zhang, M., Li, Y. et al. Lewis acid-triggered hydroxyl spillover enables selective urea electrooxidation to nitrite with concurrent energy-saving hydrogen production. Nat Commun 17, 1585 (2026). https://doi.org/10.1038/s41467-026-68302-w
Parole chiave: ossidazione dell’urea, produzione di nitrito, generazione di idrogeno, elettrocatalisi, valorizzazione delle acque reflue