Clear Sky Science · it
Varianti de novo nel gene del fattore di splicing SF3B1 sono associate a disturbi del neurosviluppo
Quando un solo gene altera il progetto iniziale del cervello
Perché alcuni bambini sviluppano difficoltà di apprendimento, crisi epilettiche o problemi di alimentazione anche quando gravidanza e parto sembrano normali? Questo studio esamina un singolo gene, chiamato SF3B1, che aiuta le cellule a elaborare i messaggi genetici. I ricercatori mostrano che cambiamenti nuovi e spontanei in questo gene possono alterare sottilmente il modo in cui le cellule cerebrali leggono le istruzioni del DNA, portando a una sindrome del neurosviluppo finora non riconosciuta.
Un editore principale dei messaggi genetici
Ogni cellula del nostro corpo deve convertire il testo genetico grezzo in istruzioni chiare prima di poter produrre proteine. Questa fase di editing, nota come splicing dell'RNA, rimuove segmenti non codificanti e salda insieme le parti utili. SF3B1 è un componente centrale della «macchina» cellulare dello splicing. Finora, le alterazioni di SF3B1 erano principalmente conosciute per il loro ruolo nei tumori, in cui le cellule neoplastiche acquisiscono mutazioni in questo gene nel corso della vita. Il nuovo lavoro pone una domanda diversa: cosa succede quando una variante dannosa di SF3B1 è presente dalla concezione in ogni cellula del corpo?
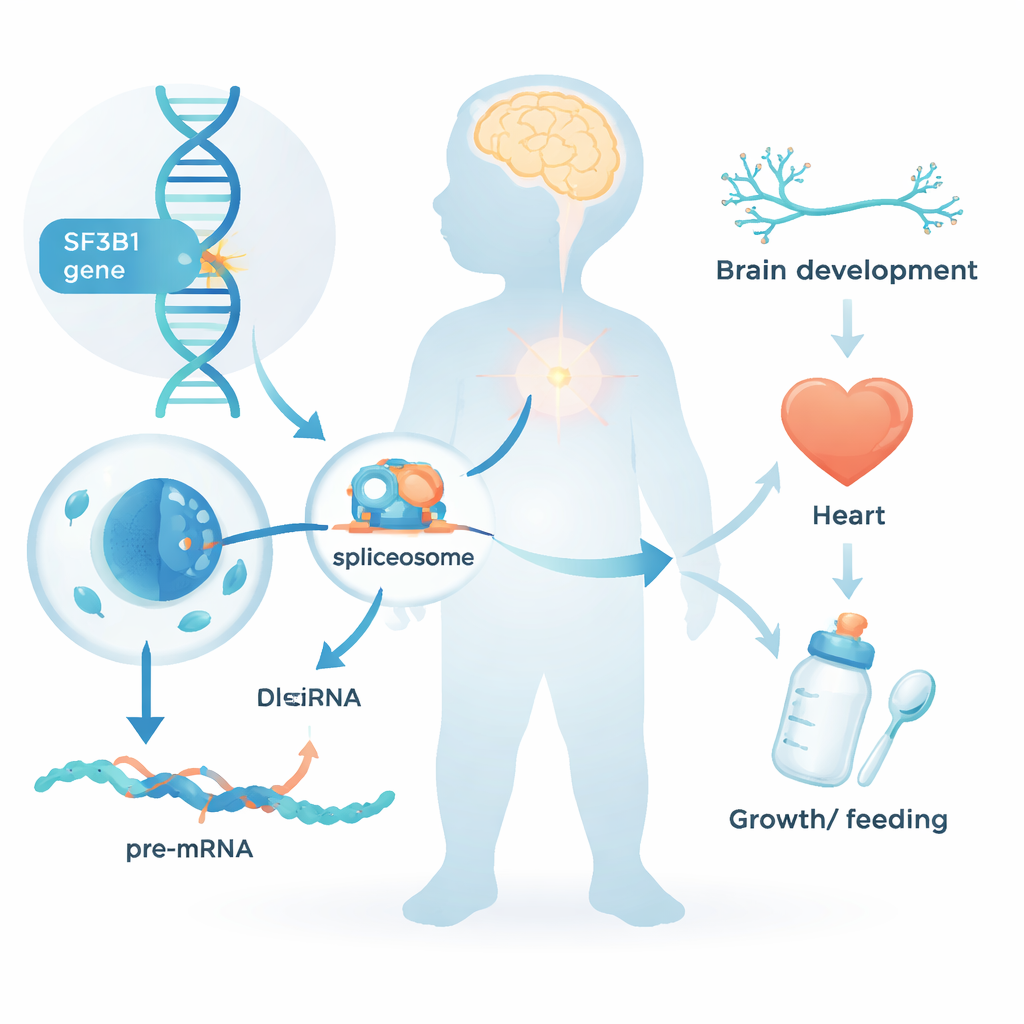
Una sindrome infantile riconosciuta di recente
Il gruppo ha raccolto dati da 26 bambini e giovani adulti che portavano varianti rare di SF3B1, per lo più emerse de novo — cioè non ereditate da nessuno dei genitori. Quasi tutti avevano problemi del neurosviluppo: ritardi nel raggiungere tappe motorie e del linguaggio come sedersi, camminare o parlare; disabilità intellettiva per lo più di grado lieve o moderato; e, in circa la metà dei casi, crisi epilettiche. Molti presentavano ipotonia e necessitavano di supporto aggiuntivo per l'alimentazione, talvolta tramite sondino gastrico. I tratti facciali erano lievemente atipici ma non identici da un bambino all'altro; una caratteristica sorprendentemente comune era il palato alto o fessurato. Diversi partecipanti avevano anche difetti cardiaci, restrizione della crescita o microcefalia, mostrando che l'impatto delle variazioni di SF3B1 si estende oltre il cervello.
Due classi di cambiamenti genetici, due quadri clinici
I ricercatori hanno distinto due tipi principali di varianti di SF3B1. Un gruppo includeva cambiamenti «loss‑of‑function», come segnali di stop prematuri, che dovrebbero ridurre la quantità di proteina SF3B1 funzionante. Il secondo gruppo conteneva varianti missenso, in cui un singolo amminoacido nella proteina è alterato. Clusterizzando i fenotipi medici dei bambini, il team ha osservato che coloro con varianti missenso tendevano ad avere problemi più gravi e complessi, inclusa una maggiore frequenza di anomalie cardiache e gastrointestinali, statura bassa e microcefalia. Le varianti loss‑of‑function, al contrario, a volte erano ereditate da un genitore lievemente affetto o addirittura apparentemente sano, suggerendo che una semplice riduzione di SF3B1 può essere compatibile con sintomi relativamente lievi in alcuni individui.
Errori di messa a punto più che un collasso completo
Per capire cosa facciano le varianti missenso nelle cellule, gli scienziati le hanno ricreate in linee cellulari di laboratorio. Sorprendentemente, queste proteine SF3B1 alterate potevano ancora svolgere il compito base dello splicing sufficientemente da ripristinare le cellule in cui l'SF3B1 normale era stato silenziato. Questo ha escluso una semplice spiegazione loss‑of‑function. Utilizzando un sequenziamento profondo dell'RNA, il team ha poi analizzato l'intero insieme di messaggi cellulari. Hanno riscontrato che le varianti missenso spostavano sottilmente lo splicing di centinaia di geni, soprattutto modificando quali siti di splicing venissero scelti ai bordi degli esoni e causando occasionali saltazioni di esoni. La scala della perturbazione era minore rispetto a quella osservata con la classica mutazione cancerogena SF3B1 K700E, ma comunque significativa: molti dei geni interessati sono coinvolti nello sviluppo cerebrale, nell'assetto dei circuiti nervosi e in processi fondamentali come la gestione dell'RNA e la sintesi proteica.
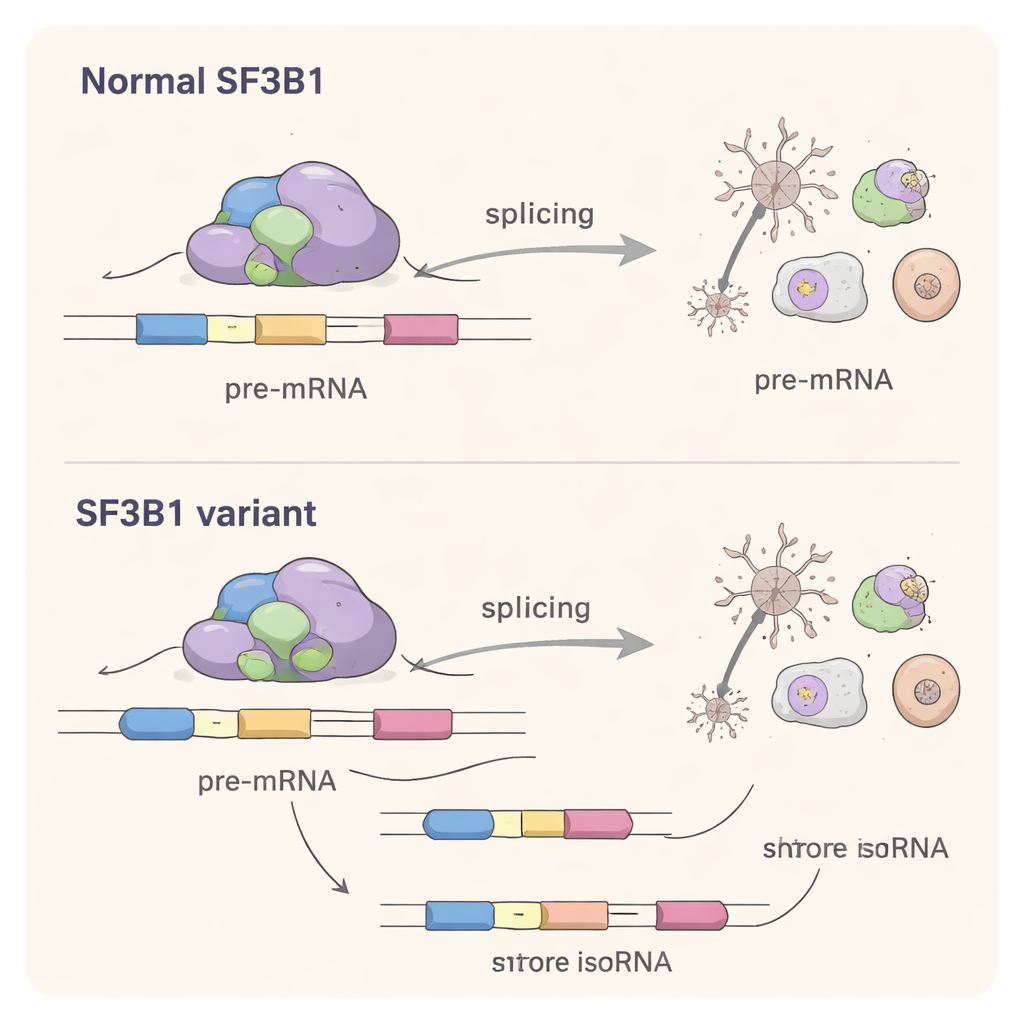
Un meccanismo condiviso tra cancro e disturbi cerebrali
Sebbene la maggior parte delle varianti di SF3B1 associate al neurosviluppo si trovi in posizioni diverse rispetto alle note mutazioni legate al cancro, esse disturbano lo stesso processo chiave: il riconoscimento preciso dei siti di splicing nell'RNA. Lo studio mostra che queste varianti dello sviluppo possiedono una loro «firma di splicing», scegliendo siti alternativi che spesso sono più vicini a quelli normali rispetto a quelli favoriti nel cancro. Ciò suggerisce un meccanismo di change‑of‑function, in cui la proteina mutata compete con la copia normale e spinge la macchina dello splicing verso scelte leggermente errate in molti geni contemporaneamente.
Cosa significa per le famiglie e per la ricerca futura
Per le famiglie coinvolte, il lavoro identifica SF3B1 come una nuova causa di disturbi del neurosviluppo che può ora essere testata nelle cliniche genetiche, ponendo potenzialmente fine a lunghe ricerche diagnostiche. Più in generale, aggiunge SF3B1 a una lista ristretta ma crescente di geni dello splicing le cui alterazioni possono guidare sia il cancro sia i disturbi cerebrali infantili, a seconda di quando e come il gene viene modificato. Mappando come varianti specifiche di SF3B1 rimodellano lo splicing dell'RNA, lo studio pone le basi per future terapie mirate a correggere il mis‑splicing in modo specifico.
Citazione: Uguen, K., Bergot, T., Scott-Boyer, MP. et al. De novo variants in the splicing factor gene SF3B1 are associated with neurodevelopmental disorders. Nat Commun 17, 1569 (2026). https://doi.org/10.1038/s41467-026-68284-9
Parole chiave: Splicing dell'RNA, SF3B1, disturbi del neurosviluppo, varianti de novo, spliceosomopatie