Clear Sky Science · it
Idrogel viscoelastico che priming dei macrofagi CAR per il trattamento della fibrosi polmonare
Trasformare gli "spazzini" del corpo in squadre di riparazione di precisione
La fibrosi polmonare è una malattia polmonare devastante in cui il normale tessuto elastico del polmone viene lentamente sostituito da una cicatrice rigida. Le persone faticano a respirare e, oggi, i farmaci disponibili per lo più rallentano solo il peggioramento. Questo studio esplora un’idea nuova: convertire le cellule addette alla pulizia del corpo, i macrofagi, in “spazzini intelligenti” ingegnerizzati e potenziarne l’attività con un gel morbido progettato appositamente. Insieme, queste strategie aiutano le cellule a rintracciare i responsabili della formazione di cicatrici e persino ad ammorbidire il tessuto rigido nei polmoni danneggiati.
Quando la guarigione diventa dannosa
Nei polmoni sani, i fibroblasti aiutano a mantenere la delicata rete di collagene che sostiene gli alveoli. Nella fibrosi polmonare, queste cellule diventano iperattive, depositando spessi filamenti di collagene che soffocano gli spazi aerei. I farmaci esistenti possono attenuare questi processi ma raramente li invertano. Gli autori si concentrano su un marcatore di superficie cellulare chiamato proteina di attivazione dei fibroblasti (FAP), abbondante nei fibroblasti iperattivi ma scarsa nei tessuti normali. Se le cellule immunitarie potessero essere addestrate a riconoscere FAP, potrebbero rimuovere selettivamente i fibroblasti “sfuggenti” che guidano la formazione di cicatrici, risparmiando le cellule sane vicine.
Riprogammare i macrofagi per colpire i costruttori di cicatrici
I macrofagi sono cellule immunitarie di pattuglia che normalmente inglobano cellule morte, microrganismi e detriti cellulari. Il gruppo le ha dotate di un recettore antigene chimerico (CAR) che riconosce FAP, creando macrofagi CAR (CAR‑M). In colture cellulari, questi CAR‑M hanno inglobato ed eliminato in modo efficiente fibroblasti ricchi di FAP, ignorando in gran parte le cellule con FAP ridotto. Hanno inoltre degradato con maggiore vigore gel ricchi di collagene rispetto ai macrofagi non modificati, suggerendo un duplice vantaggio: eliminare le cellule che creano la cicatrice e disgregare direttamente la matrice cicatriziale stessa. Questi effetti sono stati osservati sia in linee cellulari standard sia in macrofagi primari murini, più vicini alla situazione reale nei tessuti. 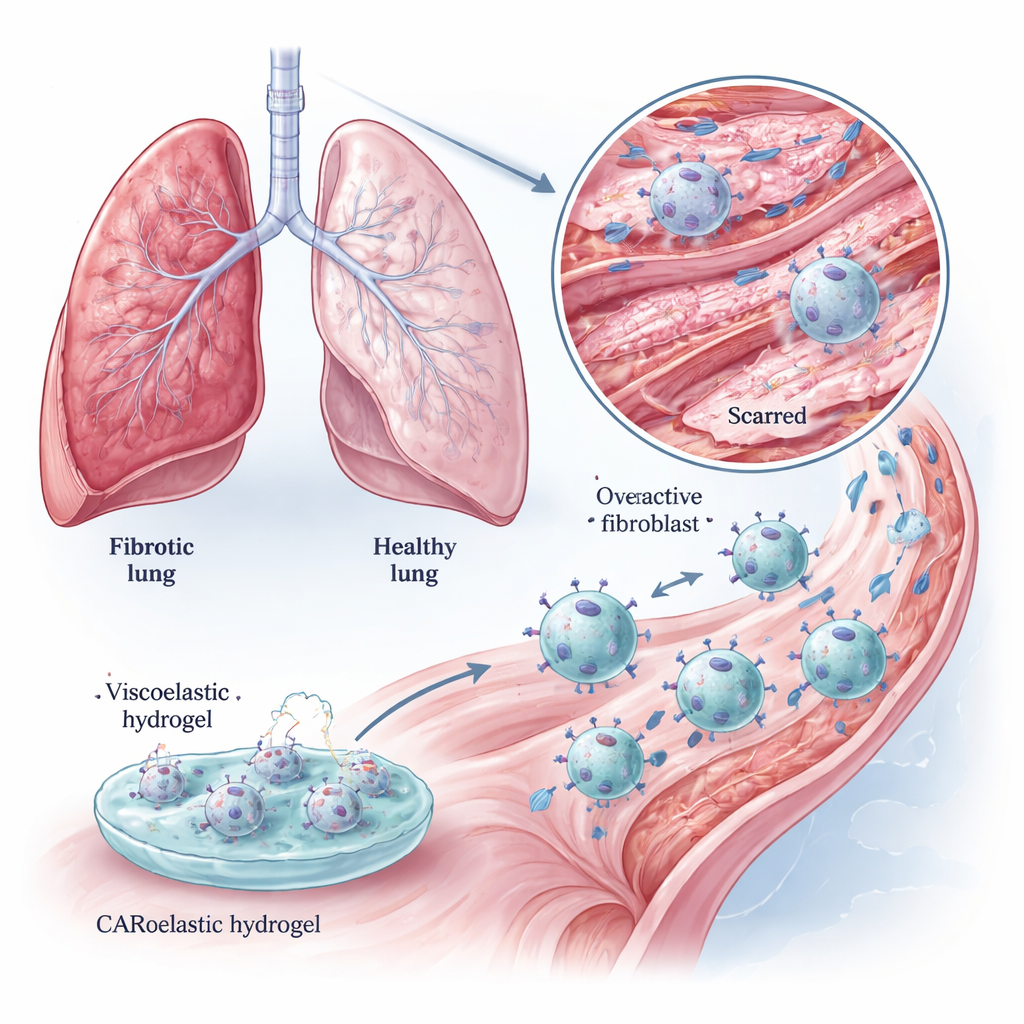
Priming delle cellule immunitarie con un gel morbido e viscoelastico
L’ingegneria genetica delle cellule è potente ma complessa. I ricercatori si sono quindi chiesti se un segnale puramente fisico — un idrogel morbido e viscoelastico — potesse ulteriormente modulare il comportamento dei CAR‑M. Hanno realizzato un idrogel a base di gelatina‑alginato il cui “modulo di perdita”, una misura di quanto si rilassa lentamente sotto sforzo, poteva essere regolato finemente senza cambiare la rigidità complessiva. Quando i CAR‑M sono stati brevemente coltivati su gel con la viscoelasticità adeguata, la loro capacità di uccidere i fibroblasti bersaglio è aumentata più che con i comuni stimolanti chimici, e l’aumento è durato per almeno due giorni. Questi “Gel‑CAR‑M” hanno anche attivato geni legati all’attivazione immunitaria e al rimodellamento tissutale, mentre hanno ridotto l’espressione di geni associati alla fibrosi, suggerendo che l’esperienza sul gel ha impresso alle cellule un’identità più anti‑cicatriziale.
Come una superficie più morbida riorganizza il comportamento cellulare
Per capire perché il gel avesse effetto, il gruppo ha esaminato lo stato fisico dei recettori CAR sulla superficie cellulare. Una sonda fluorescente ha rivelato che i CAR‑M primati con l’idrogel avevano una tensione di membrana inferiore — la “pelle” esterna della cellula era più rilassata. In queste condizioni, le molecole CAR si sono disperse da ammassi stretti in unità più isolate, singole o in coppia. Test biochimici hanno mostrato che questi recettori dispersi favorivano forme che innescano più facilmente la segnalazione interna, specialmente lungo vie come ERK che controllano l’attivazione e la capacità citotossica. Riprodurre la riduzione di tensione con una piccola molecola ha prodotto lo stesso allargamento dei recettori e un miglioramento nell’uccisione delle cellule bersaglio, sostenendo l’idea che il rilassamento meccanico della membrana sia sufficiente a “pre‑armare” le cellule prima ancora che incontrino i loro bersagli. 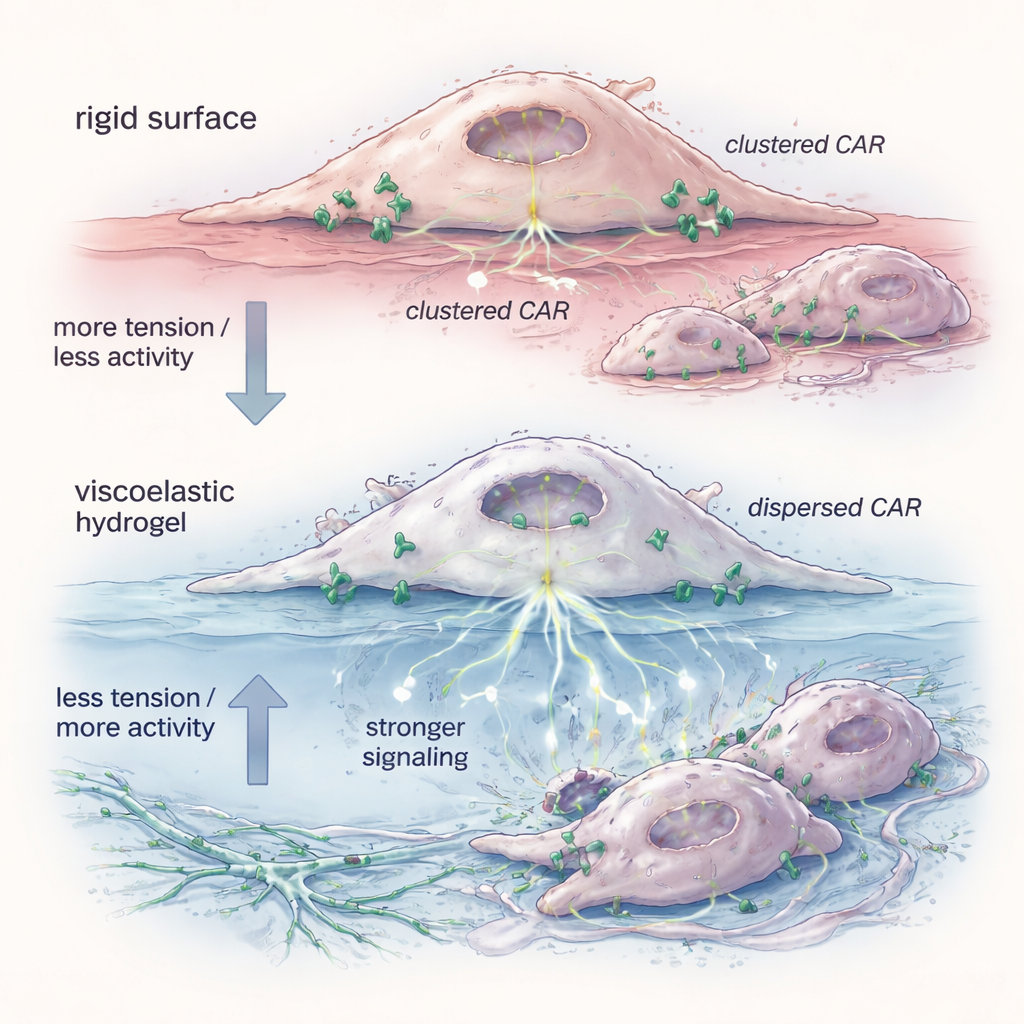
Riparare i polmoni cicatrizzati nei topi
La prova definitiva è stata in un modello murino di fibrosi polmonare indotta da farmaci. Gli animali hanno ricevuto macrofagi semplici, CAR‑M standard o Gel‑CAR‑M primati con l’idrogel. Tutti i topi trattati sono migliorati rispetto ai controlli non trattati, ma i Gel‑CAR‑M hanno ottenuto i risultati migliori: i loro polmoni contenevano meno collagene, spazi aerei più normali e meno fibroblasti positivi per FAP. Le analisi geniche del tessuto polmonare hanno mostrato che i Gel‑CAR‑M hanno attenuato i segnali infiammatori e ridotto l’espressione di geni correlati alla cicatrice in modo più efficace rispetto ai CAR‑M standard. Le cellule tracciate sono persistite nel polmone per almeno una settimana e controlli di sicurezza estesi fino a 12 settimane non hanno rilevato danni agli organi, anomalie del sangue o segni di autoimmunità.
Una nuova direzione per le terapie cellulari anti‑fibrosi
Per i non specialisti, il messaggio chiave è che la combinazione di ingegneria cellulare mirata e materiali intelligenti può trasformare cellule immunitarie innate in strumenti anticitine altamente efficaci, senza eccessive complicazioni genetiche. Riposando brevemente i macrofagi ingegnerizzati su un gel morbido e accuratamente tarato, i ricercatori hanno “pre‑impostato” meccanicamente i loro recettori di superficie in una modalità più reattiva. Nei topi con fibrosi polmonare, questo si è tradotto in una migliore rimozione dei fibroblasti dannosi, nella degradazione dell’eccesso di collagene e in una parziale restaurazione della struttura polmonare normale — senza problemi di sicurezza evidenti. Pur rimanendo molto lavoro prima di studi clinici sull’uomo, questa strategia suggerisce che ottimizzare l’ambiente fisico delle cellule terapeutiche potrebbe un giorno rendere i trattamenti per le malattie polmonari fibrotiche più potenti e più precisi.
Citazione: Zhang, Y., Liu, Z., Kong, W. et al. Viscoelastic hydrogel primed CAR-macrophage for pulmonary fibrosis treatment. Nat Commun 17, 1663 (2026). https://doi.org/10.1038/s41467-025-68033-4
Parole chiave: fibrosi polmonare, terapia con macrofagi CAR, idrogel viscoelastico, proteina di attivazione dei fibroblasti, meccanobiologia cellulare