Clear Sky Science · it
Base molecolare dell'inibizione della metilazione del DNA de novo da parte di TCL1A
Come le cellule decidono cosa ricordare
Ogni cellula del corpo contiene sostanzialmente lo stesso DNA, eppure neuroni, cellule del sangue e cellule della pelle si comportano in modo molto diverso. Un modo in cui le cellule «ricordano» la propria identità è attraverso tag chimici aggiunti al DNA, un processo chiamato metilazione del DNA. Questo studio svela, a livello atomico, come una piccola proteina chiamata TCL1A possa spegnere gli enzimi che scrivono questi segni metilici. Poiché sia la metilazione del DNA sia TCL1A sono collegati a cancro e disturbi riproduttivi, comprendere questa lotta molecolare potrebbe infine ispirare nuove terapie.
La macchina cellulare che marca il DNA
La metilazione del DNA funziona come un segno a matita nei margini del genoma, contribuendo a silenziare alcuni geni e a stabilizzare il genoma durante lo sviluppo cellulare. Due enzimi, DNMT3A e DNMT3B, sono i principali «scribi» che applicano nuovi marchi metilici durante lo sviluppo precoce e quando le cellule staminali si specializzano. Se questi enzimi sono mutati o regolati in modo anomalo, il pattern dei segni sul DNA può andare in confusione, contribuendo a sindromi dello sviluppo e a tumori del sangue. TCL1A è una proteina nota soprattutto per il suo ruolo nei tumori delle cellule immunitarie, dove è frequentemente sovraespressa. Lavori precedenti avevano suggerito che TCL1A possa legarsi a DNMT3A e DNMT3B e attenuarne l’attività, ma non si sapeva esattamente come realizzasse questo blocco.
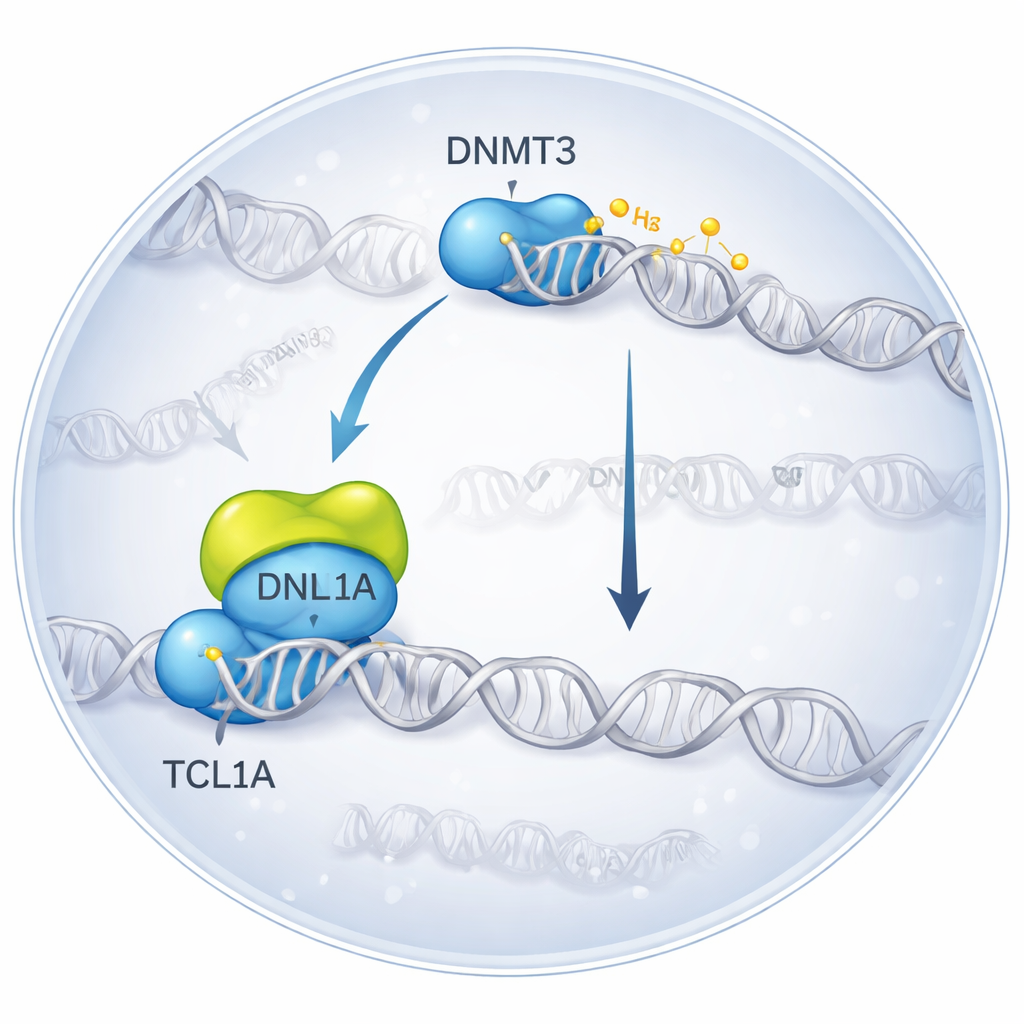
Congelare in 3D un incontro molecolare
I ricercatori hanno usato la crio‑microscopia elettronica, una tecnica che fotografa molecole rapidamente congelate, per visualizzare il complesso formato quando DNMT3A si lega a TCL1A. Hanno scoperto che due molecole di DNMT3A si affiancano e che su ciascun lato un dimero di TCL1A si ancora alla porzione catalitica di DNMT3A — proprio la regione che normalmente interagisce con proteine ausiliarie e con il DNA. Questa superficie di legame si sovrappone al punto in cui un altro partner, DNMT3L, si attacca solitamente per aumentare l’attività di DNMT3A. In test biochimici, l’aggiunta di TCL1A ha ridotto drasticamente la capacità di metilare il DNA sia di DNMT3A sia di DNMT3B, anche in presenza di DNMT3L, confermando che il complesso strutturale corrisponde a uno stato fortemente inibito.
Un cambiamento di forma che inceppa l’enzima
Osservando più in dettaglio, il gruppo ha visto che il legame di TCL1A non si limita a posarsi sul sito attivo come un coperchio. Invece, induce un cambiamento sottile ma esteso nella conformazione di DNMT3A. Due regioni flessibili dell’enzima, note come il loop di riconoscimento del bersaglio e il loop catalitico, si allontanano dalle posizioni che occupano quando DNMT3A è legato al DNA. Nella forma attiva, questi loop si appoggiano contro il DNA e formano una tasca per una piccola molecola carburante chiamata SAM, che dona il gruppo metile. Con TCL1A legato, il loop catalitico invece si ripiega nella tasca del SAM e la ostruisce, rendendo anche più difficile l’accesso del DNA all’enzima. Misure di legame hanno confermato che DNMT3A associato a TCL1A non riesce più a trattenere in modo rilevabile né il DNA né il SAM.
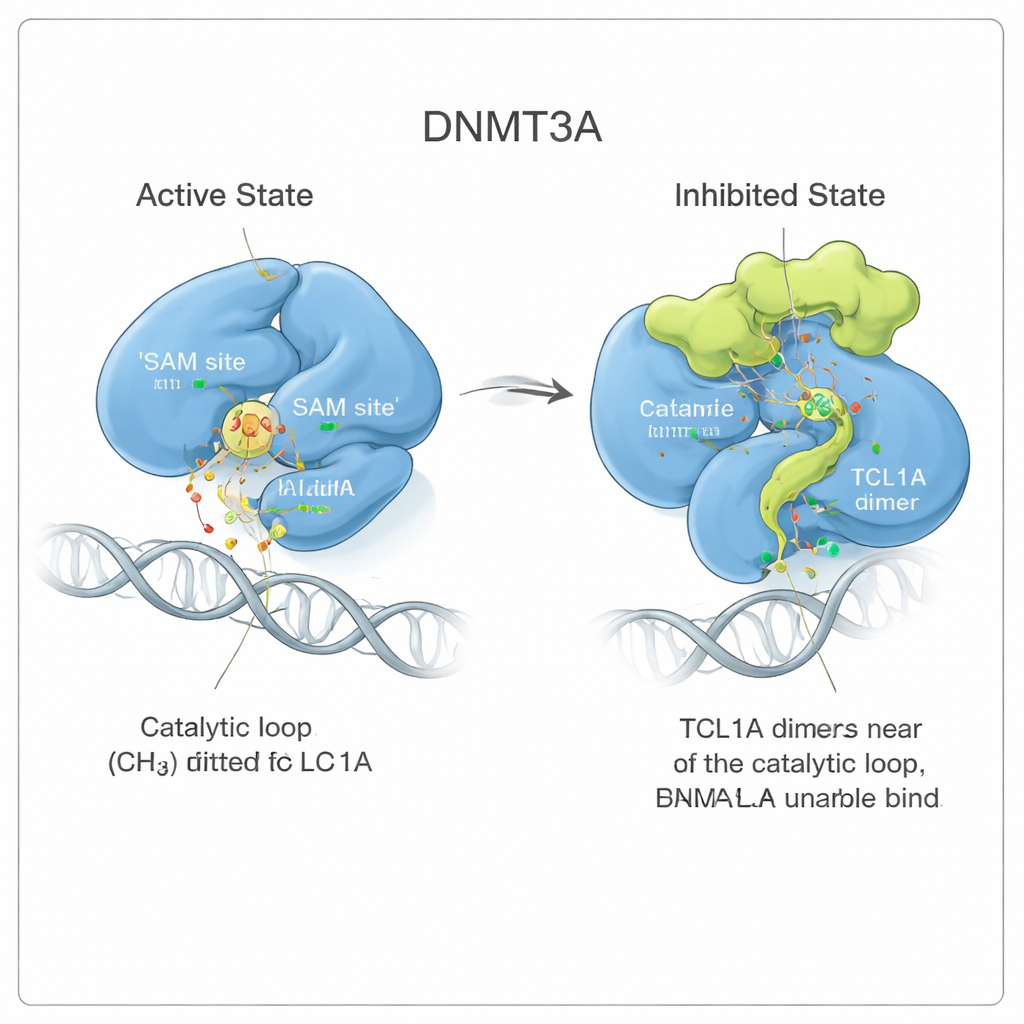
Osservare in movimento un blocco dinamico
Per capire quanto sia stabile questa conformazione inibita, gli autori hanno eseguito lunghe simulazioni di dinamica molecolare, cioè filmati basati sulla fisica delle molecole in soluzione. Quando DNMT3A era legato al suo attivatore DNMT3L, il loop catalitico rimaneva saldo nella posizione attiva. In presenza di TCL1A, quel loop diventava molto più mobile, sbattendo ma occupando ripetutamente la tasca del SAM come alghe che svolazzano e comunque intasano uno scarico. Questo movimento continuo ha ridotto lo spazio disponibile per il SAM di oltre dieci volte, supportando un modello in cui TCL1A sfrutta la naturale flessibilità di DNMT3A per imporre una modalità di inibizione dinamica, più che rigida.
Conseguenze per le cellule in sviluppo e per la malattia
Il team ha poi chiesto cosa significhi questo blocco molecolare per cellule reali. Hanno ingegnerizzato cellule staminali embrionali di topo per produrre TCL1A umano in una fase in cui le cellule normalmente aumentano la metilazione del DNA mentre iniziano a differenziarsi. Mappature genomiche della metilazione hanno mostrato che le cellule che sovraesprimevano TCL1A non hanno acquisito il normale alto livello di metilazione del DNA, assomigliando molto a cellule in cui i geni Dnmt3a e Dnmt3b erano entrambi eliminati. Una versione mutante di TCL1A che lega male gli enzimi DNMT3 ha avuto scarso effetto, sottolineando che l’interazione fisica è cruciale. Questi risultati collegano il meccanismo strutturale a cambiamenti epigenetici estesi attraverso il genoma.
Cosa significa per la salute
Nel complesso, il lavoro rivela come TCL1A possa agire come un forte freno sugli enzimi che instaurano nuove metilazioni del DNA. Ancorandosi a un’interfaccia critica, TCL1A riposiziona loop flessibili in DNMT3A e DNMT3B in modo che non possano più legare il filamento di DNA o il carburante chimico, portando a una perdita globale dei segni di metilazione nelle cellule. Nello sviluppo normale, questo tipo di controllo finemente regolato può aiutare a bilanciare quando e dove la metilazione viene aggiunta. Quando TCL1A è dislocato o sovraespresso, come in alcuni tumori del sangue e in rari disturbi riproduttivi, lo stesso meccanismo può mandare fuori strada il programma epigenetico della cellula. Comprendere questa interazione a risoluzione atomica apre la strada alla progettazione di molecole che imitino o contrastino gli effetti di TCL1A, con la possibilità di ripristinare pattern di metilazione del DNA sani.
Citazione: Liu, Q., Li, J., Wang, X. et al. Molecular basis for the inhibition of de novo DNA methylation by TCL1A. Nat Commun 17, 2159 (2026). https://doi.org/10.1038/s41467-025-67710-8
Parole chiave: metilazione del DNA, DNMT3A, TCL1A, epigenetica, cancro