Clear Sky Science · it
La riduzione di RAD23A prolunga la vita e attenua la patologia in un modello murino di proteinopatia da TDP-43
Perché questa ricerca è importante per famiglie e pazienti
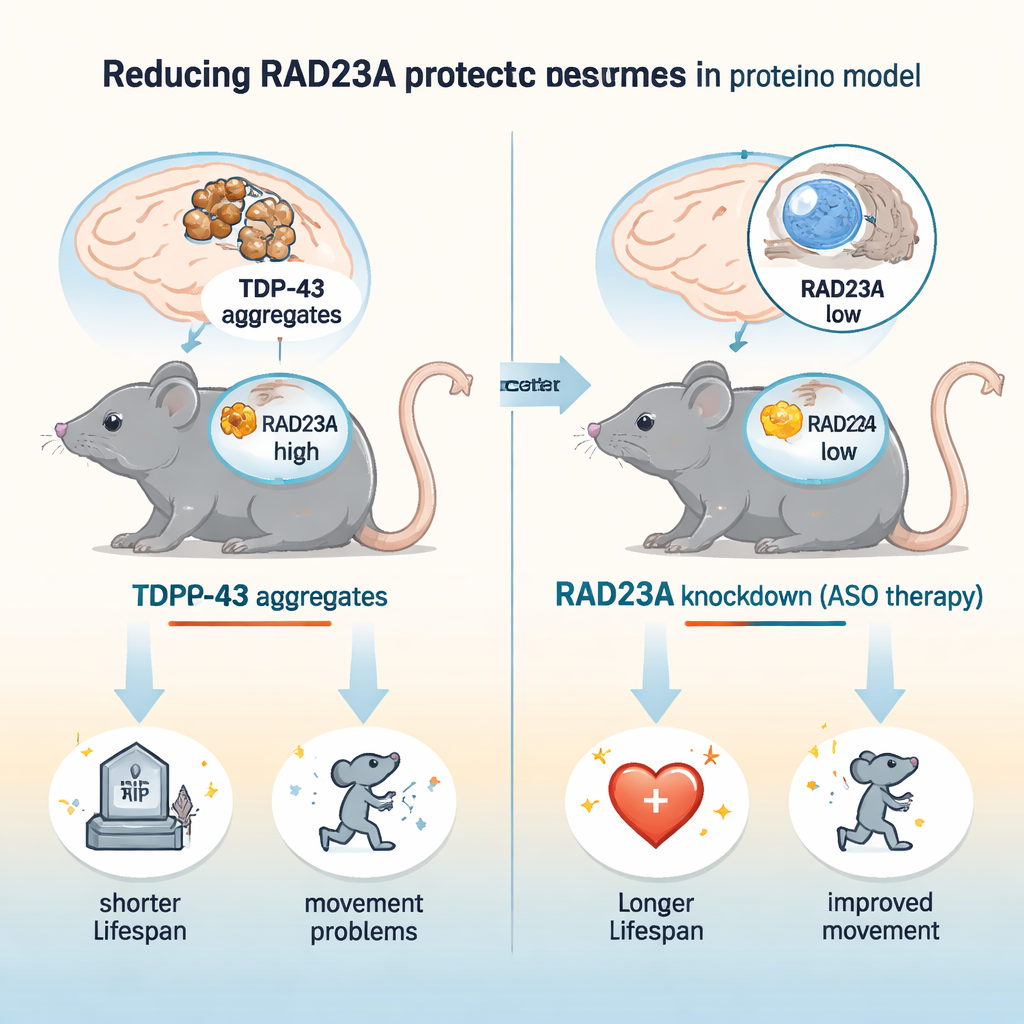
Molte forme di demenza e di malattia dei motoneuroni, inclusa la sclerosi laterale amiotrofica (SLA) e la demenza frontotemporale (FTD), coinvolgono proteine nelle cellule cerebrali che si ripiegano in modo errato, si aggregano e lentamente avvelenano i neuroni. Uno dei colpevoli chiave è una proteina chiamata TDP-43, che normalmente aiuta a gestire l’RNA ma diventa tossica quando si aggrega. Questo studio pone una domanda promettente: possiamo rendere le cellule cerebrali più resilienti riducendo un’altra proteina, RAD23A, che contribuisce a come vengono gestite le proteine danneggiate? Gli autori mostrano nei topi che abbassare RAD23A può prolungare la vita, migliorare il movimento e ridurre il danno cerebrale in un modello di malattia guidata da TDP-43, suggerendo una nuova strategia terapeutica.
Ingorgo del traffico proteico nei neuroni malati
Le malattie neurodegenerative sono spesso caratterizzate da cumuli di proteine mal ripiegate che la macchina di smaltimento cellulare non riesce a eliminare. Nella SLA e nella FTD, TDP-43 esce dal nucleo, forma ammassi appiccicosi e viene pesantemente marcata con ubiquitina, un segnale che normalmente indirizza le proteine al proteasoma, il principale trituratore cellulare. RAD23A è una delle diverse proteine “shuttle” che può trasportare i cargo marcati con ubiquitina al proteasoma. Tuttavia, lavori precedenti in vermi e neuroni coltivati suggerivano che la perdita di proteine simili a RAD23 potesse in realtà proteggere dal danno indotto da TDP-43, un paradosso che questo studio ha voluto esplorare nel cervello di un mammifero vivente.
Abbassare RAD23A in un modello murino di TDP-43
I ricercatori hanno usato un modello murino ben consolidato, chiamato TAR4/4, che sovraproduce TDP-43 umano nei neuroni e sviluppa problemi di movimento, curvatura spinale, tremore e morte precoce, rispecchiando caratteristiche chiave di SLA/FTD. Hanno ridotto RAD23A in due modi: iniettando topi neonati con oligonucleotidi antisenso (ASO) che riducono l’RNA di Rad23a, e incrociando topi portatori di un knockout genetico di Rad23a. Un singolo trattamento con ASO ha ridotto i livelli di RAD23A nel cervello e nel midollo spinale di circa tre quarti. In questi topi TDP-43, il knockdown di RAD23A ha esteso la durata della vita di circa il 50% e ha ritardato insorgenza e gravità dei problemi di andatura, del tremore, della curvatura spinale e del clasping degli arti posteriori. Interessante, una perdita genetica completa di RAD23A non ha apportato ulteriori benefici, suggerendo che una riduzione parziale è ottimale e che l’assenza totale a lungo termine potrebbe scatenare cambiamenti compensatori.
Meno infiammazione, migliore gestione delle proteine e un genoma più calmo
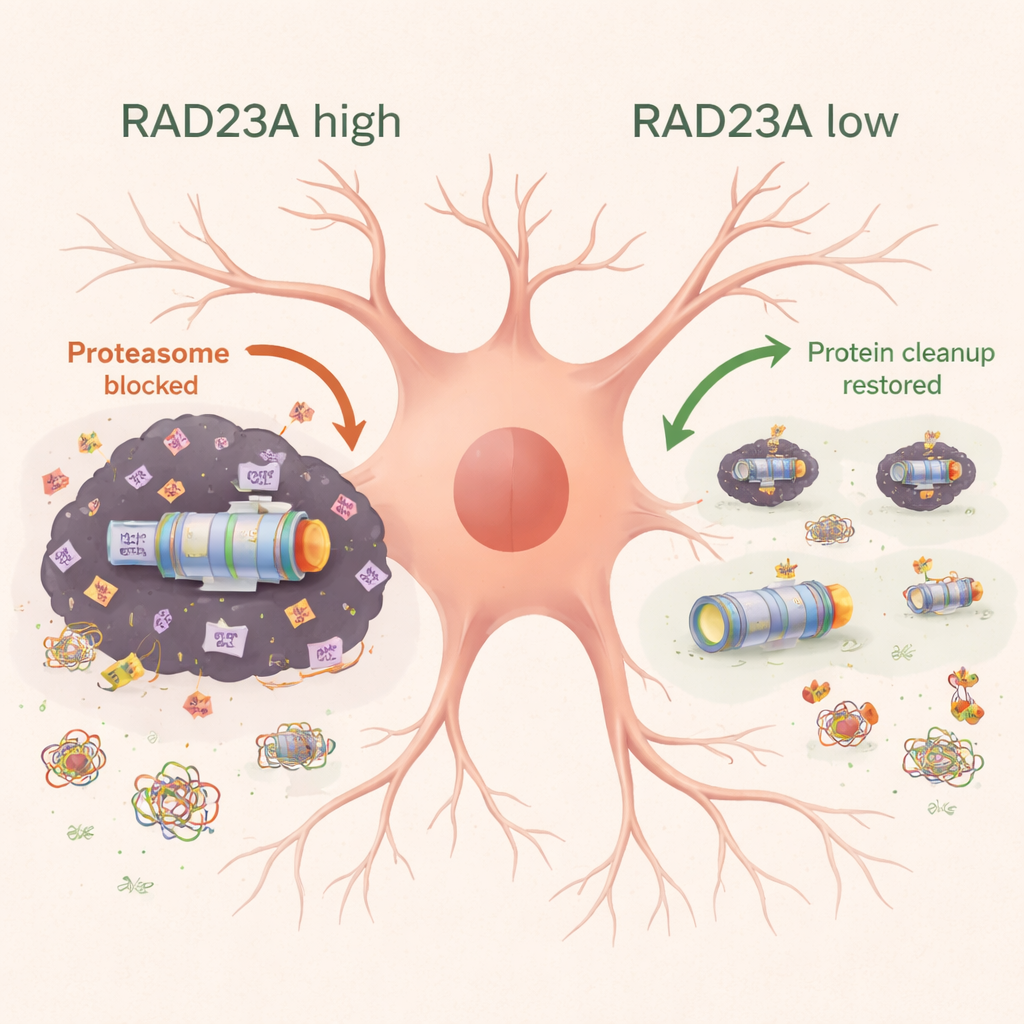
L’esame microscopico della corteccia motoria ha mostrato che i topi TDP-43 perdevano neuroni e sviluppavano una forte attivazione di astrociti e microglia, le cellule di supporto e immunitarie del cervello. Abbassare RAD23A ha preservato il numero di neuroni e ridotto i marcatori di infiammazione e morte cellulare. Analisi biochimiche hanno rivelato che la sovrapproduzione di TDP-43 saturava le cellule di proteine insolubili marcate con ubiquitina e trascinava sotto forma di aggregati sottounità del proteasoma, indebolendo la capacità cellulare di eliminare le proteine danneggiate. Riducendo RAD23A si è abbassato il carico totale di proteine ubiquitinate, si è mantenuto un maggior numero di proteasomi nella frazione solubile e funzionante e si è ripristinata verso la normalità diverse attività del proteasoma. Contemporaneamente, il knockdown di RAD23A ha ridotto sia le forme totali sia quelle aggregate di TDP-43, incluso un frammento particolarmente tossico di 25 kilodalton, e ha riportato TDP-43 dal citoplasma verso il nucleo. Il sequenziamento dell’RNA a livello di genoma ha mostrato che migliaia di cambiamenti nell’espressione genica indotti da TDP-43 sono stati parzialmente invertiti quando RAD23A è stato ridotto, in particolare geni coinvolti nella funzione neuronale, nella produzione di energia mitocondriale e nelle vie di smaltimento degli aggregati come l’aggrephagy.
Rimodellamento del proteoma “insolubile” nascosto
Per esaminare più da vicino gli aggregati ostinati che resistono ai detergenti normali, il gruppo ha utilizzato spettrometria di massa con isotopi pesanti per catalogare le proteine intrappolate nella frazione insolubile della corteccia murina. L’espressione di TDP-43 umano ha attirato componenti del proteasoma, proteine del citoscheletro e del trasporto, e altra macchina cellulare. Quando RAD23A è stato ridotto, la composizione complessiva di questo proteoma insolubile è cambiata: sono state sequestrate meno proteine legate al proteasoma e al trasporto, mentre alcune proteine ribosomiali e legate allo stress sono aumentate negli aggregati. Notevolmente, questo rimodellamento non rifletteva semplicemente cambiamenti nei livelli di RNA, suggerendo che RAD23A influenza soprattutto come le proteine esistenti sono ripartite tra stati solubili e aggregati, piuttosto che quanto di ciascuna proteina viene prodotto.
Cosa potrebbe significare per terapie future
Nel complesso, questi risultati dipingono RAD23A come un potente regolatore della qualità proteica nei neuroni sotto stress. Riducendo parzialmente RAD23A in un modello murino guidato da TDP-43, gli autori sono riusciti a ridurre gli aggregati proteici tossici, ripristinare l’attività della macchina di smaltimento delle proteine, attenuare cambiamenti dannosi nell’espressione genica, limitare l’infiammazione cerebrale e prolungare la vita e la funzione motoria. Poiché l’accumulo anomalo di TDP-43 è diffuso sia nelle forme ereditarie sia in quelle sporadiche di SLA, FTD e disordini correlati, mirare a RAD23A con farmaci antisenso compatibili con l’uomo potrebbe offrire un modo per proteggere i neuroni senza bloccare direttamente TDP-43, una proteina essenziale. Pur restando molto da testare in altri modelli e nell’uomo, questo lavoro identifica RAD23A come una nuova e promettente leva su una via comune della neurodegenerazione.
Citazione: Guo, X., Prajapati, R.S., Chun, J. et al. Reduction of RAD23A extends lifespan and mitigates pathology in a mouse model of TDP-43 proteinopathy. Nat Commun 17, 1820 (2026). https://doi.org/10.1038/s41467-025-65104-4
Parole chiave: TDP-43, SLA, aggregazione proteica, proteasoma, terapia antisenso