Clear Sky Science · it
Istologia a super-risoluzione ottica di campioni fissati in formalina e inclusi in paraffina: sfide e opportunità
Vedere di più nei campioni tissutali conservati
Ospedali di tutto il mondo conservano sottili fette di organi dei pazienti in blocchi di cera affinché malattie come il cancro o i danni renali possano essere studiate per anni. Questo articolo di revisione spiega come nuovi tipi di microscopi ottici stiano trasformando quei campioni di routine in potenti finestre sulla malattia, rivelando dettagli troppo piccoli per i microscopi ospedalieri standard. Questi progressi potrebbero aiutare i medici a individuare le malattie prima, comprendere come progrediscono e personalizzare i trattamenti con maggiore precisione.
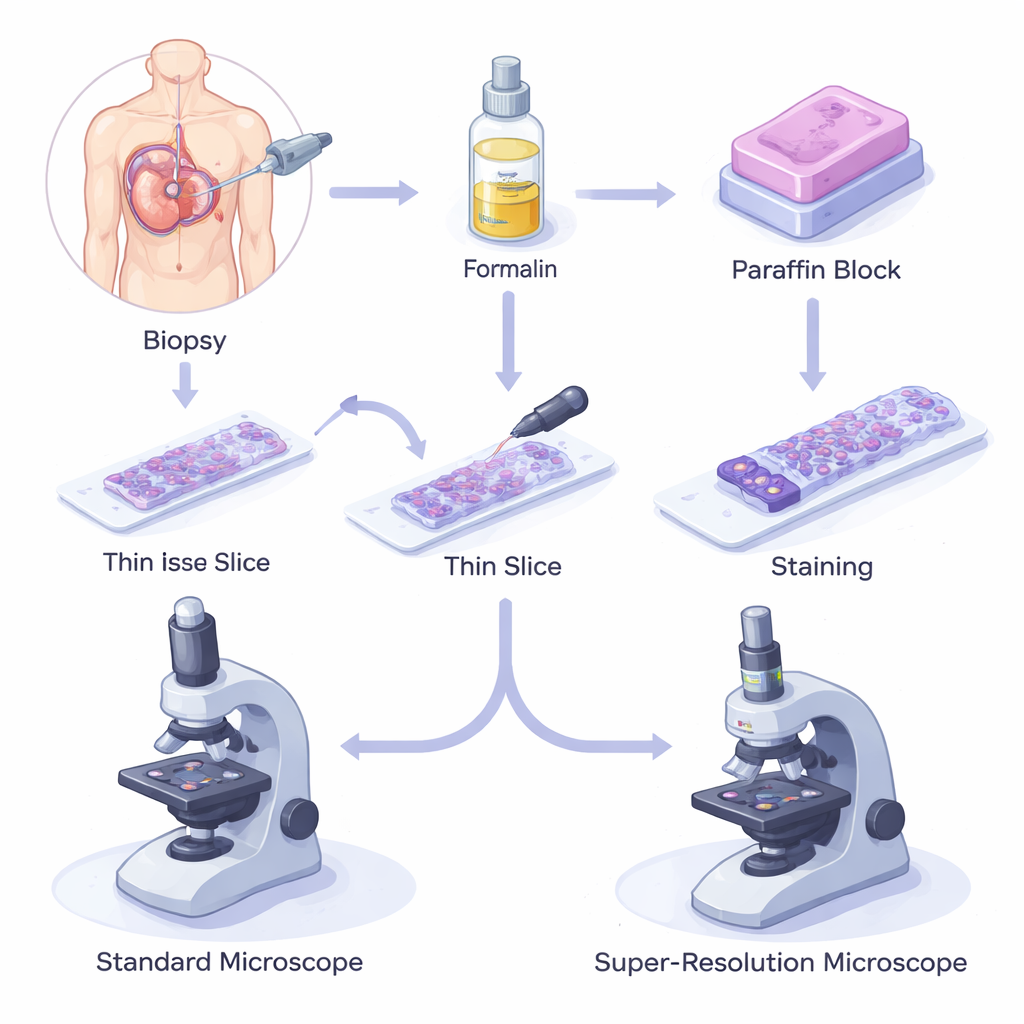
Come i tessuti conservati in cera sostengono la medicina moderna
Quando un paziente esegue una biopsia, un piccolo pezzo di tessuto viene rimosso, fissato in una soluzione chimica chiamata formalina per arrestare la degradazione e quindi incluso in paraffina. Il blocco viene tagliato in sezioni sottilissime come un capello, posate su vetrini, colorate e osservate al microscopio ottico. Il metodo formalin-fixed paraffin-embedded (FFPE) è economico, affidabile e può conservare i campioni per decenni a temperatura ambiente. Di conseguenza, milioni di campioni FFPE sono immagazzinati in biobanche in tutto il mondo, supportando tutto, dalla biologia di base agli studi avanzati su geni e proteine, e costituendo la spina dorsale della diagnosi e della prognosi moderne.
Perché i microscopi ordinari non bastano più
I microscopi ottici tradizionali sono limitati dalla fisica della luce: i dettagli inferiori a circa 250 nanometri si sfocano. Molte strutture rilevanti per le malattie — come i sottili filtri renali, le connessioni tra neuroni o piccole modificazioni nell’architettura del DNA nel nucleo — ricadono al di sotto di questo limite. Il flusso di lavoro attuale spesso combina la microscopia ottica standard per una panoramica con la microscopia elettronica per dettagli a livello nanometrico, ma questo approccio è lento, costoso e richiede una preparazione del campione completamente diversa. Clinici e ricercatori cercano quindi un unico sistema flessibile che possa scansionare ampie aree rapidamente e allo stesso tempo ingrandire per vedere caratteristiche su scala nanometrica nelle stesse sezioni FFPE già in uso.
Nuovi modi per affinare la visione
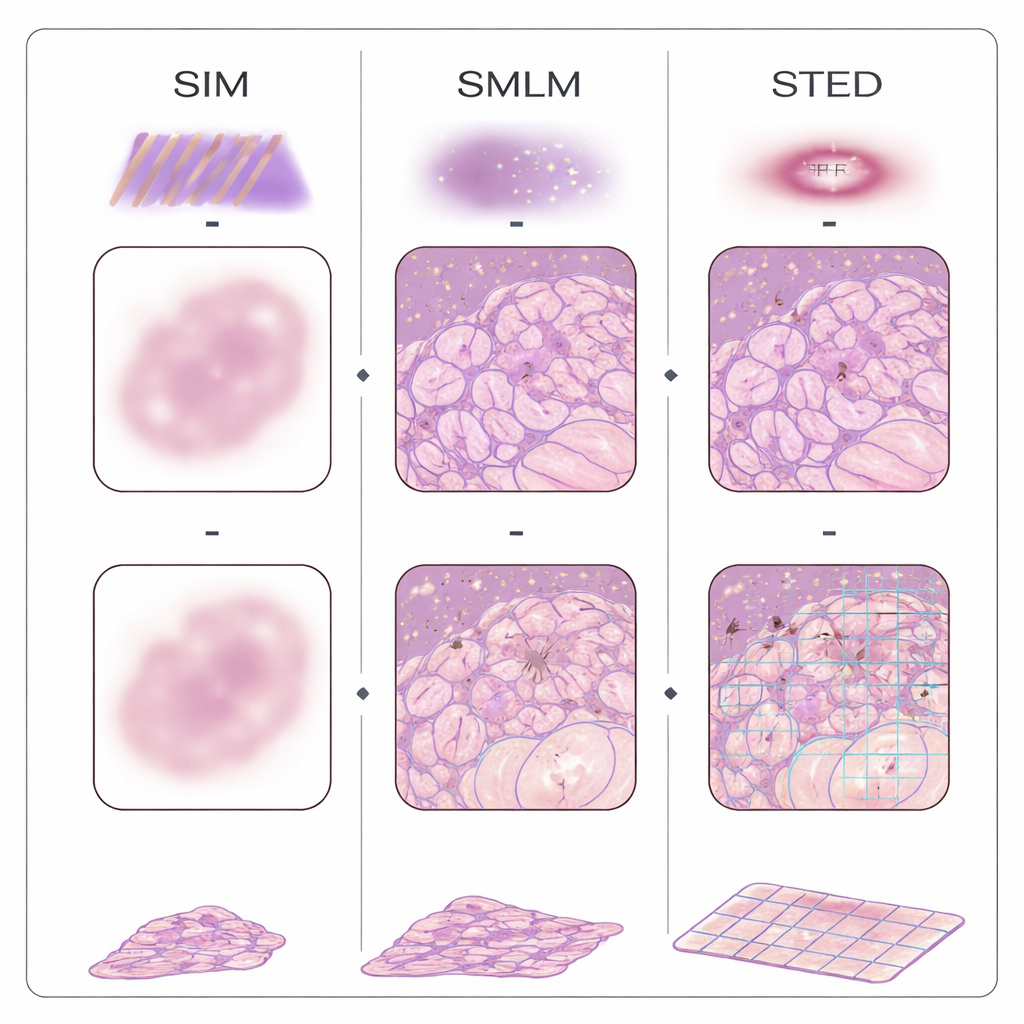
Negli ultimi due decenni diverse famiglie di microscopi “a super-risoluzione” hanno rotto la barriera di risoluzione tradizionale usando colorazioni fluorescenti e ottiche ingegnose. I metodi di localizzazione di molecole singole spengono e accendono le molecole e ne determinano la posizione una per una; l’illuminazione strutturata proietta motivi a strisce sul tessuto e usa il calcolo per recuperare dettagli più fini; lo stimulated emission depletion (STED) scolpisce un minuscolo spot luminoso con un fascio a forma di ciambella; e gli approcci basati sulle fluttuazioni analizzano sottili sfarfallii nell’immagine per inferire la struttura. Una strategia diversa, chiamata expansion microscopy, evita ottiche complesse facendo fisicamente gonfiare il tessuto in un gel, così che microscopi ordinari possano vedere dettagli precedentemente invisibili. Questi metodi sono già stati applicati a campioni FFPE di seno, colon, pancreas, rene, cervello, pelle, placenta e altri organi, rivelando come i mitocondri cambiano nei tumori, come i filtri renali falliscono e come si formano ammassi proteici nella malattia di Alzheimer.
Ostacoli sulla strada per l’uso quotidiano
Nonostante le promesse, queste tecniche non sono ancora pronte per diventare strumenti di routine nella maggior parte dei laboratori di patologia. Molti sistemi a super-risoluzione sono lenti, coprono solo campi visivi molto piccoli o richiedono decine di migliaia di immagini per costruire una singola immagine ad alta definizione, cosa impraticabile quando un patologo deve valutare ampie aree di tessuto. Gli stessi tessuti FFPE sono otticamente complessi: diffondono la luce, emettono autofluorescenza e possono nascondere le molecole che devono essere marcate, il che può provocare immagini sfocate o strutture artefatte. Alcuni metodi richiedono coloranti speciali, buffer personalizzati o trattamenti chimici multi-step che non si integrano facilmente nei flussi di lavoro istologici standard. Inoltre, gli strumenti commerciali sono costosi e complessi da usare e i dati risultanti richiedono un intenso processamento e capacità di archiviazione computazionale.
Unire ottiche intelligenti e software intelligente
Per superare questi ostacoli, i ricercatori stanno combinando ottiche migliorate con imaging senza marcatori e intelligenza artificiale. Metodi ad alto rendimento e limitati dalla diffrazione come la ptychography di Fourier e la microscopia ottica non lineare possono scansionare rapidamente grandi sezioni FFPE, anche non colorate, e fornire mappe quantitative della struttura tissutale. Le piattaforme di patologia digitale ora catturano interi vetrini ad alta risoluzione e usano l’apprendimento automatico per rilevare tumori e quantificare biomarcatori come HER2, Ki-67 e PD-L1. Modelli di deep learning possono persino trasformare immagini a bassa risoluzione in viste a super-risoluzione, riducendo potenzialmente la necessità di parte dell’hardware specializzato e sfruttando meglio gli archivi di biopsie esistenti.
Cosa significa questo per i pazienti futuri
Gli autori concludono che una vera “istologia a super-risoluzione” dei campioni FFPE — che combini dettaglio a scala nanometrica, alta velocità, costi ragionevoli e compatibilità con le routine di laboratorio attuali — non è ancora pienamente realizzata, ma è alla portata. Con il perfezionarsi dei metodi ottici e il consolidarsi dell’analisi basata sull’IA, questi strumenti potrebbero rivelare sottili cambiamenti precoci nei tessuti oggi inosservati, migliorare la precisione diagnostica e guidare decisioni terapeutiche più personalizzate. A lungo termine, trasformare ogni blocco di cera archiviato in una mappa ad alta definizione della malattia potrebbe rivoluzionare sia la ricerca sia l’assistenza clinica.
Citazione: Villegas-Hernández, L.E., Dubey, V.K., Acharya, G. et al. Optical super-resolution histology of formalin-fixed paraffin-embedded tissue samples: challenges and opportunities. Nat Commun 16, 9760 (2025). https://doi.org/10.1038/s41467-025-64626-1
Parole chiave: microscopia a super-risoluzione, tessuto FFPE, patologia digitale, imaging ottico, diagnostica oncologica