Clear Sky Science · it
Nanozymi che espandono i confini della biocatalisi
Piccoli aiutanti che accelerano la chimica
Dal fare la birra al digerire la cena, la nostra vita dipende da aiutanti invisibili chiamati catalizzatori che fanno andare più veloci le reazioni chimiche. Per più di un secolo, i catalizzatori della biologia sono stati ritenuti soltanto proteine fragili e, più tardi, RNA catalitico. Questa recensione presenta i “nanozymi” – piccole particelle ingegnerizzate che si comportano come enzimi ma sono costruite con materiali robusti come metalli, ossidi e carbonio. Possono sopravvivere a caldo, freddo e condizioni aggressive, e stanno cominciando a rimodellare il nostro modo di pensare la chimica nei sistemi viventi, nelle malattie, nell’industria e persino nell’origine della vita.
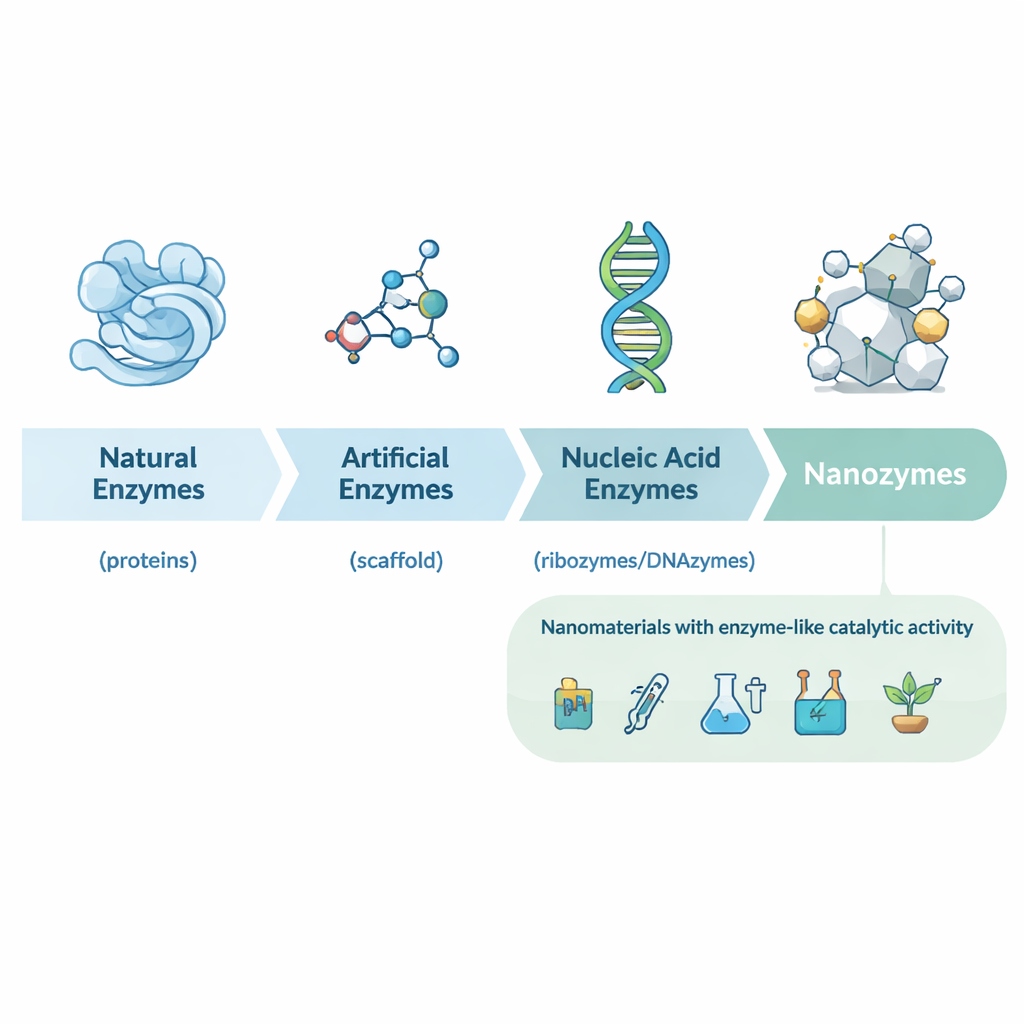
Dagli enzimi naturali ai nanocatalizzatori progettati
L’articolo ripercorre innanzitutto la storia della biocatalisi, dalle prime scoperte di enzimi proteici nel lievito e nei succhi gastrici fino ai ribozimi (RNA catalitico) e a una vasta gamma di enzimi artificiali costruiti con piccole molecole e anticorpi. Questi catalizzatori tradizionali sono potenti ma spesso costosi, instabili e difficili da produrre in massa. All’inizio degli anni 2000, i ricercatori scoprirono che alcuni nanomateriali – per esempio nanoparticelle di ossido di ferro – potevano imitare il comportamento di enzimi classici come la perossidasi di rafano. Da qui nacque il concetto di nanozymi: particelle su scala nanometrica la cui stessa struttura conferisce attività simile a quella degli enzimi, anziché dipendere da proteine o piccoli catalizzatori attaccati alla loro superficie.
Che cosa rende i nanozymi diversi
A differenza degli enzimi, che hanno una singola tasca attiva dalla forma precisa, i nanozymi espongono numerosi punti attivi sulla loro superficie. Questi punti possono trovarsi ai bordi dei cristalli, a difetti o alle interfacce tra due materiali e, collettivamente, possono trasformare molte molecole contemporaneamente. Un singolo sito attivo su un nanozima è di solito meno efficiente di quello di un enzima, ma una singola nanoparticella può ospitare migliaia di tali siti, perciò la sua potenza catalitica complessiva può eguagliare o superare quella degli enzimi naturali. La loro attività può inoltre essere modulata variando dimensione, forma, drogaggio chimico e rivestimenti superficiali – molto come regolare l’architettura e il cablaggio di una piccola macchina. Essendo fatti di solidi robusti piuttosto che di proteine ripiegate delicate, i nanozymi continuano a funzionare a temperature elevate, a basse temperature o in concentrazioni saline alte che disattiverebbero rapidamente la maggior parte degli enzimi.
Come funzionano i nanozymi e come vengono misurati
Gli autori mostrano che i nanozymi spesso seguono le stesse regole cinetiche di base che i biochimici usano per gli enzimi, come il comportamento di Michaelis–Menten, dove la velocità della reazione dipende da quanto facilmente un catalizzatore lega e converte il suo substrato. Ma ci sono svolte importanti. Una particella può ospitare più tipi di siti attivi, così un singolo nanozima può svolgere reazioni diverse o addirittura contrastanti, come generare e distruggere specie reattive dell’ossigeno. Questo può produrre curve cinetiche complesse “non da manuale” che mascherano più processi sotto un’unica tendenza liscia. La recensione spiega come i ricercatori dissecano questi comportamenti, stimano quanti siti attivi esistono realmente e confrontano l’attività complessiva di diversi nanozymi usando unità standardizzate, tutte operazioni cruciali per trasformare un materiale interessante in uno strumento affidabile.
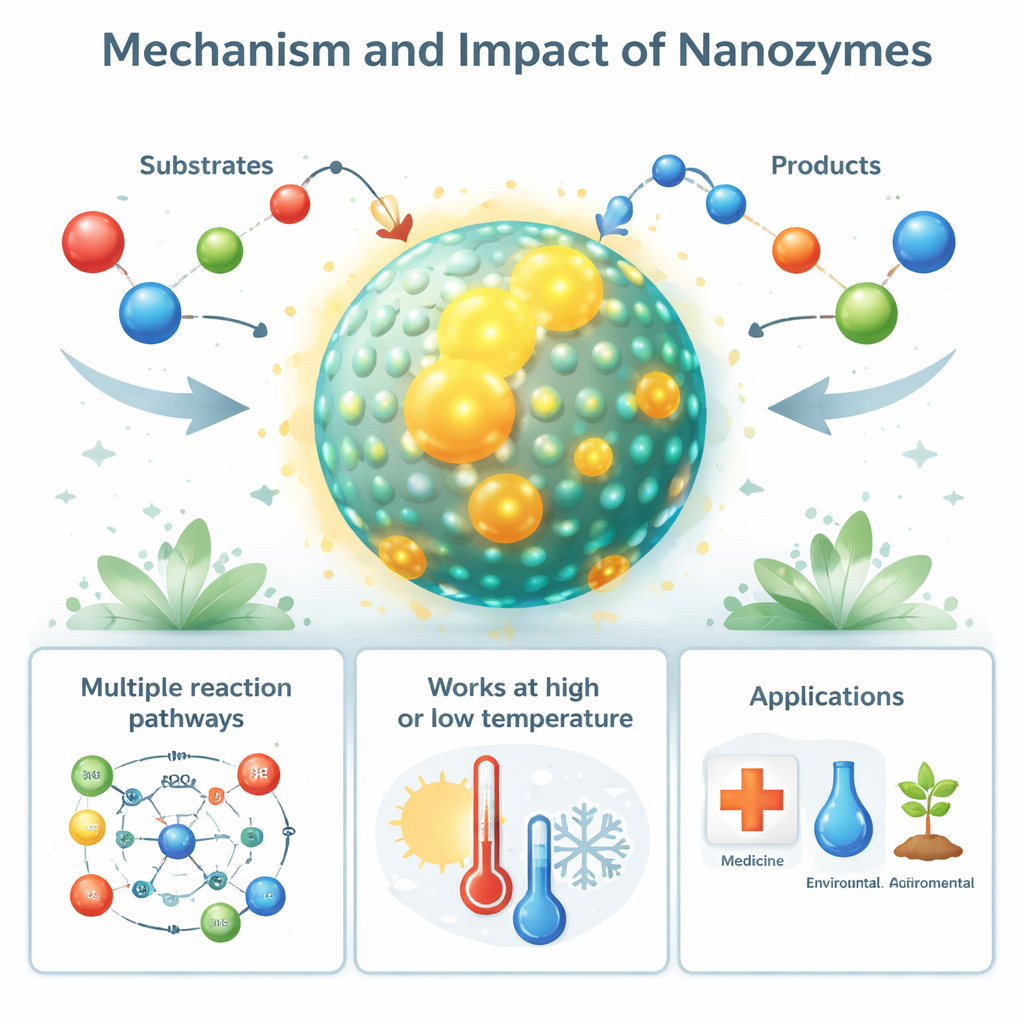
Dai nanozymi naturali agli usi nel mondo reale
Curiosamente, il comportamento simile ai nanozymi non è limitato al laboratorio. Alcune nanostrutture biologiche, come gabbie proteiche riempite di ferro (ferritina) e particelle magnetiche nei batteri (magnetosomi), agiscono come nanozymi naturali che aiutano a controllare le specie reattive dell’ossigeno dannose. Anche fibre proteiche correlate a malattie, come i depositi amiloidi nella malattia di Alzheimer, possono adottare un’attività perossidasica simile a quella dei nanozymi che danneggia le cellule vicine. Sul versante applicativo, i nanozymi sintetici sono impiegati come sostituti più economici e resistenti degli enzimi nei test diagnostici, nei biosensori e negli saggi industriali. La loro capacità di generare o rimuovere specie reattive dell’ossigeno viene sfruttata per uccidere cellule tumorali e batteri, proteggere i tessuti dallo stress ossidativo e aiutare le colture a resistere a siccità, salinità e inquinamento.
Progettare la prossima generazione di catalizzatori intelligenti
Guardando avanti, gli autori evidenziano le sfide chiave: individuare le esatte strutture atomiche che fungono da siti attivi, migliorare la selettività delle reazioni in modo che i nanozymi agiscano solo dove e quando desiderato, e garantire sicurezza e stabilità all’interno del corpo. Indicano tecniche di imaging avanzato, simulazioni a livello quantistico e apprendimento automatico come strumenti potenti per prevedere e ottimizzare le prestazioni dei nanozymi. Poiché i nanozymi possono operare in condizioni estreme, rispondere a luce, calore, suono o campi magnetici e talvolta eseguire più reazioni in sequenza, potrebbero sostenere nuove terapie, tecnologie ambientali e processi industriali. La recensione conclude che i nanozymi ampliano la stessa definizione di biocatalisi e potrebbero persino offrire indizi su come catalizzatori primitivi alimentassero un tempo la chimica dell’origine della vita.
Citazione: Zhang, R., Yan, X., Gao, L. et al. Nanozymes expanding the boundaries of biocatalysis. Nat Commun 16, 6817 (2025). https://doi.org/10.1038/s41467-025-62063-8
Parole chiave: nanozymi, biocatalisi, nanoparticelle, mimetici enzimatici, specie reattive dell'ossigeno