Clear Sky Science · it
Combinare la transcriptomica spaziale con la morfologia dei tessuti
Esplorare i tessuti in due modi diversi
Medici e ricercatori vogliono sempre più sapere non solo quali geni sono attivi in un tessuto, ma esattamente dove vengono accesi. Allo stesso tempo, i microscopi degli ospedali catturano già immagini ricche della struttura dei tessuti che i patologi utilizzano quotidianamente. Questo articolo spiega come un nuovo campo stia cercando di mettere in collegamento queste due prospettive — mappe dettagliate dell'attività genica e immagini microscopiche ordinarie — e perché questa integrazione potrebbe portare a diagnosi più precoci, una classificazione più accurata dei tumori e una comprensione più profonda di come le malattie si sviluppano e si diffondono.
Dalle cellule sparse alle mappe dell'attività genica
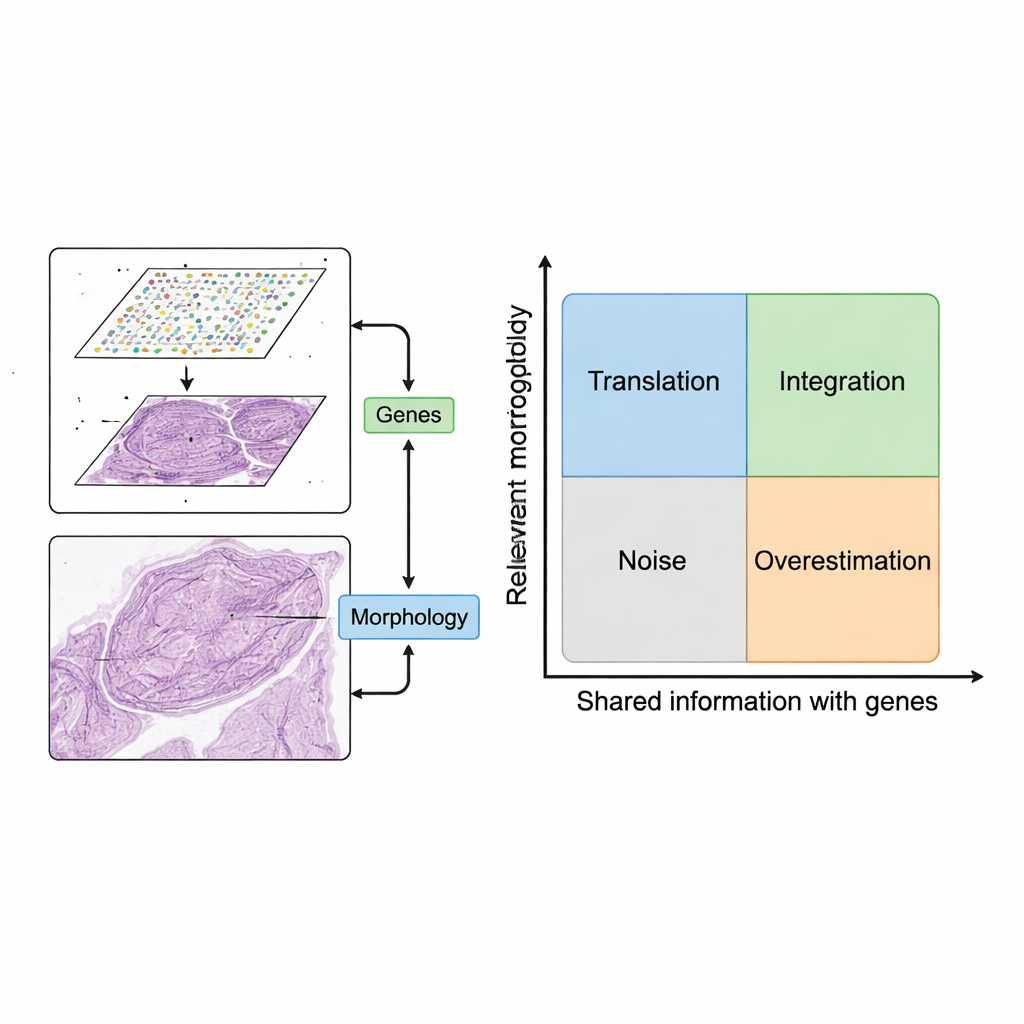
Per anni potenti metodi “omici” richiedevano che i tessuti venissero triturati in una miscela di singole cellule, distruggendo l'informazione sulla provenienza di ciascuna cellula. La transcriptomica spaziale ha cambiato questo approccio misurando l'attività genica mantenendo la posizione di ogni cellula nel tessuto. Il risultato è una griglia di punti, ognuno con un profilo di espressione genica e coordinate precise. Da sola, questa informazione spaziale sui geni ha già rivelato nuovi schemi di diversità cellulare e architettura della malattia. Tuttavia non è modificabile dopo la misurazione, e ripetere l'esperimento è costoso. In contrapposizione, le immagini tissutali colorate con colorazioni standard, come l'ematossilina-eosina (H&E) ampiamente usata, sono economiche e abbondanti, e contengono indizi visivi su forma cellulare, densità e organizzazione tissutale.
Due modi per combinare immagini e geni
La recensione propone un quadro semplice ma potente per utilizzare insieme queste due fonti di dati. Innanzitutto, le patch di immagine vengono associate ai punti di espressione genica vicini. Poi, modelli computazionali estraggono caratteristiche dalle immagini — schemi che catturano forma, texture e organizzazione — e le confrontano con i modelli nell'espressione genica. Gli autori descrivono due scenari desiderabili. Nella “traduzione”, le caratteristiche dell'immagine seguono da vicino l'attività genica pertinente, consentendo ai modelli di prevedere quali geni siano attivi usando soltanto l'immagine del tessuto. Questo può servire a riempire misurazioni geniche mancanti, raggiungere una risoluzione più fine rispetto alla griglia originale o inferire l'attività genica da vetrini clinici di routine senza ulteriori analisi di laboratorio. Nell’“integrazione”, le caratteristiche dell'immagine catturano informazioni utili che i dati genetici non colgono, come cambiamenti strutturali lenti o organizzazioni tissutali sottili, aiutando a definire regioni o “domini” più chiari all'interno di un tessuto.
Quando l'informazione aggiuntiva aiuta — e quando danneggia
Non tutte le caratteristiche dell'immagine valgono la pena di essere usate. Gli autori introducono una mappa concettuale con due assi: quanto una caratteristica dell'immagine è rilevante per la domanda biologica e quanto si sovrappone con l'informazione genica. Caratteristiche che non sono né rilevanti né correlate ai geni equivalgono a rumore, come artefatti di colorazione. Caratteristiche che seguono schemi genici ma sono legate a geni non importanti (per esempio geni “housekeeping” di base) possono far sembrare i modelli efficaci nei test pur aggiungendo poco valore clinico. Organizzando i metodi in quattro quadranti — traduzione, integrazione, rumore e sovrastima — il quadro chiarisce quando combinare immagini e dati genetici aggiunge realmente informazioni e quando semplicemente ripete o oscura ciò che è già noto.
Strumenti, test e difficoltà attuali
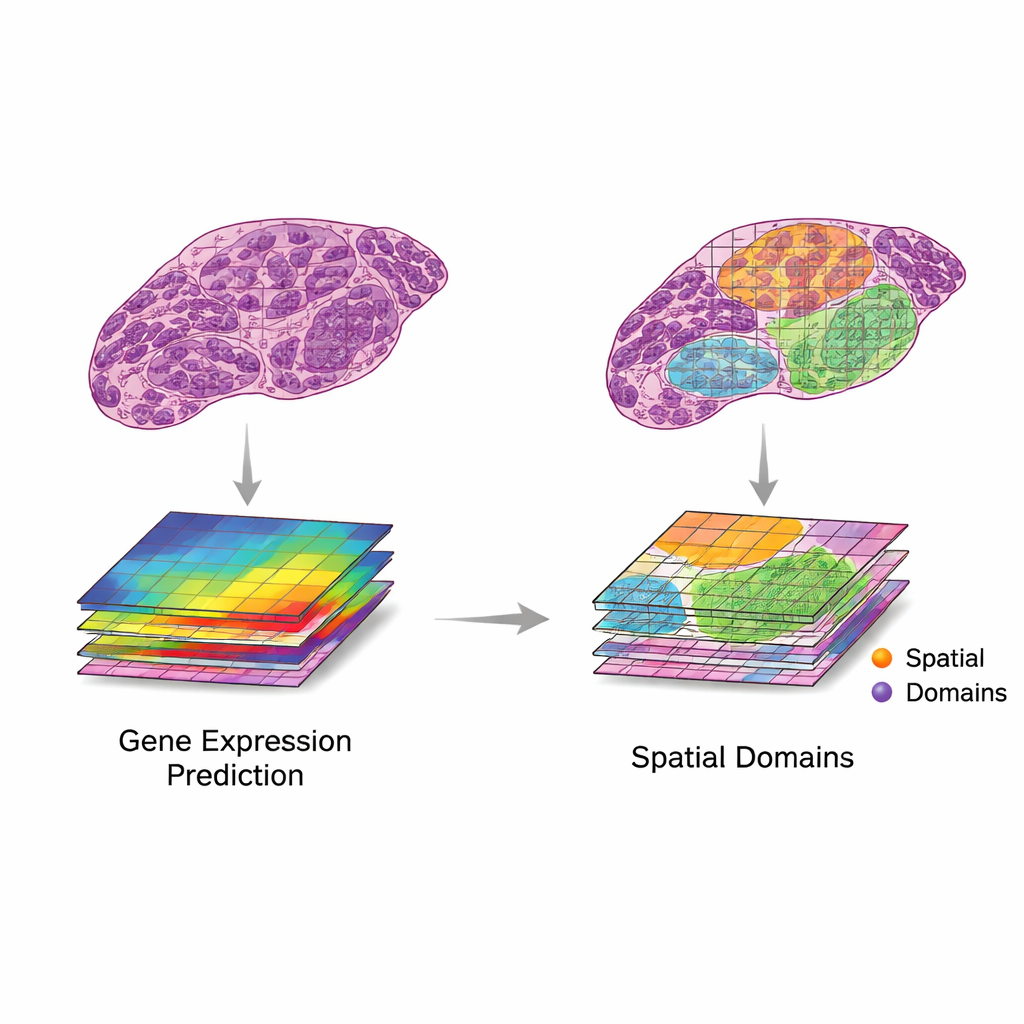
Un'ondata rapida di metodi di intelligenza artificiale ora prova a effettuare traduzione e integrazione su dati reali. I primi sistemi si basavano su reti neurali convoluzionali, mentre quelli più recenti impiegano transformer, reti neurali a grafi e modelli multi-scala in grado di cogliere dettagli dalle minuscole strutture cellulari fino al contesto dell'intero vetrino. Questi metodi sono stati usati per prevedere l'attività genica da immagini H&E, generare mappe a super‑risoluzione e aiutare a identificare regioni tissutali con comportamenti distinti. Per valutare le prestazioni, i ricercatori si affidano a misure statistiche come la correlazione tra livelli genici previsti e osservati o la concordanza tra regioni definite dall'IA e le etichette degli esperti patologi. Tuttavia, i dataset sono ancora piccoli e variabili, e il confronto tra studi è difficile. Molti miglioramenti riportati potrebbero riflettere overfitting o successi su geni e schemi che hanno scarso impatto clinico.
Dove potrebbe portare questo approccio
Gli autori concludono che combinare mappe geniche spaziali con immagini tissutali è un percorso promettente ma ancora in fase iniziale. I modelli odierni raggiungono spesso solo accuratezze moderate e non hanno ancora dimostrato di essere pronti per l'uso clinico di routine. I progressi futuri probabilmente arriveranno da caratteristiche d'immagine migliori, in particolare grandi “modelli fondamentali” addestrati su milioni di vetrini di patologia, e dal concentrarsi su geni e schemi che influenzano realmente la cura del paziente. Un'integrazione progettata con cura potrebbe un giorno rivelare segnali precoci di malattia individuando discrepanze tra l'aspetto attuale del tessuto e ciò che i suoi geni prevedono succederà. In breve, questo lavoro delinea una road map per trasformare immagini microscopiche di routine in mappe ricche e informate sui geni che aiutino i medici a comprendere e curare le malattie con maggiore precisione.
Citazione: Chelebian, E., Avenel, C. & Wählby, C. Combining spatial transcriptomics with tissue morphology. Nat Commun 16, 4452 (2025). https://doi.org/10.1038/s41467-025-58989-8
Parole chiave: transcriptomica spaziale, morfologia dei tessuti, patologia digitale, predizione dell'espressione genica, IA per l'imaging