Clear Sky Science · it
Rilevamento tramite nanopori della conformazione di proteine e peptidi per applicazioni point-of-care
Perché le piccole forme delle proteine potrebbero cambiare il tuo prossimo controllo medico
Con l’invecchiamento delle popolazioni, malattie come Alzheimer, Parkinson, cardiopatie e cancro diventano sempre più diffuse. Molte di queste patologie iniziano quando proteine essenziali e piccoli frammenti proteici (peptidi) cambiano sottilmente la loro forma molto prima che compaiano i sintomi. I test clinici attuali solitamente misurano quanto biomarcatore è presente, non se la sua forma è normale o alterata. Questo articolo esplora una tecnologia chiamata rilevamento con nanopori, che può “sentire” elettricamente la forma e la chimica di singole molecole proteiche, e sostiene che potrebbe diventare la base di futuri test point-of-care che si eseguono in pochi minuti su un piccolo dispositivo.
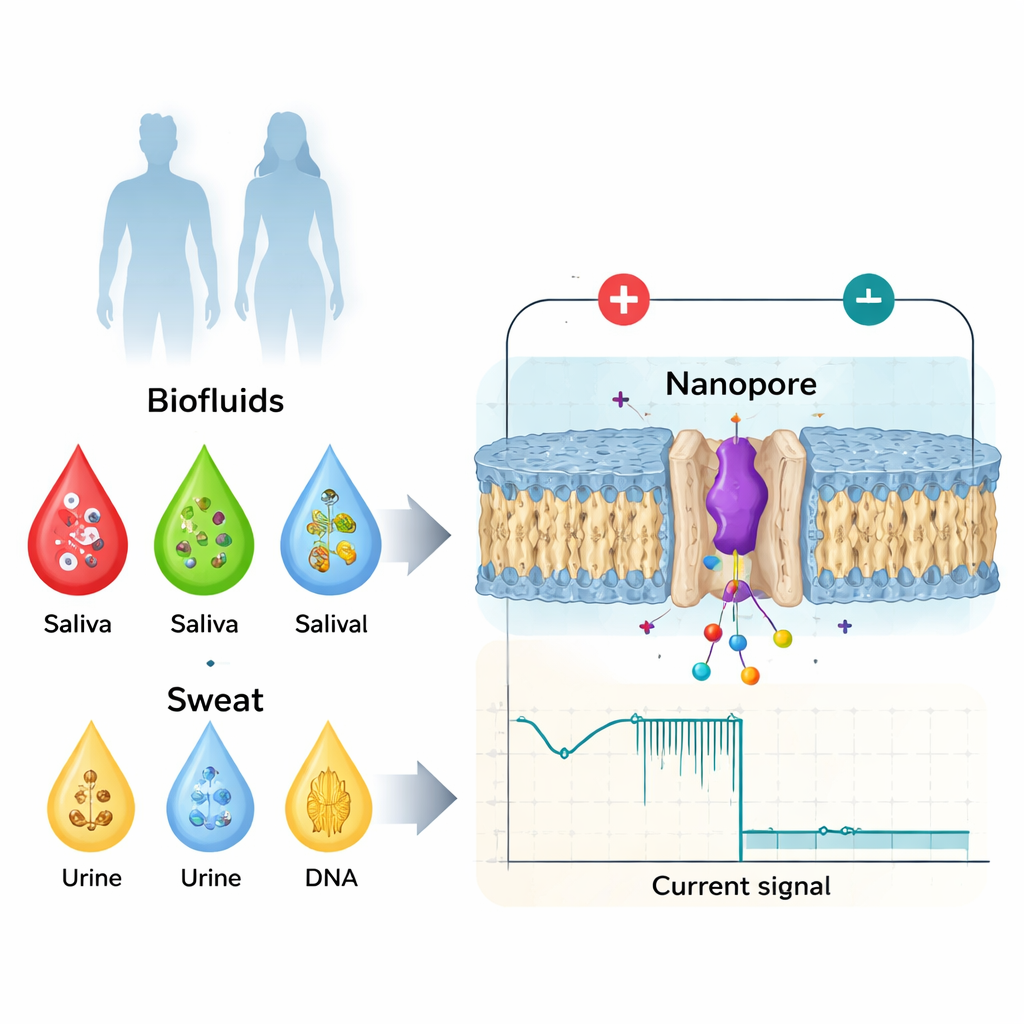
Dai semplici esami del sangue ai biomarcatori sensibili alla forma
I medici già usano molti biomarcatori prelevati da sangue, saliva, urine o sudore—come proteine, ormoni o piccole molecole—per monitorare salute e malattia. Tradizionalmente ci si è concentrati su variazioni evidenti: copie extra di una proteina, DNA danneggiato o la presenza di un componente virale. Ma la biologia è più sfumata. La stessa proteina può essere attivata o disattivata da piccole variazioni della sua struttura, da etichette chimiche aggiunte dopo la sintesi o da versioni speculari dei suoi mattoni costitutivi. Questi piccoli cambiamenti possono alterare il modo in cui una proteina si lega a partner, forma aggregati o trasmette segnali, e sono collegati a problemi di coagulazione, malattie neurodegenerative e cancro. Strumenti ospedalieri standard come spettrometria di massa, test basati su anticorpi e imaging ad alta risoluzione sono potenti, ma costosi, lenti, richiedono personale altamente qualificato e in genere non sono facilmente deployabili come dispositivi point-of-care rapidi e semplici.
Come funziona diversamente un nanoporo
Il rilevamento con nanopori rovescia il problema. Invece di fare la media su trilioni di molecole, esamina una alla volta mentre passa attraverso un foro minuscolo in una membrana, largo solo pochi miliardesimi di metro. Viene applicata una tensione in modo che ioni fluiscano attraverso il poro e creino una corrente elettrica stabile. Quando una proteina o un peptide entra nel poro, ne ostacola parzialmente la corrente. La profondità della caduta di corrente, la sua durata e i dettagli fini della sua forma dipendono dalle dimensioni, dalla carica e dalla conformazione della molecola (il suo ripiegamento tridimensionale). Progettando con cura il poro—usando proteine ingegnerizzate o materiali a stato solido—i ricercatori possono confinare singole biomolecole abbastanza a lungo da creare ricchi “impronte” elettriche che distinguono non solo proteine diverse, ma anche varianti sottili dello stesso biomarcatore.
Leggere cambiamenti rilevanti per la malattia, una molecola alla volta
La rassegna evidenzia come i nanopori siano già stati usati per risolvere differenze clinicamente importanti che altri metodi faticano a vedere. Possono distinguere peptidi che differiscono per un singolo amminoacido, rilevare varianti dell’emoglobina legate alla malattia direttamente dal sangue e discriminare peptidi simili agli ormoni che variano per un solo mattone costitutivo o perfino per una forma speculare di quel mattone. I nanopori possono anche rilevare modificazioni post-traduzionali—piccoli gruppi chimici come fosfato, zucchero o solfato—che regolano se proteine coinvolte in Alzheimer, Parkinson, coagulazione o cancro si comportano normalmente o patologicamente. In alcuni esperimenti, un singolo enzima o una proteina legante viene trattenuto all’interno del poro, e le variazioni del suo segnale elettrico rivelano, in tempo reale, come si lega ai partner o svolge reazioni, esponendo potenzialmente vie malfunzionanti nella malattia.
Verso test rapidi al letto del paziente
Poiché ogni evento di occlusione corrisponde a una singola molecola, i dispositivi a nanopori possono essere estremamente sensibili, rilevando anche solo migliaia di copie di un biomarcatore in un fluido complesso. Gli autori discutono strategie per superare gli ostacoli chiave per l’uso clinico: aumentare la velocità di cattura delle molecole rare, stabilizzare le membrane o utilizzare pori ibridi solido–biologici, e impiegare apprendimento automatico per classificare automaticamente pattern elettrici complessi in categorie diagnostiche chiare. Mostrano anche come approcci indiretti—come attaccare tag di DNA o partner leganti—possano amplificare segnali deboli o permettere la misura simultanea di più biomarcatori, conservando però gran parte del dettaglio conformazionale che rende i nanopori unici.
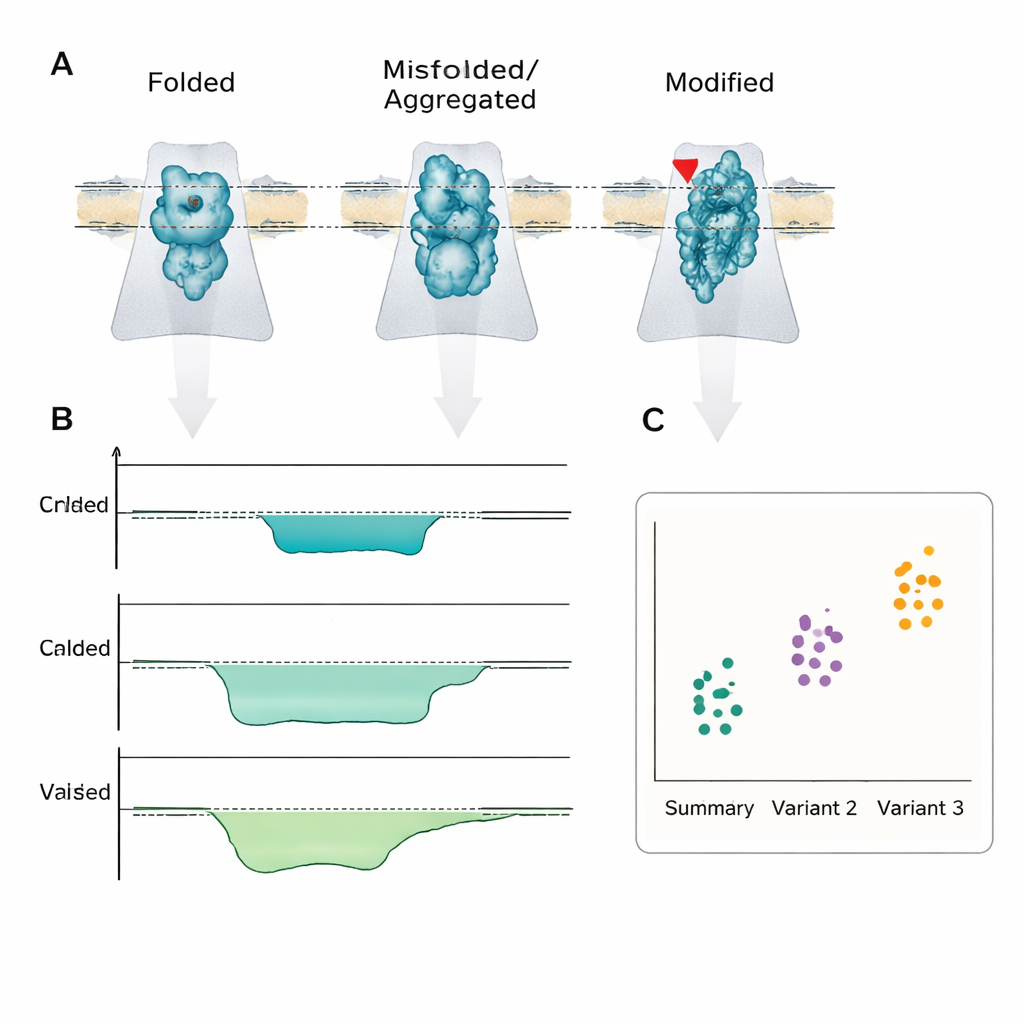
Cosa potrebbe significare per i pazienti
Il messaggio centrale è che la malattia è spesso determinata meno dalla quantità di proteina presente e più da quale forma o versione chimica è presente. Il rilevamento con nanopori è una delle poche tecnologie in grado di leggere direttamente queste differenze a livello di singola molecola, abbastanza rapidamente e semplicemente da poter essere integrata in dispositivi portatili. Sebbene rimangano importanti sfide di ingegneria e standardizzazione, gli autori sostengono che, così come i sequenziatori nanopore per il DNA sono entrati in ambito clinico, i sensori per proteine e peptidi basati su nanopori potrebbero infine fornire test rapidi al letto del paziente che non solo indicano che “c’è qualcosa che non va” ma rivelano anche il preciso malripiegamento o la modifica molecolare alla base della condizione del paziente.
Citazione: Ratinho, L., Meyer, N., Greive, S. et al. Nanopore sensing of protein and peptide conformation for point-of-care applications. Nat Commun 16, 3211 (2025). https://doi.org/10.1038/s41467-025-58509-8
Parole chiave: rilevamento con nanopori, biomarcatori proteici, diagnostica point-of-care, modificazioni post-traduzionali, malattie da malripiegamento