Clear Sky Science · it
Una lunga strada verso genomi di piante medicinali affidabili e completi
Perché le mappe del DNA delle piante contano per la salute umana
Molti dei farmaci più potenti di oggi — da antitumorali come il paclitaxel a antidolorifici come la morfina e l’antimalarico artemisinina — provengono dalle piante. Eppure per la maggior parte delle piante medicinali gli scienziati non hanno ancora un “manuale di istruzioni” completo del loro DNA. Questa recensione spiega come le nuove tecnologie genomiche stiano trasformando la nostra capacità di leggere quei manuali, perché i genomi vegetali attuali sono spesso ancora incompleti o difettosi, e come genomi veramente accurati potrebbero sbloccare farmaci migliori, produzioni più sostenibili e una conservazione migliorata delle specie di valore.
La promessa di leggere i progetti delle piante medicinali
Per millenni le persone si sono affidate a rimedi a base di erbe, e la farmacologia moderna continua a attingere fortemente ai prodotti naturali delle piante. Queste molecole specializzate — alcaloidi, terpenoidi, composti fenolici e molti altri — sono prodotte tramite percorsi metabolici intricati codificati nel DNA delle piante. Fino a poco tempo fa, gli scienziati dovevano ricostruire questi percorsi usando strumenti lenti e laboriosi come il tracciamento con isotopi e il clonaggio gene‑per‑gene. L’arrivo di sequenziamenti del DNA ad alta produttività e a costi accessibili ha cambiato il quadro. A febbraio 2025, i genomi di 431 piante medicinali (in 203 specie) erano stati sequenziati, dando ai ricercatori un modo sistematico per cercare i geni dei percorsi, capire come sono regolati i composti preziosi ed esplorare come queste chimie si siano evolute.
Un boom nel sequenziamento, ma molti genomi imperfetti
Le tecnologie di sequenziamento a letture lunghe di PacBio e Oxford Nanopore, abbinate a dati a letture corte Illumina e a metodi di mappatura a livello di cromosoma come Hi‑C, hanno migliorato drasticamente la qualità dei genomi vegetali. Quasi la metà di tutti gli assemblaggi di piante medicinali sono stati rilasciati negli ultimi tre anni, e la maggior parte dei genomi recenti è ora costruita a scala cromosomica. Tuttavia, la recensione mostra che la quantità ha superato la qualità. Più della metà dei genomi esistono soltanto in una versione iniziale, molti rimangono a livello di bozza, e solo 11 piante medicinali hanno assemblaggi “da telomero a telomero” (T2T) senza gap che catturano pienamente centromeri e altre regioni ripetitive. Metriche standard come l’N50 (una misura della contiguità) e i punteggi BUSCO (una misura dei geni conservati) appaiono complessivamente promettenti, ma possono mascherare lacune critiche proprio dove risiedono i geni chiave della biosintesi.
Lacune nascoste dove dovrebbero esserci i geni dei farmaci
Per testare quanto siano utili i genomi attuali, gli autori hanno esaminato geni di percorsi noti e sperimentalmente validati in nove piante medicinali ben studiate. Anche in alcuni assemblaggi a livello cromosomico, enzimi importanti per composti come i ginsenosidi nel ginseng o l’artemisinina in Artemisia annua risultavano completamente assenti o solo parzialmente catturati. In altri casi, i geni erano presenti nella sequenza grezza del genoma ma assenti o troncati nelle annotazioni geniche ufficiali, rendendoli difficili da trovare. Un esempio eclatante viene dall’erba produttrice di cumarine Peucedanum praeruptorum: un vecchio genoma a livello cromosomico aveva spezzato un gene chiave e ne aveva perso altri due; un nuovo assemblaggio T2T non solo ha ripristinato questi geni ma ha anche rivelato che diversi di essi si trovano insieme in un cluster genico biosintetico compatto. Questo tipo di mappa di cluster è esattamente ciò di cui i ricercatori hanno bisogno per ingegnerizzare piante o microrganismi e produrre farmaci in modo più efficiente.
Perché i genomi vegetali sono così difficili da assemblare
Le piante medicinali pongono sfide speciali che vanno oltre quelle di molte specie coltivate. I loro genomi spesso presentano alti livelli di eterozigosi (molte differenze di DNA tra le due copie di ciascun cromosoma), poliploidia frequente (set di cromosomi multipli) e grandi frazioni di DNA ripetitivo — caratteristiche che confondono gli algoritmi di assemblaggio e portano a rotture o giunzioni errate. Circa un terzo delle piante medicinali sequenziate ha genomi con più del 70% di contenuto ripetitivo, e oltre un quarto mostra eterozigosi molto elevata. Ottenere linee altamente consanguinee o isolare tessuti aploidi può aiutare, ma ciò è lento, costoso o biologicamente difficile per molte specie. Nuove strategie che assemblano separatamente ogni aplotipo parentale, e algoritmi più potenti tarati per genomi ricchi di ripetizioni e poliploidi, stanno iniziando ad attenuare questi ostacoli ma non sono ancora la norma.
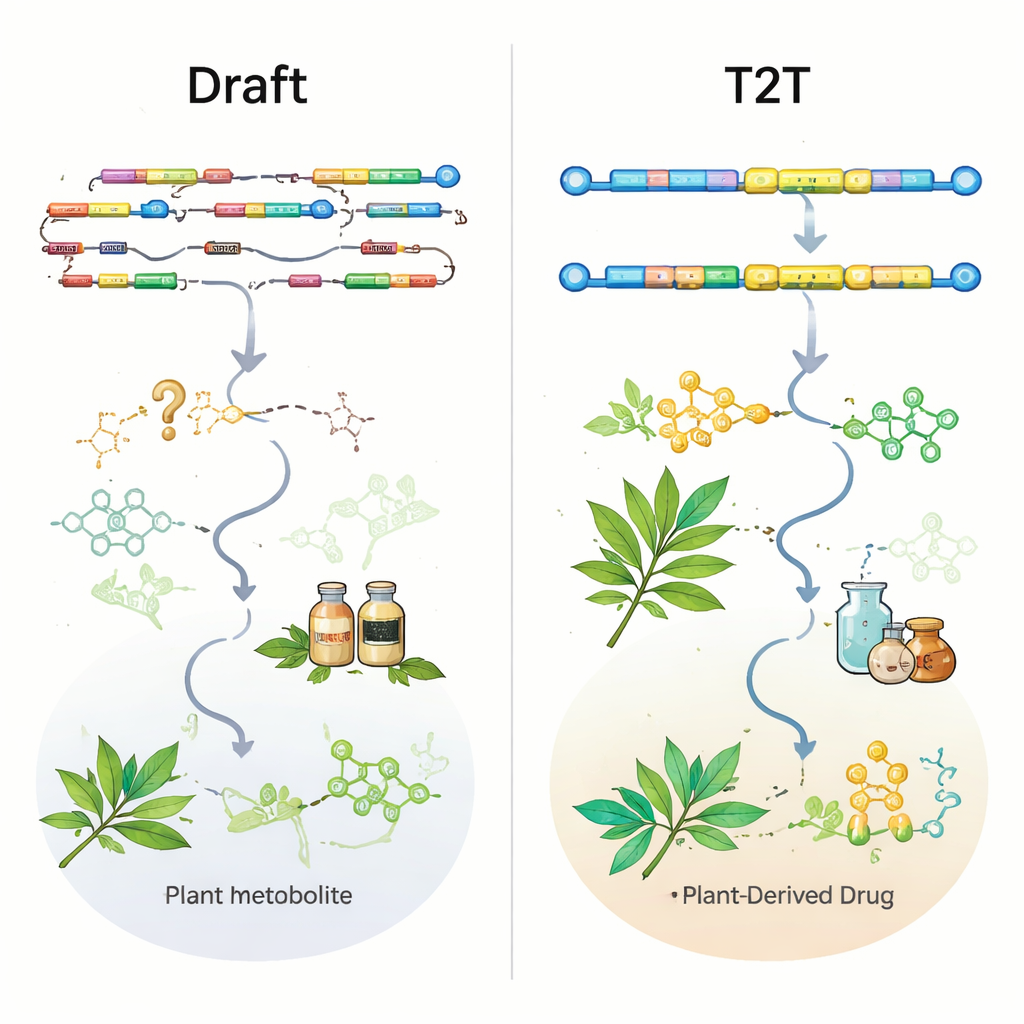
Dai genomi a nuovi farmaci e direzioni future
Quando i genomi sono sufficientemente buoni, diventano potenti motori di scoperta. I ricercatori possono combinare i dati del genoma intero con trascrittomica, metabolomica e biologia sintetica per individuare enzimi, geni regolatori e cluster genici biosintetici che controllano la produzione di composti di alto valore. Queste intuizioni hanno già permesso la ricostruzione di percorsi vegetali complessi — come quelli per la vinblastina, il paclitaxel e molti altri farmaci — in lievito o in piante modello, aprendo la strada a una bioproduzione stabile e su larga scala. Guardando avanti, gli autori sostengono il passaggio da “un genoma grezzo per specie” a molteplici assemblaggi di alta qualità, T2T e risolti per aplotipo che catturino la diversità intra‑specifica, in modo analogo ai pan‑genomi nella ricerca sulle colture. Accoppiare questi genomi di riferimento con grandi programmi di resequenziamento, fenotipizzazione avanzata e le emergenti tecnologie di trascrittomica cellulare e spaziale dovrebbe chiarire come ambiente, tipo cellulare e reti geniche interagiscano per modellare la chimica medicinale.
Cosa significa per i pazienti e per il pianeta
Il messaggio centrale della recensione è che genomi di piante medicinali affidabili e completi non sono un lusso; sono la base per trasformare secoli di conoscenza erboristica in terapie moderne e precise. Genomi migliori aiuteranno gli scienziati a trovare passaggi mancanti nei percorsi farmacologici, a progettare forniture più sicure e abbondanti di farmaci critici e a identificare specie alternative in grado di produrre gli stessi composti. Guidaranno inoltre la conservazione e l’uso sostenibile delle piante medicinali minacciate, la maggior parte delle quali è ancora priva di qualsiasi risorsa genomica. In breve, completare il lavoro di mappatura accurata di questi genomi potrebbe accelerare la scoperta di farmaci, stabilizzare le catene di approvvigionamento e preservare la diversità botanica — tutti benefici che, in ultima analisi, avvantaggiano la salute umana.
Citazione: Cheng, LT., Wang, ZL., Zhu, QH. et al. A long road ahead to reliable and complete medicinal plant genomes. Nat Commun 16, 2150 (2025). https://doi.org/10.1038/s41467-025-57448-8
Parole chiave: genomica delle piante medicinali, cluster genici biosintetici, genomi da telomero a telomero, biosintesi di prodotti naturali, biologia sintetica