Clear Sky Science · it
Illuminare l’impatto dell’acetilazione N-terminale: dalla proteina alla fisiologia
Come piccole etichette chimiche possono cambiare il comportamento delle proteine
Ogni cellula del corpo è piena di proteine che devono ripiegarsi correttamente, andare nel posto giusto, assemblarsi in macchine molecolari e venire rimosse quando sono danneggiate. Questo articolo di recensione esplora un cambiamento chimico sottile ma estremamente comune a un’estremità di molte proteine — chiamato acetilazione N-terminale — e mostra come questo piccolo “cappuccio” aiuti a controllare tutto, dalla crescita cellulare e le risposte allo stress allo sviluppo del cuore e alla funzione cerebrale.
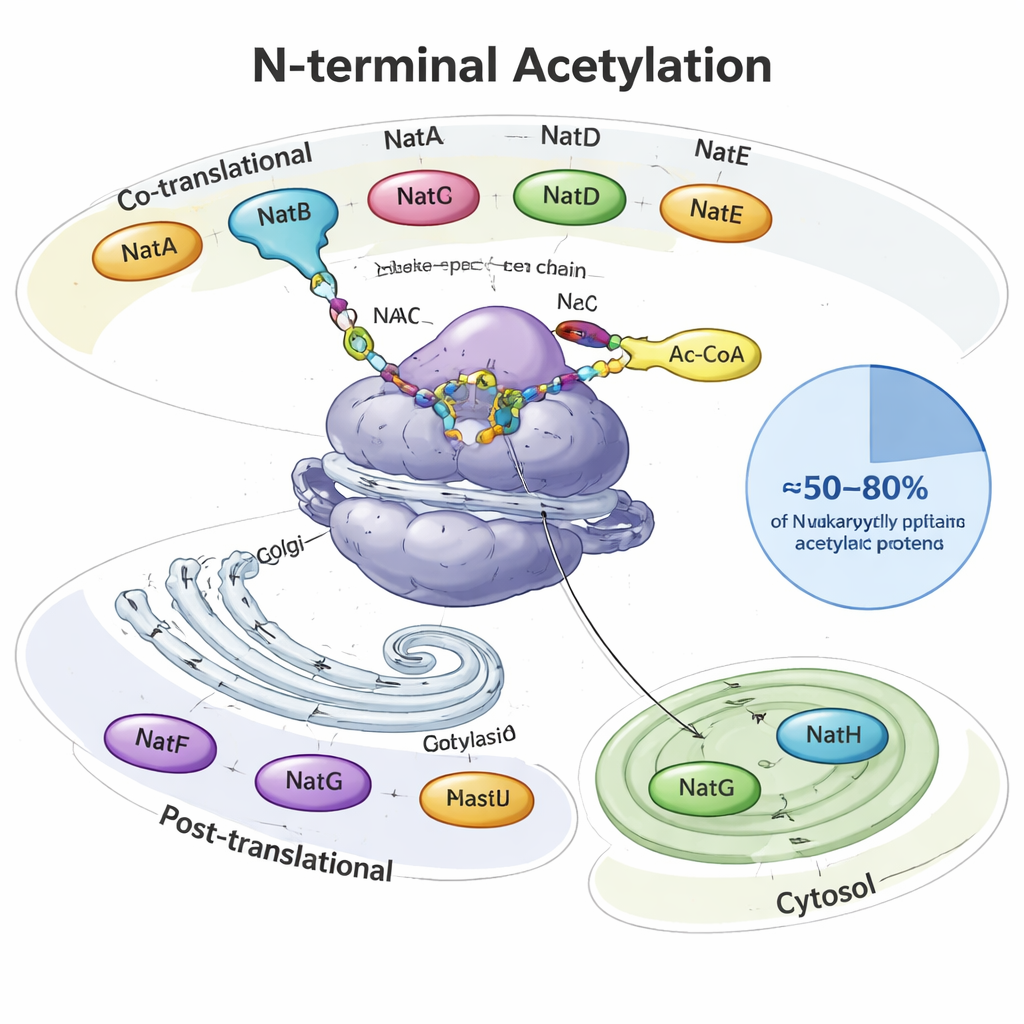
Il cappuccio delle proteine di cui la maggior parte di noi non ha mai sentito parlare
Quando una proteina viene sintetizzata, emerge dalla “fabbrica” proteica della cellula, il ribosoma, come un filo che cresce. All’inizio stesso — l’N-terminale — molte proteine eucariotiche ricevono un gruppo acetile, un minuscolo cappuccio di due atomi di carbonio. Enzimi specializzati chiamati acetiltransferasi N-terminali (NAT) svolgono questo compito, usando una comune molecola metabolica (acetil‑CoA) come donatrice. In lieviti, piante e animali, otto tipi principali di NAT (NatA–NatH) si dividono il lavoro. Alcuni agiscono mentre la proteina è ancora in fase di sintesi, altri operano dopo ed sono collocati in posizioni specifiche come l’apparato di Golgi o i plastidi delle piante. Insieme modificano circa metà fino a quattro quinti di tutte le proteine cellulari, ciascun NAT riconoscendo sequenze iniziali preferite di due‑quattro amminoacidi.
Molti enzimi, ognuno con la propria specialità
NatA, NatB e NatC sono i lavoratori principali, agendo proprio al ribosoma e coprendo vaste porzioni dell’“acetiloma N-terminale”. Solo NatA può modificare circa il 40% delle proteine umane, in genere quelle il cui primo metionina è stata rimossa. NatB e NatC agiscono su proteine che mantengono la metionina iniziale, ma differiscono nei residui amminoacidici adiacenti che preferiscono. Altri NAT sono più selettivi: NatD si concentra su poche istone che impacchettano il DNA, NatF prende di mira proteine transmembrana al Golgi, NatG opera all’interno dei plastidi vegetali, e NatH (NAA80) completa un particolare processo di maturazione in due fasi sull’actina, un componente chiave dello scheletro cellulare. L’articolo riunisce studi strutturali e biochimici che mostrano come subunità di supporto ancorino questi enzimi ai ribosomi o alle membrane e affinino quali proteine vengano modificate.
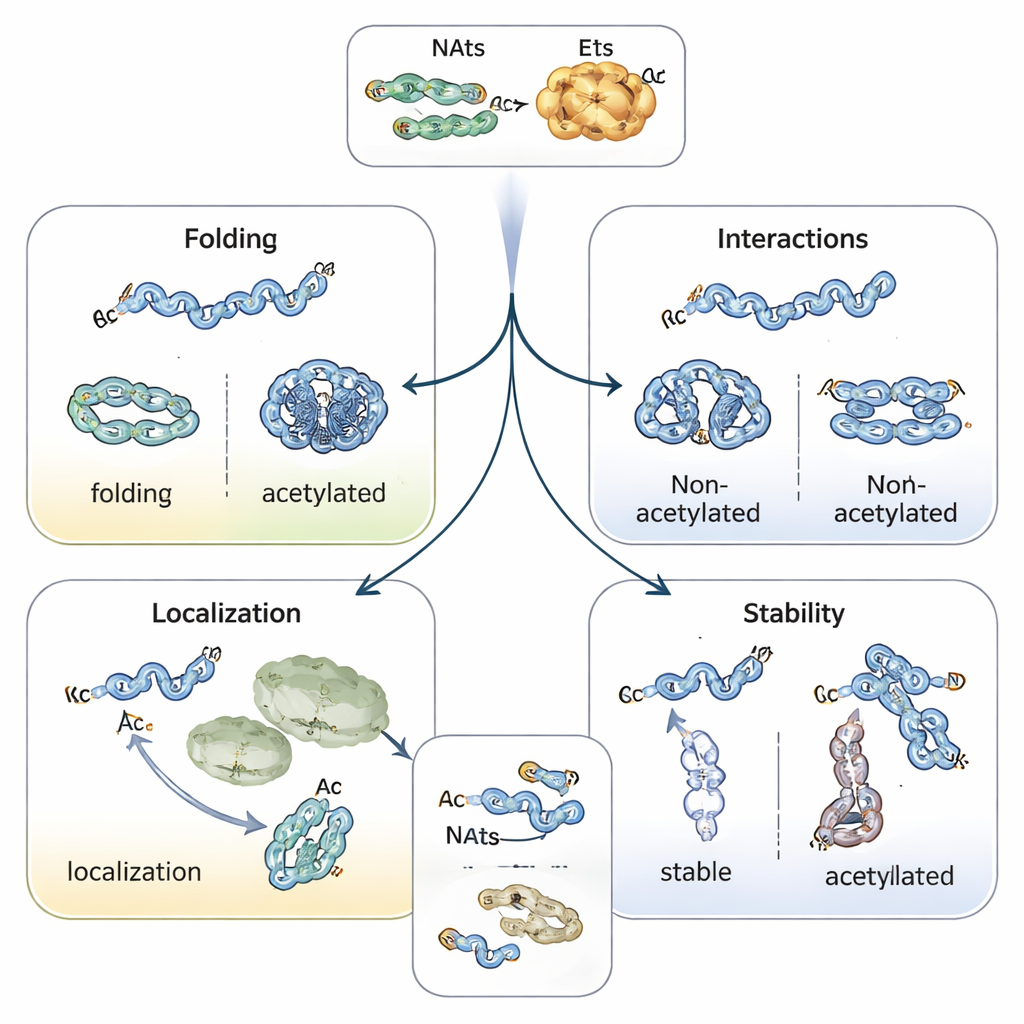
Indirizzare il ripiegamento, la localizzazione e la durata delle proteine
Aggiungere un cappuccio acetile cambia la natura chimica dell’inizio della proteina, stabilizzando spesso strutture eliche e influenzando il modo in cui le proteine si ripiegano. Ad esempio, la proteina associata al morbo di Parkinson, alfa‑sinucleina, tende ad aggregarsi meno e ad adottare una forma più sicura quando il suo N-terminale è acetilato. La tropomiosina, partner dell’actina, si lega e regola i filamenti di actina molto meglio quando è correttamente acetilata. In piante e animali, l’acetilazione N-terminale può funzionare come una sorta di etichetta d’indirizzo, aiutando le proteine a trovare cloroplasti, lisosomi o il Golgi. Forse più sorprendente è il suo ruolo nel determinare la durata della vita delle proteine: un N-terminale non protetto può essere interpretato come un “segnale di degradazione” dagli enzimi che attaccano ubiquitina, mentre l’acetilazione può mascherare quel segnale e stabilizzare la proteina — o, in alcuni casi, creare un’etichetta condizionata che viene riconosciuta solo quando la proteina è mal ripiegata o non è nel complesso giusto.
Dalla fisiologia cellulare allo sviluppo e alla malattia
Poiché l’acetilazione N-terminale interessa così tante proteine, la perturbazione dei NAT ha conseguenze ampie per gli organismi interi. La rimozione di NatA, NatB o NatC in specie modello spesso causa gravi difetti dello sviluppo, risposte allo stress alterate o perfino letalità, mentre enzimi più specializzati come NatF e NatH producono problemi più circoscritti come calcificazioni cerebrali o perdita dell’udito. Nell’uomo, mutazioni ereditarie in diversi geni NAT sono alla base di sindromi neuroevolutive rare con disabilità intellettiva, difetti cardiaci o debolezza muscolare. La stessa macchina è frequentemente iperattiva nei tumori, dove livelli elevati di NAT correlano con una prognosi sfavorevole e possono promuovere la crescita tumorale, la metastasi e la resistenza alla terapia. Variazioni nell’acetilazione N-terminale influenzano anche proteine propense all’aggregazione come alfa‑sinucleina e huntingtina, collegando questa modificazione a meccanismi delle malattie neurodegenerative.
Direzioni future e prospettive mediche
Gli autori concludono che, sebbene ora conosciamo la maggior parte degli enzimi di base che aggiungono questi cappucci N‑terminali, comprendiamo ancora solo una frazione dei bersagli proteici specifici e delle regole regolatorie. Un tema principale è che l’acetilazione all’inizio della proteina spesso la protegge dalla distruzione prematura, pur creando segnali contestuali per il controllo di qualità. Identificare quali ligasi dell’ubiquitina leggono quali schemi N‑terminali e scoprire se esista qualche enzima in grado di rimuovere questi cappucci sono domande chiave ancora aperte. Poiché i NAT si trovano all’incrocio tra stabilità proteica, regolazione genica e risposte allo stress cellulare, inibitori selettivi dei NAT — e forse futuri strumenti che modulano l’acetilazione N‑terminale di proteine specifiche coinvolte nelle malattie — emergono come vie promettenti per nuove terapie in cancro, malattie cardiache e neurodegenerazione.
Citazione: McTiernan, N., Kjosås, I. & Arnesen, T. Illuminating the impact of N-terminal acetylation: from protein to physiology. Nat Commun 16, 703 (2025). https://doi.org/10.1038/s41467-025-55960-5
Parole chiave: modificazione proteica, acetilazione N-terminale, controllo di qualità delle proteine, malattie neurodegenerative, biologia del cancro