Clear Sky Science · it
La metilazione m6A dell'RNA modula la risposta antivirale nella malattia celiaca
Quando un virus e il glutine fanno squadra
La malattia celiaca è spesso percepita come un problema alimentare semplice: si assume glutine e l'intestino si danneggia. Questo studio racconta una storia più profonda, in cui un comune virus intestinale e un minuscolo marcatore chimico sui nostri RNA collaborano per spingere il sistema immunitario verso un danno duraturo. Comprendere questo livello nascosto di controllo può aiutare a spiegare perché solo alcune persone sviluppano la celiachia e indicare nuove terapie che vadano oltre la dieta senza glutine. 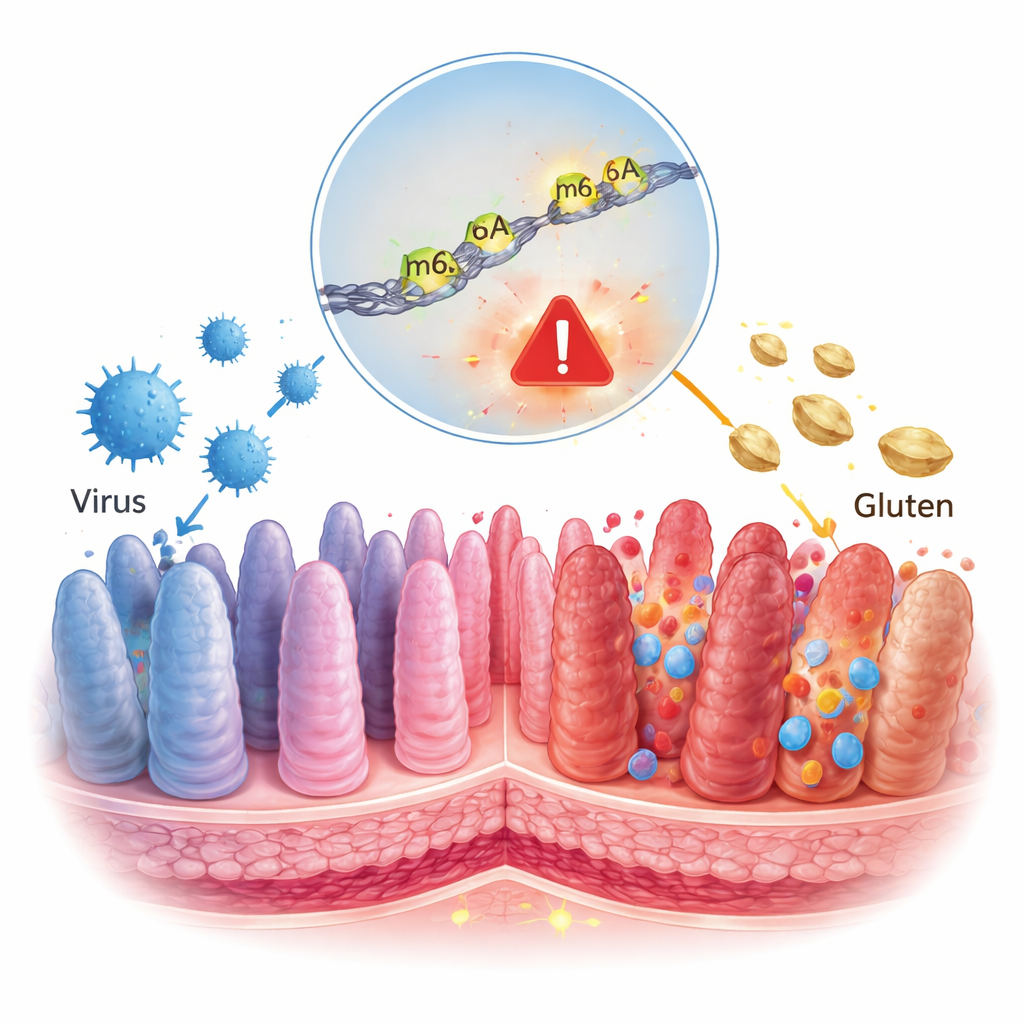
Un marcatore nascosto sui nostri messaggi genetici
Le nostre cellule leggono costantemente i geni e li copiano in RNA, brevi “messaggi” che dicono alla cellula quali proteine produrre. Questi messaggi non sono fissi; possono essere decorati con segni chimici che funzionano come evidenziatori, modificando l'intensità con cui un messaggio viene letto. Uno dei segni più comuni è chiamato m6A, una piccola modifica alle lettere dell'RNA. È noto che i virus alterano questi segni sull'RNA nelle cellule infette, e lavori precedenti avevano già collegato m6A al modo in cui il glutine scatena l'infiammazione nell'intestino celiaco. Gli autori di questo articolo si sono chiesti se una modifica m6A indotta dal virus potesse contribuire a far passare il sistema immunitario dalla tolleranza dell'alimento all'attacco.
Evidenze da pazienti con malattia celiaca
I ricercatori hanno prima esaminato sangue e biopsie intestinali di persone con malattia celiaca attiva e di controlli non celiaci. Hanno trovato che i pazienti celiaci presentavano livelli più alti di anticorpi contro il reovirus, un virus a RNA a doppio filamento che infetta l'intestino, suggerendo esposizioni più frequenti o più intense. Nel tessuto intestinale di questi pazienti, geni chiave di allarme antivirale, in particolare uno chiamato IRF7, risultavano maggiormente attivati, insieme a molecole infiammatorie come STAT1 e l'attrattore per cellule immunitarie CXCL10. Allo stesso tempo, la macchina cellulare che aggiunge e legge i segni m6A era più attiva, e i livelli totali di m6A sull'RNA erano più elevati. L'espressione dei geni antivirali aumentava e diminuiva in parallelo con quella dei geni legati a m6A, suggerendo che lo stesso sistema di controllo potesse guidare sia la difesa virale sia il danno autoimmune.
Come il glutine amplifica l'allarme virale
Per sondare causa ed effetto, il gruppo ha costruito un modello simile alla celiachia in cellule intestinali coltivate in laboratorio. Hanno simulato un'infezione virale usando un RNA a doppio filamento sintetico, quindi hanno aggiunto frammenti di glutine digerito simili a quelli che si troverebbero nell'intestino dopo un pasto. Il solo simulacro virale aumentava sia IRF3 sia IRF7, due interruttori principali delle risposte antivirali. Ma quando è stato aggiunto anche il glutine, IRF7 ha mostrato un forte incremento extra, mentre IRF3 no. I ricercatori hanno scoperto che, in queste condizioni, i segni m6A aumentavano in una regione specifica dell'RNA di IRF7, e che questo RNA interagiva fisicamente con un enzima che scrive m6A (METTL3) e con un enzima che lo cancella (ALKBH5). Aumentare m6A, sia aggiungendo più METTL3 sia riducendo ALKBH5, portava a livelli ancora più alti di IRF7, collegando direttamente la sinergia glutine‑più‑virus a questa modifica dell'RNA. 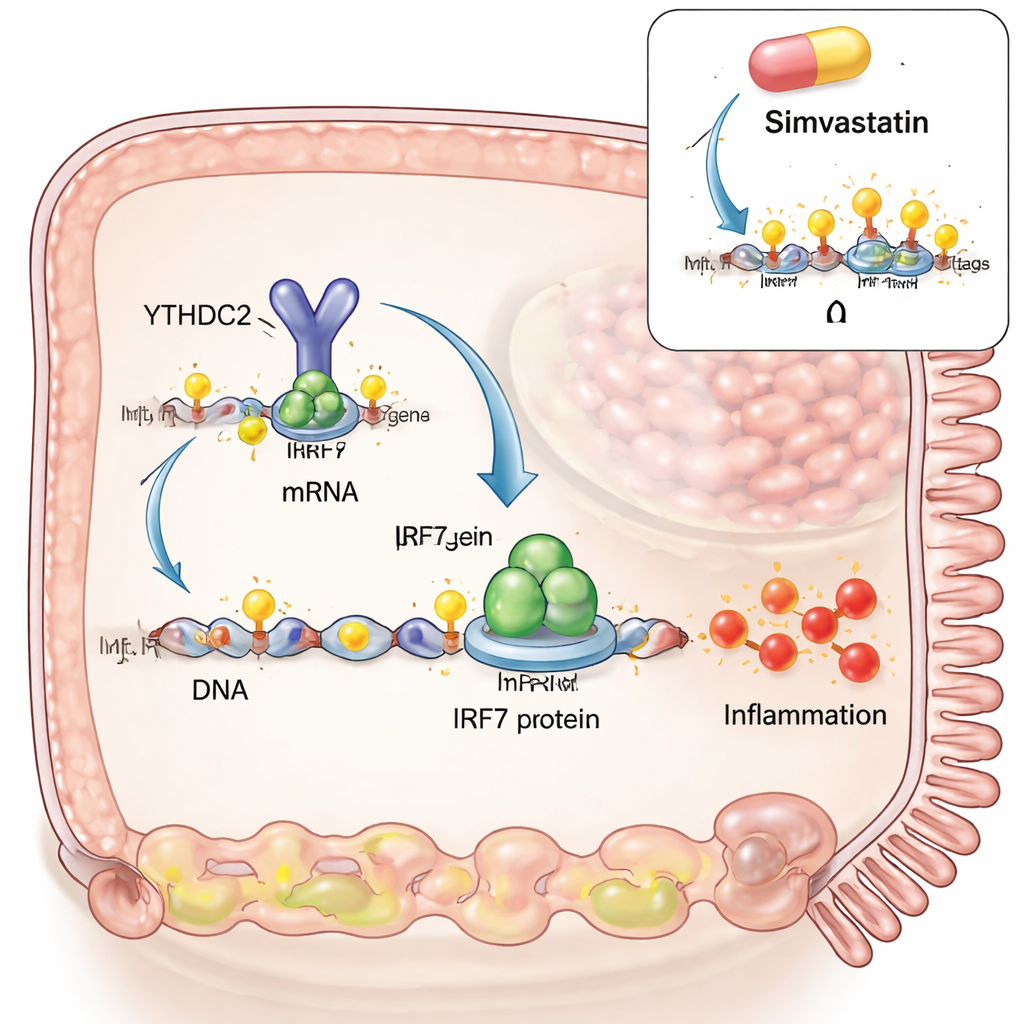
Il mediatore molecolare e un farmaco sorprendente
Successivamente, gli autori hanno indagato come i segni m6A sull'RNA di IRF7 modificassero effettivamente il comportamento cellulare. Hanno progettato una versione dell'RNA di IRF7 con lo stesso codificante proteico ma priva dei siti m6A. Quest'RNA produceva quantità simili di trascritto, ma molta meno proteina IRF7, e non riusciva ad attivare i geni infiammatori a valle come STAT1 e CXCL10. Il collegamento mancante era una proteina 'lettore' chiamata YTHDC2, che normalmente si lega a m6A all'interno della regione codificante e aiuta a favorire una traduzione efficiente in proteina. Senza i siti m6A, YTHDC2 non poteva più agganciarsi all'RNA di IRF7. Bloccare lo 'scrittore' m6A METTL3 nel modello cellulare riduceva la proteina IRF7 e CXCL10, abbassando la risposta infiammatoria. Un farmaco ipocolesterolemizzante, la simvastatina, che è stato recentemente mostrato ridurre m6A in altri tessuti, ha anch'esso ridotto m6A sull'RNA di IRF7, abbassato la proteina IRF7 nelle cellule e attenuato i geni correlati a IRF7 in biopsie intestinali celiache ottenute fresche e coltivate ex vivo. Confronti su larga scala di profili di espressione genica suggerivano che la simvastatina spingesse il tessuto celiaco verso un profilo più simile a quello dei pazienti in dieta priva di glutine.
Cosa significa per le persone con malattia celiaca
Questo lavoro disegna un quadro in cui un virus intestinale e il glutine agiscono insieme su uno strato finemente regolato di controllo dell'RNA. Nelle persone suscettibili, l'infezione virale sembra aumentare il marchio m6A sull'RNA di IRF7 nelle cellule intestinali. L'esposizione al glutine amplifica ulteriormente quel segnale marcato, portando a più proteina IRF7, allerte antivirali più forti e livelli più elevati di messaggeri infiammatori che contribuiscono all'attacco autoimmune della mucosa intestinale. Abbassando i segni m6A—sia geneticamente sia con un farmaco come la simvastatina—la catena di reazioni può essere smorzata, almeno nei modelli di laboratorio e negli esperimenti ex vivo. Per il pubblico generale, il messaggio chiave è che la malattia celiaca non riguarda soltanto ciò che si mangia, ma anche come infezioni e sottili marcature chimiche sugli RNA modellano la decisione del sistema immunitario di tollerare o attaccare. Mirare a questi segni sull'RNA potrebbe un giorno integrare la dieta senza glutine e ispirare nuovi trattamenti per una più ampia gamma di malattie autoimmuni.
Citazione: Sebastian-delaCruz, M., Olazagoitia-Garmendia, A., Pascual-Gonzalez, I. et al. m6A RNA methylation modulates antiviral response in celiac disease. Genes Immun 27, 130–139 (2026). https://doi.org/10.1038/s41435-025-00373-z
Parole chiave: malattia celiaca, metilazione dell'RNA, immunità antivirale, IRF7, simvastatina