Clear Sky Science · it
CRISPR-AuNP: ottimizzazione fisico-chimica di una piattaforma a nanoparticelle d'oro per l'editing genico non virale modulare e a basso costo nelle CSE
Portare l'editing genico a più pazienti
Strumenti di editing genico come CRISPR hanno già cambiato la vita di persone con malattie del sangue ereditarie, ma i trattamenti restano costosi, tecnicamente impegnativi e per lo più limitati a pochi centri specializzati. Questo articolo descrive un nuovo modo di consegnare CRISPR nelle cellule staminali ematopoietiche usando minuscole particelle a base d'oro che possono essere assemblate su un banco di laboratorio in poche ore. L'obiettivo è rendere gli approcci di editing genico potenti più semplici, economici e più facilmente distribuibili in più luoghi nel mondo.
Perché le cellule staminali del sangue sono importanti
Le cellule staminali e progenitrici ematopoietiche risiedono nel midollo osseo e riforniscono continuamente tutti i diversi tipi di cellule del sangue dell'organismo. Se i medici riescono a correggere in modo sicuro le mutazioni che causano malattie in queste cellule, un trattamento una tantum potrebbe fornire una cura permanente per condizioni come l'anemia falciforme e alcune immunodeficienze. Oggi, il metodo più comune per introdurre CRISPR in queste cellule è l'elettroporazione, un processo che usa impulsi elettrici per aprire pori nelle membrane cellulari. Pur essendo potente, l'elettroporazione è traumatica per le cellule, richiede apparecchiature costose e reagenti specializzati, e non si presta facilmente a scala o all'esportazione in contesti con risorse limitate. I vettori virali più sicuri sono eccellenti per molte terapie geniche, ma sono meno adatti alla consegna di CRISPR perché continuano a produrre gli strumenti di editing troppo a lungo, aumentando il rischio di modifiche fuori bersaglio.
Costruire un minuscolo veicolo di consegna in oro
I ricercatori hanno cercato di migliorare un sistema a nanoparticelle d'oro precedentemente descritto che portava componenti CRISPR sulla sua superficie. Nei progetti iniziali, l'RNA guida che indirizza la proteina di taglio CRISPR verso il bersaglio era ancorato direttamente al nucleo d'oro e poi associato alla proteina Cas9. Questo funzionava abbastanza bene per un tipo di enzima CRISPR, ma rese risultati scadenti con Cas9, centrale in molte strategie terapeutiche. Analizzando da vicino il comportamento di Cas9 e del suo RNA guida nelle condizioni acide usate durante l'assemblaggio delle particelle, il team scoprì che il duplex di RNA guida diventava instabile sulla superficie d'oro, portando a poco o nessun Cas9 attivo legato alla particella. La microscopia confocale suggerì inoltre che il rivestimento polimerico pensato per aiutare le particelle a uscire dai compartimenti cellulari si staccava prima di poter svolgere la sua funzione.
Riprogettazione della piattaforma per fasi
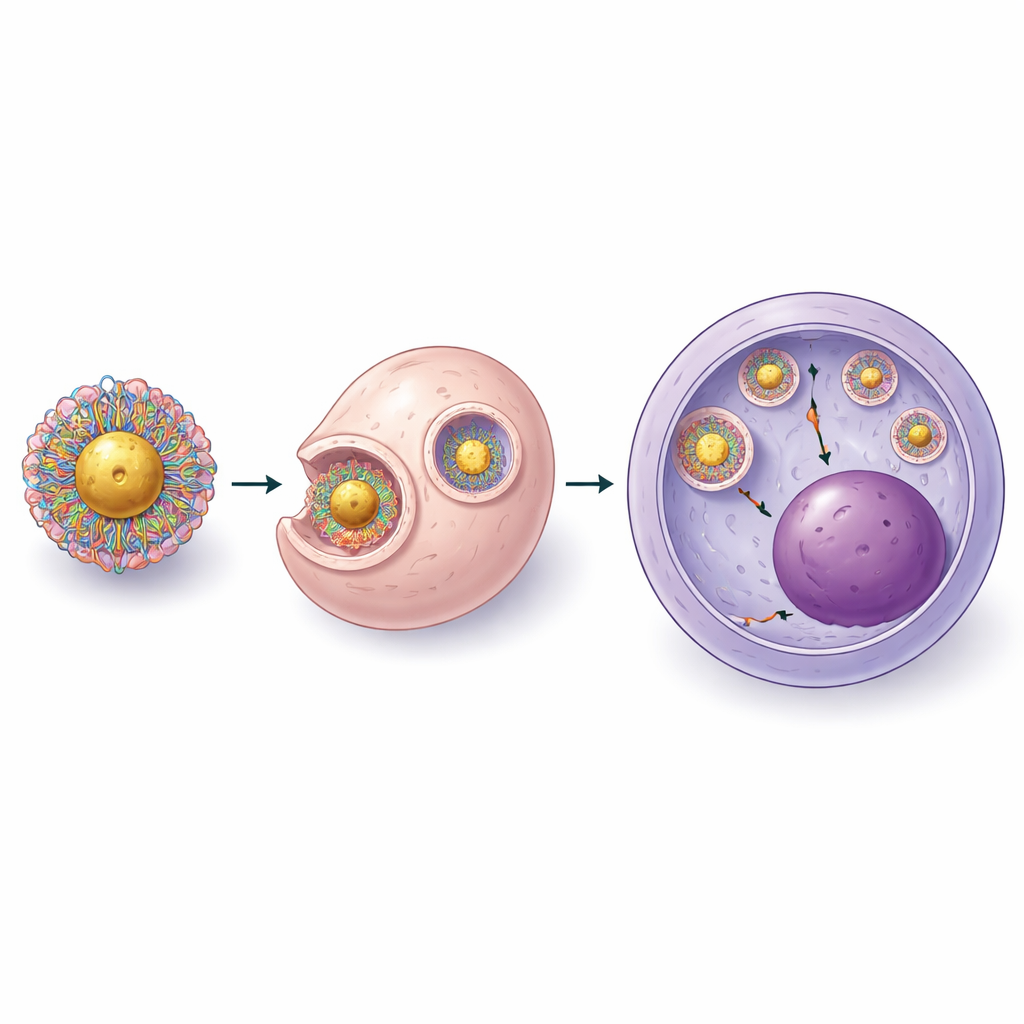
Per superare questi problemi, gli scienziati hanno ricostruito il sistema da zero in tre fasi. Innanzitutto, invece di ancorare RNA nudo all'oro e poi aggiungere la proteina, hanno formato complessi ribonucleoproteici CRISPR completi (proteina più RNA guida) prima di metterli a contatto con la superficie d'oro. Hanno identificato una condizione leggermente acida che permetteva a questi complessi di legarsi alle particelle mantenendo comunque l'attività della proteina di taglio. Successivamente, hanno rivestito le particelle caricate con polimeri appositamente ingegnerizzati che combinavano catene cariche positivamente—necessarie per la fuga dai compartimenti cellulari—con segmenti flessibili e idrofili di polietilenglicole che impediscono l'aggregazione. Misurando dimensione, carica superficiale e contenuto proteico, hanno dimostrato di poter caricare riproducibilmente decine di complessi CRISPR per particella mantenendo la stabilità in soluzione.
Forzare le difese cellulari
Anche con un carico migliorato, le particelle di seconda generazione incontravano ancora un ostacolo chiave: far uscire CRISPR dalle vescicole intracellulari e portarlo nella parte della cellula dove si trova il DNA. Il team ha quindi messo a punto in modo sistematico la chimica dello strato polimerico e il rapporto tra gruppi positivi sul polimero e gruppi negativi sul complesso CRISPR. Hanno scoperto che aggiungere più catene corte di polietilenglicole e un numero controllato di ancore contenenti zolfo migliorava sia la stabilità delle particelle sia la capacità di perturbare le membrane endosomiali senza danneggiare le cellule. Nel design finale, di terza generazione, hanno prima creato complessi compatti di CRISPR e polimero, poi li hanno attaccati a nuclei d'oro concentrati. La microscopia elettronica ha mostrato un sottile involucro di CRISPR e polimero attorno a ciascuna sfera d'oro, e le immagini in cellule staminali vive hanno confermato che il carico poteva uscire nell'interno cellulare e raggiungere il nucleo.
Risultati di editing con diversi strumenti CRISPR
Per testare l'efficacia delle particelle ottimizzate, i ricercatori hanno preso di mira un gene chiamato beta-2-microglobulina, che produce una proteina presente sulla superficie di quasi tutte le cellule del sangue e può essere misurata facilmente tramite citometria a flusso. Usando la loro piattaforma d'oro di terza generazione, hanno ottenuto oltre il 10% di interruzioni precise di questo gene in cellule staminali e progenitrici ematopoietiche umane primarie—livelli considerati significativi per molte applicazioni terapeutiche—mantenendo al contempo un'elevata sopravvivenza cellulare. Sebbene questa efficienza sia inferiore a quella ottenibile con l'elettroporazione, il sistema a base d'oro non richiedeva apparecchiature specializzate e causava uno stress minimo alle cellule. È importante che la stessa piattaforma potesse essere usata con diversi enzimi CRISPR, inclusi Cas9, Cas12a e un enzima più recente chiamato Cas12a-M29-1, con livelli di editing simili e nessuna tossicità rilevabile, mettendo in evidenza la natura modulare del design.
Cosa potrebbe significare per le terapie future
In termini semplici, questo lavoro mostra che è possibile costruire un piccolo vettore a base d'oro, attentamente ingegnerizzato, che può portare strumenti CRISPR in sensibili cellule staminali del sangue senza elettricità o virus, usando materiali pronti all'uso per meno di settanta dollari ogni milione di cellule. Pur richiedendo ulteriori miglioramenti per eguagliare l'efficienza dei migliori metodi clinici attuali, in particolare per malattie che richiedono livelli molto alti di cellule corrette, questa piattaforma assemblata su banco abbassa le barriere pratiche per eseguire editing genico sofisticato. Con continui perfezionamenti e test di sicurezza, tali nanoparticelle potrebbero aiutare a diffondere i benefici delle terapie basate su CRISPR oltre i centri specializzati, rendendo i trattamenti curativi più accessibili ai pazienti nel mondo.
Citazione: Gottimukkala, K.S.V., Lane, D.D., Cunningham, R. et al. CRISPR-AuNP: physicochemical optimization of a gold nanoparticle platform for cost-effective and modular non-viral gene editing in HSPCs. Gene Ther 33, 188–202 (2026). https://doi.org/10.1038/s41434-025-00591-0
Parole chiave: editing genico CRISPR, nanoparticelle d'oro, cellule staminali ematopoietiche, consegna non virale, nanomedicina