Clear Sky Science · it
Riconsiderare la genomica della distrofia muscolare facioscapolomerale nell’era telomero-a-telomero: insidie nel paesaggio nascosto delle ripetizioni D4Z4
Perché questa storia sulle malattie muscolari è importante
La distrofia muscolare facioscapolomerale (FSHD) è una delle più comuni malattie muscolari ereditarie caratterizzate da perdita di massa muscolare, spesso con indebolimento dei muscoli del viso e delle spalle in giovani adulti per il resto sani. Per anni i ricercatori si sono concentrati su un unico tratto di DNA vicino all’estremità del cromosoma 4 come causa principale. Questo nuovo studio mostra che il quadro è molto più complesso: ripetizioni di DNA simili sono diffuse in tutto il genoma e molti test di laboratorio standard non sono in grado di distinguerle. Comprendere questo paesaggio nascosto è essenziale per diagnosi accurate, ricerche migliori e, in ultima analisi, terapie più sicure.
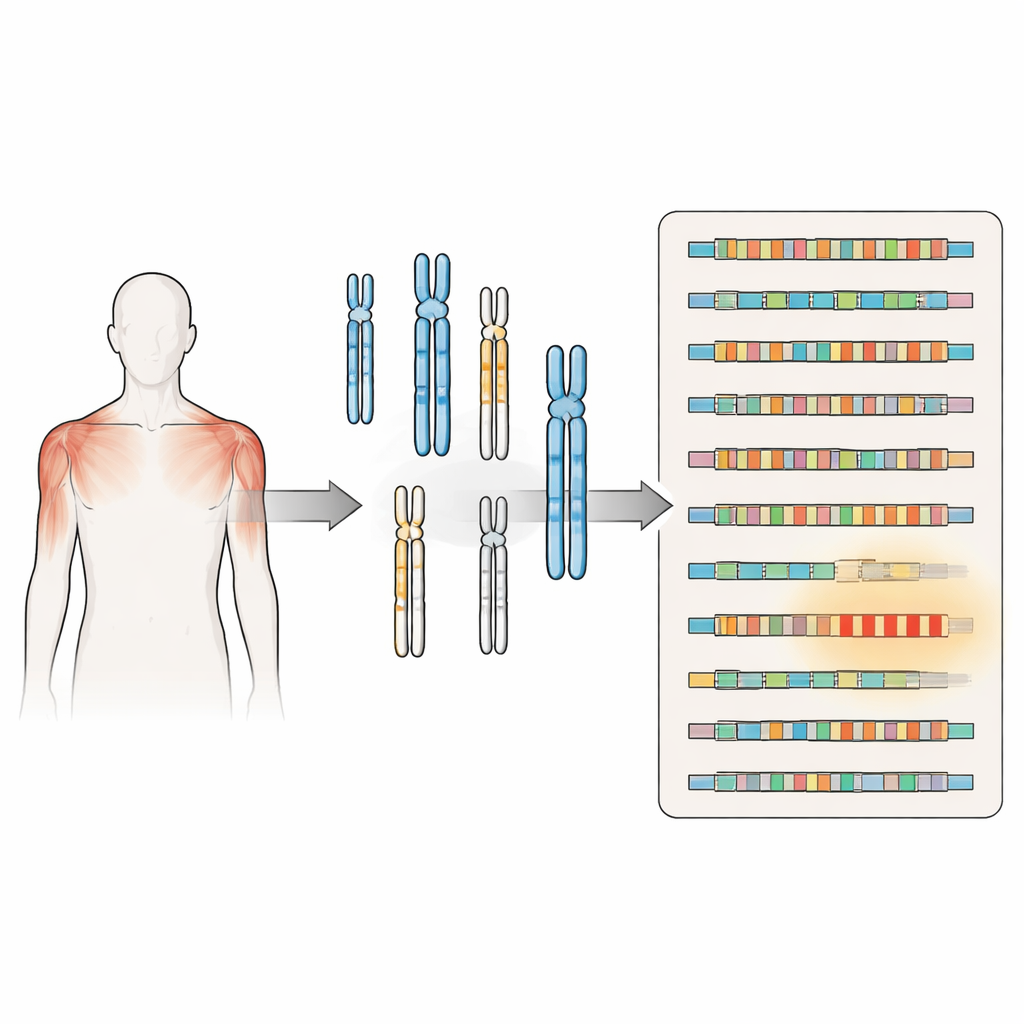
Uno sguardo ravvicinato a un disturbo muscolare enigmatico
Da tempo la FSHD è associata all’accorciamento di una sequenza ripetuta di DNA chiamata D4Z4 vicino alla fine del cromosoma 4. Quando questa regione di ripetizione si riduce oltre una certa soglia e si trova su un particolare contesto genetico, permette la produzione di una proteina chiamata DUX4, che può danneggiare le cellule muscolari. Una seconda forma della malattia deriva da mutazioni in geni che normalmente mantengono questa regione compattata e silente, consentendo nuovamente l’espressione di DUX4. Entrambe le vie convergono sullo stesso problema: un gene che dovrebbe essere per lo più spento nel muscolo adulto diventa sporadicamente attivo, contribuendo alla debolezza e all’atrofia muscolare.
Ripetizioni nascoste in tutto il genoma
Le mappe del genoma umano precedenti erano incomplete, specialmente nelle regioni ricche di DNA ripetitivo alle estremità dei cromosomi e vicino ai centromeri. Utilizzando la nuova assemblaggio del genoma umano telomero-a-telomero, che colma queste lacune, gli autori hanno riesaminato l’intero genoma usando la sequenza D4Z4 del cromosoma 4 come modello di ricerca. Hanno scoperto cluster e copie isolate di ripetizioni simili a D4Z4 in almeno altre dieci coppie di cromosomi. Alcune di queste ripetizioni sono strutturalmente complete e si trovano accanto a segnali che potrebbero stabilizzare RNA simili a DUX4, suggerendo che potrebbero produrre proteine correlate o molecole RNA in determinate condizioni.
Quando i test di laboratorio vedono più di un luogo alla volta
La ricerca sulla FSHD e la diagnostica spesso si affidano a test che amplificano frammenti specifici di DNA o RNA con brevi sequenze primer, una strategia nota come PCR. Questi primer sono stati originariamente progettati con l’assunzione che le ripetizioni D4Z4 esistessero solo sui cromosomi 4 e 10. Combinando previsioni computazionali con esperimenti su cellule che portano singoli cromosomi umani, gli autori mostrano che molti set di primer ampiamente usati si legano non solo alla regione associata alla malattia sul cromosoma 4, ma anche a ripetizioni simili sparse nel genoma. I primer diretti all’esone principale di DUX4 o agli RNA lunghi non codificanti vicini amplificano frequentemente prodotti provenienti da diversi cromosomi contemporaneamente, rendendo impossibile sapere da dove provenga realmente un dato segnale.
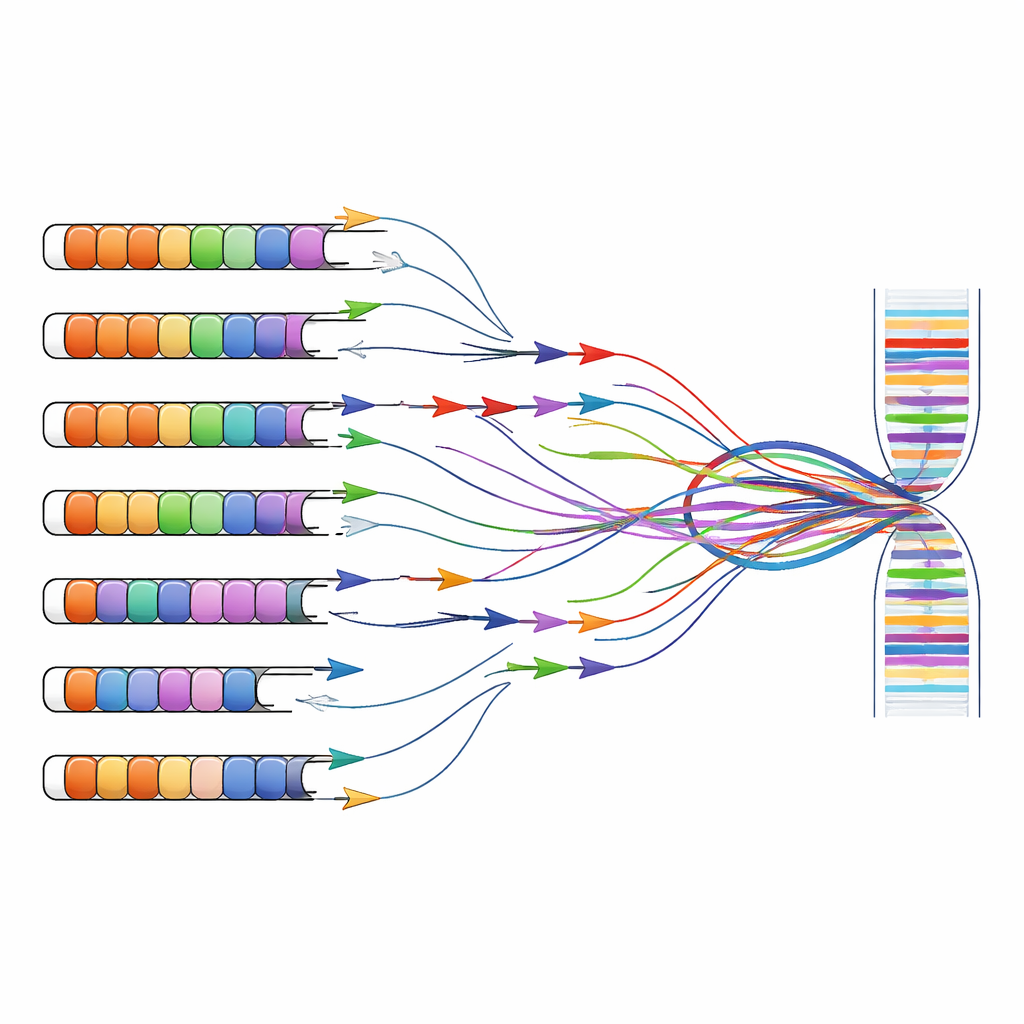
Riconsiderare gli strumenti diagnostici e di ricerca
Questo problema multi‑sito si estende oltre la ricerca di base fino alla clinica. Test più recenti che misurano la metilazione del DNA (un marchio chimico associato al silenziamento genico) o che utilizzano il sequenziamento a letture corte spesso aggregano segnali provenienti da molte ripetizioni quasi identiche. Di conseguenza, le misurazioni di “metilazione D4Z4” o di “trascritti DUX4” in dataset pubblici possono riflettere in realtà una miscela di contributi dal cromosoma 4, dal cromosoma 10 e da altri siti. Gli autori sostengono che per collegare correttamente le variazioni genetiche ai sintomi, gli scienziati devono ora adottare metodi consapevoli delle ripetizioni che distinguano locus individuali — per esempio il sequenziamento a letture lunghe che può attraversare interi blocchi di ripetizioni e catturarne i modelli di metilazione e i prodotti RNA nella loro interezza.
Cosa significa per i pazienti e le terapie future
Lo studio non ribalta il ruolo centrale della regione D4Z4 accorciata sul cromosoma 4 nella FSHD, ma mostra che questa regione vive in un quartiere affollato di sequenze simili. Segnali un tempo ritenuti la prova di attività nel locus della malattia possono in realtà provenire in parte dai suoi cugini genomici. Per i pazienti, ciò significa che gli strumenti diagnostici più affidabili saranno quelli che risolvono fisicamente quale cromosoma e quale matrice di ripetizioni sono coinvolti, piuttosto che fare affidamento esclusivamente su misure indirette. Per i ricercatori e gli sviluppatori di farmaci, evidenzia la necessità di design altamente specifici che evitino di colpire accidentalmente ripetizioni innocue altrove nel genoma. Nell’era telomero-a-telomero, comprendere e trattare la FSHD dipenderà dal vedere l’intero paesaggio delle ripetizioni, non solo un singolo punto di riferimento.
Citazione: Salsi, V., Losi, F., Pini, S. et al. Rethinking genomics of facioscapulohumeral muscular dystrophy in the telomere-to-telomere era: pitfalls in the hidden landscape of D4Z4 repeats. Eur J Hum Genet 34, 357–367 (2026). https://doi.org/10.1038/s41431-025-02000-x
Parole chiave: distrofia muscolare facioscapolomerale, ripetizioni D4Z4, DUX4, genoma telomero-a-telomero, diagnostica genetica