Clear Sky Science · it
Chaperon artificiali: dai progetti convenzionali ai sistemi intelligenti
Aiutare le molecole a piegarsi nel modo giusto
All'interno di ogni cellula vivente, lunghe catene di proteine e materiale genetico devono piegarsi e torcersi in forme precise per funzionare correttamente. Quando si ripiegano in modo errato, possono aggregarsi, perdere la loro funzione e persino scatenare malattie come quelle neurodegenerative. La natura si affida a molecole “chaperon” per mantenere l'ordine in questo affollato mondo microscopico, ma questi aiutanti naturali sono costosi, fragili e difficili da impiegare al di fuori delle cellule. Questo articolo esplora come gli scienziati stiano oggi costruendo chaperon artificiali—aiutanti ingegnerizzati che possono indurre le molecole smarrite a ritrovare la forma corretta e che possono anche essere attivati e disattivati come strumenti intelligenti.
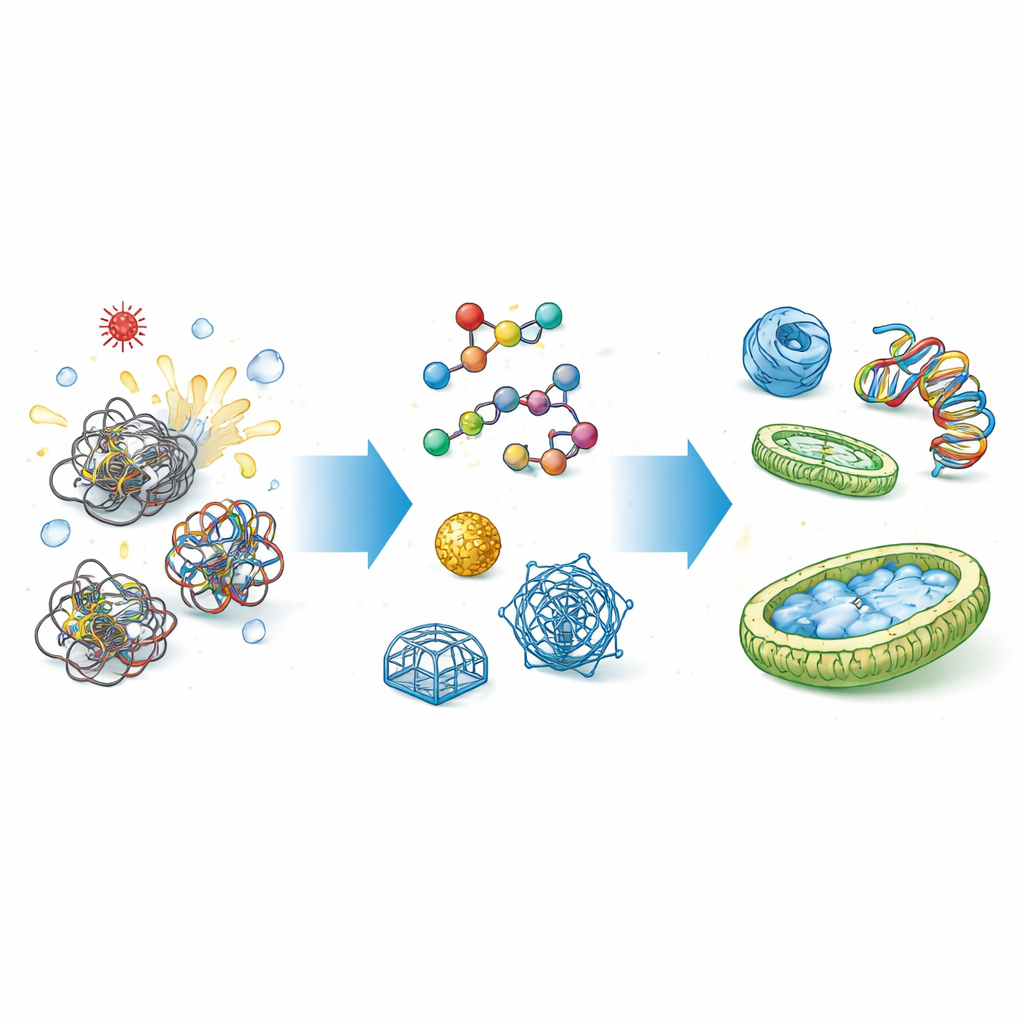
Perché le cellule hanno bisogno di aiutanti per il ripiegamento
Proteine e acidi nucleici (come DNA e RNA) non nascono pronti: devono ripiegarsi in complesse strutture tridimensionali. Il percorso verso queste forme è pieno di insidie, dove le catene possono bloccarsi o aderire tra loro. I chaperon naturali, come le proteine da shock termico, afferrano queste catene flosce, schermano le loro parti appiccicose e forniscono uno spazio protetto perché si ripieghino correttamente. Ruoli analoghi si osservano per gli acidi nucleici, dove i chaperon aiutano a districare nodi e riorganizzare gli appaiamenti delle basi. Quando questo controllo viene meno, il risultato può essere perdita di funzione, aggregati tossici, malattia e costosi insuccessi nella produzione industriale di proteine.
Dai semplici chimici ai polimeri su misura
I primi chaperon artificiali erano sostanze relativamente semplici che modificano l'ambiente in cui le molecole si trovano. Alcuni solventi e detergenti possono nascondere regioni appiccicose delle proteine, prevenire l'aggregazione e dare loro una seconda opportunità per ripiegarsi. Alcuni piccoli acidi grassi, per esempio, aiutano il collagene mutato a ripiegarsi più correttamente e riducono lo stress nelle cellule colpite da malattie ereditarie. Ma questi aiuti chimici di solito devono essere somministrati a dosi elevate, sono difficili da adattare a bersagli specifici e possono disturbare altri componenti in miscele complesse. Per ottenere maggior controllo, i ricercatori si sono rivolti a polimeri più grandi e su misura—catene flessibili che possono essere decorate con ramificazioni cariche o idrofile per accogliere DNA, RNA e proteine in modo più selettivo.
Kit di strumenti: polimeri e nanogel
I polimeri progettati possono legarsi ai dorsali caricati del DNA o alle patch esposte delle proteine, appianando il paesaggio energetico in modo che queste molecole trovino le loro forme preferite più rapidamente e con maggiore affidabilità. Per gli acidi nucleici, i polimeri cationici (carichi positivamente) possono neutralizzare la repulsione tra filamenti, accelerando l'appaiamento delle basi, lo scambio di filamenti e la formazione di strutture esotiche utilizzate nel calcolo a DNA e nei biosensori. Per le proteine, polimeri come anelli di polietilenglicole sagomati o polianioni sintetici possono superare alcuni chaperon naturali nel prevenire l'aggregazione indotta dal calore. Altri sistemi accoppiano polimeri chaperon flessibili con brevi peptidi per rimodellare membrane simili a quelle cellulari in nanoschede piatte o vescicole, creando piattaforme bidimensionali reversibili per il trasporto di carico e l'ingegneria tissutale.

Costruire chaperon intelligenti e commutabili
Oltre a trattenere e rilasciare i loro clienti, i chaperon artificiali moderni possono ora rispondere all'ambiente. I ricercatori hanno costruito nanogel, nanoparticelle e reti polimeriche la cui presa sulle proteine si stringe o si allenta con cambiamenti di acidità, temperatura, luce o di sostanze chimiche specifiche come il glucosio. Per esempio, alcuni micelli diventano più idrofobici a pH leggermente acido, imitando i chaperon naturali catturando le proteine minacciate e poi rilasciandole quando il pH torna a cambiare. I polimeri termoresponsivi collassano o si espandono oltre una soglia, permettendo loro di sequestrare proteine danneggiate a una temperatura e rilasciare quelle ripiegate a un'altra. Gruppi fotosensibili possono essere usati come interruttori molecolari, accendendo o spegnendo vie di assemblaggio del DNA con un lampo di luce, mentre particelle sensibili agli zuccheri possono proteggere un ormone terapeutico e poi rilasciarlo preferenzialmente quando la glicemia è alta.
Cosa significa per medicina e tecnologia
L'articolo conclude che i chaperon artificiali stanno evolvendo da semplici stabilizzatori chimici a “strumenti molecolari” altamente programmabili in grado di riconoscere, proteggere e rimodellare molti tipi di strutture biologiche su richiesta. Bilanciando con cura forze attrattive e repulsive e integrando sensibilità a segnali come pH, calore, luce o stress meccanico, questi sistemi possono piegare le molecole bersaglio nel luogo e nel momento giusti. A lungo termine, tali aiutanti intelligenti potrebbero rendere più efficiente la produzione industriale di proteine, affinare i biosensori, alimentare computer molecolari e offrire nuovi modi per affrontare malattie legate a proteine mal ripiegate—potenzialmente includendo condizioni come l'Alzheimer—imitando da vicino il controllo sottile che le cellule viventi già esercitano.
Citazione: Zhang, W., Maruyama, A. Artificial chaperones: from conventional designs to smart systems. NPG Asia Mater 18, 12 (2026). https://doi.org/10.1038/s41427-026-00640-z
Parole chiave: chaperon artificiali, ripiegamento delle proteine, polimeri intelligenti, nanomedicina, materiali reattivi a stimoli