Clear Sky Science · it
Superatomi molecolari: legami atomici naturali e non naturali tra superatomi
Mattoni minuscoli che si comportano come atomi
La maggior parte di noi impara che gli atomi sono i mattoni fondamentali della materia. Questo articolo di revisione mostra che, a scale molto piccole, gruppi di alcune dozzine di atomi metallici possono a loro volta comportarsi come “super‑atomi” e che questi superatomi possono unirsi per formare “molecole superatomiche”. Comprendendo e progettando questi insoliti mattoni, gli scienziati sperano di creare nuovi materiali con proprietà ottiche, elettroniche e catalitiche finemente tarate che le molecole ordinarie non possono offrire.
Aggregati che imitano singoli atomi
I superatomi sono agglomerati metalliche ultra‑piccoli—spesso costituiti da oro, argento o rame—i cui elettroni si dispongono in schemi ordinati a guscio, proprio come i gusci nei diagrammi di un atomo sui libri di testo. Quando i gusci sono completamente riempiti, a particolari “numeri magici” di elettroni, l’aggregato diventa particolarmente stabile. I chimici possono stabilizzare ulteriormente questi cluster avvolgendoli in molecole organiche dette ligandi, trasformandoli in nano‑oggetti precisi dalle dimensioni e forme ben definite. Molti di questi superatomi sono quasi sferici e la loro stabilità può essere spiegata con un modello semplice in cui gli elettroni liberi del metallo si muovono all’interno come in una goccia carica positivamente e omogenea.
Quando i superatomi si legano come molecole ordinarie
Alcuni cluster metallici non sono affatto sferici. Invece, somigliano a due o più superatomi fusi insieme, formando ciò che l’autore definisce molecole superatomiche. Per spiegare queste strutture, i ricercatori hanno sviluppato la teoria del “super valence bond”, che tratta ogni superatomo come un atomo gigante con i propri orbitali e descrive come questi orbitali si mescolano per creare orbitali molecolari superatomici condivisi. In molti casi queste combinazioni si comportano esattamente come legami chimici familiari. Per esempio, coppie di superatomi d’oro possono formare versioni superatomiche del legame presente nella molecola di fluoro, mentre fusioni più complesse danno analoghi della molecola di ossigeno con ordini di legame superiori o addirittura legami a tre centri ricordando l’ozono. Questi arrangiamenti generano ricchi schemi di legame—singoli, multipli e multicipi—che riecheggiano le regole di legame della chimica ordinaria, ma ora alla scala di cluster contenenti decine di atomi. 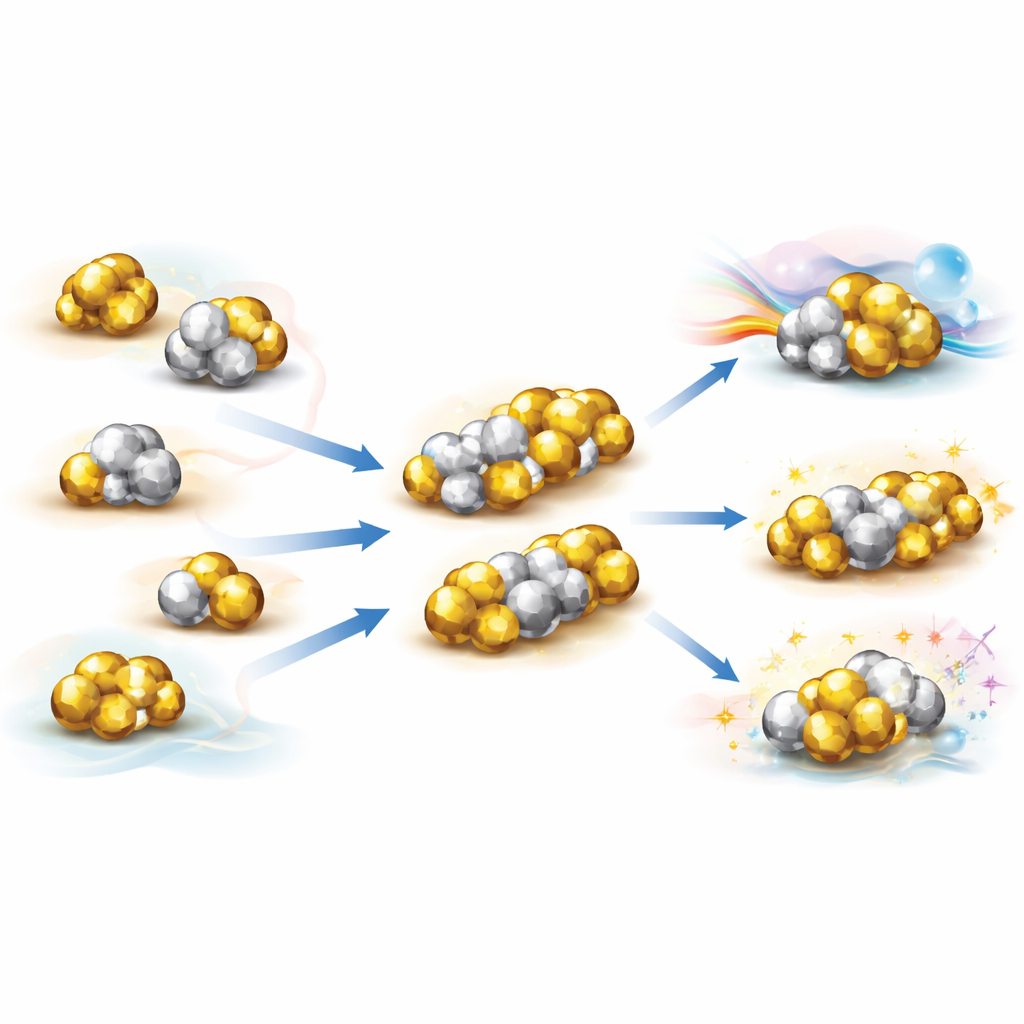
Legami strani con unità simili ai gas nobili
Le molecole superatomiche non si limitano a semplici analogie con i legami di tutti i giorni. La recensione evidenzia motivi di legame “non‑naturali” in cui superatomi con gusci elettronici chiusi—simili nello spirito ai gas nobili come elio o neon—si combinano in strutture più grandi anche se, secondo le regole di conteggio standard, non dovrebbe esistere alcun legame. In questi sistemi i superatomi possono condividere un singolo atomo metallico, disporsi borda‑a‑borda o collegarsi in assemblaggi ciclici e a forma di asta. Formalmente il loro ordine di legame è zero, eppure le interazioni tra le loro nuvole elettroniche e i ligandi circostanti stabilizzano l’insieme. Sorprendentemente, questi assemblaggi mostrano nuove bande di assorbimento e altre caratteristiche elettroniche assenti nei superatomi isolati, rivelando che interazioni orbitali sottili possono produrre risposte ottiche del tutto nuove.
Dai super‑anelli alle super‑catene
L’articolo esamina anche esempi più esotici in cui i superatomi formano anelli e catene con comportamento collettivo. Un caso notevole è un cluster d’oro costruito da cinque superatomi icosaedrici disposti in un anello; studi teorici suggeriscono che, con il numero di elettroni opportuno, questo “super‑anello” può diventare aromatico, distribuendo i suoi elettroni lungo il ciclo in modo direttamente analogo a molecole aromatiche classiche come il benzene o lo ione ciclopentadienile. Un’altra famiglia di strutture collega piccole unità d’oro di tre atomi in catene a forma di asta. Anche se le connessioni tra unità vicine sono deboli e in parte antibonding, il pattern ripetuto di orbitali interagenti si comporta come un “polimero superatomico”, dando luogo a un forte assorbimento nel vicino infrarosso e indicando potenziali applicazioni in dispositivi fototermici e optoelettronici. 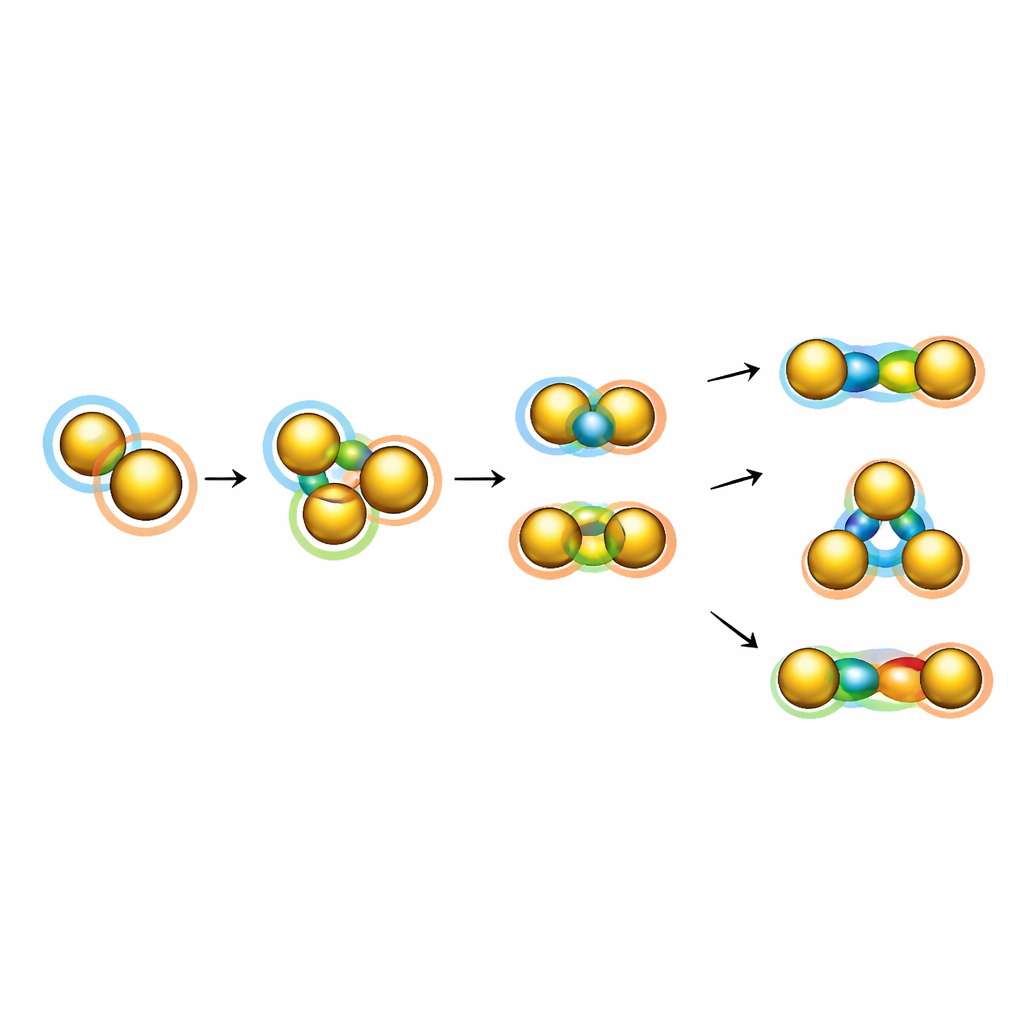
Perché queste piccole super‑molecole sono importanti
Nel complesso, la recensione sostiene che trattare i cluster metallici come unità atomiche in grado di legarsi in molecole superatomiche fornisce un potente linguaggio di progettazione per nuovi materiali. Scegliendo quante cariche elettroniche porta ciascun superatomo, come sono collegati e quali ligandi li circondano, gli scienziati possono ingegnerizzare non solo la stabilità ma anche l’assorbimento della luce, il trasporto di carica, il magnetismo e l’attività catalitica. I legami di tipo naturale offrono regole di progettazione familiari, mentre assemblaggi non‑naturali e debolmente legati sbloccano comportamenti senza un analogo diretto nella chimica ordinaria. Con il maturare di questa comprensione, le molecole superatomiche potrebbero diventare una cassetta degli attrezzi per costruire catalizzatori di nuova generazione, sistemi di raccolta della luce e componenti elettronici realizzati da cluster di atomi disposti con precisione.
Citazione: Isozaki, K. Superatomic molecules: natural and non-natural atom-like bonding between superatoms. NPG Asia Mater 18, 9 (2026). https://doi.org/10.1038/s41427-026-00636-9
Parole chiave: superatomi, nanocluster metallici, molecole superatomiche, nanomateriali, proprietà optoelettroniche