Clear Sky Science · it
Affrontare la cuprotosi: dal riprogrammamento metabolico allo sfruttamento terapeutico nel cancro
Quando un metallo utile si rivolta contro il cancro
Il rame è più noto come componente dei fili elettrici e dell’impiantistica idraulica, ma scorre silenzioso anche nelle nostre cellule, aiutando gli enzimi a produrre energia e a proteggerci dai danni. Questo articolo di recensione esplora una svolta sorprendente: nelle condizioni giuste, un eccesso di rame può spingere le cellule tumorali verso una forma particolare di morte. Comprendere questo processo — chiamato “cuprotosi” — potrebbe aprire nuove strade per trattare tumori che hanno eluso le terapie standard.
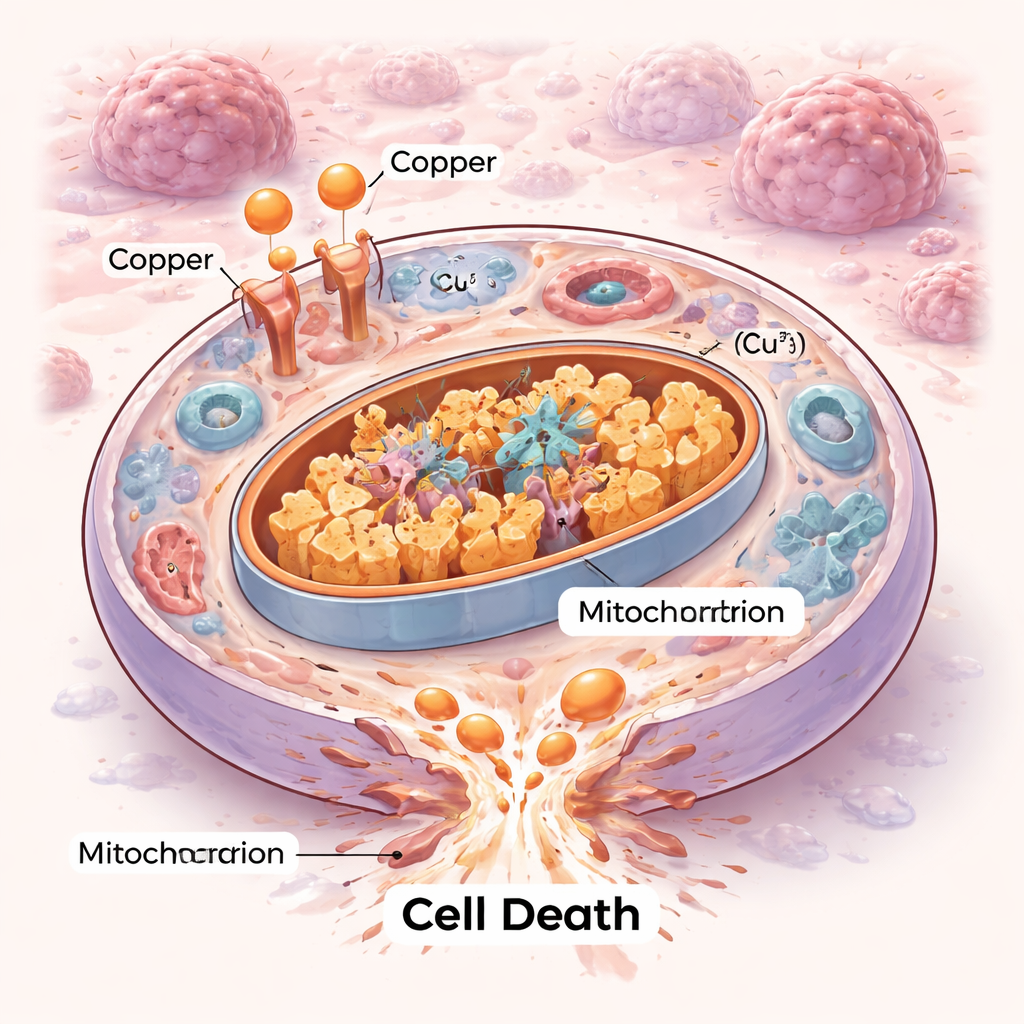
Un nuovo modo in cui le cellule possono morire
Le cellule non muoiono tutte allo stesso modo. Per decenni gli scienziati hanno mappato programmi ordinati di autodistruzione come l’apoptosi e forme più recenti come la ferroptosi. La cuprotosi aggiunge un capitolo nuovo. Qui, un eccesso di rame inonda le centrali energetiche della cellula — i mitocondri — e si lega a enzimi metabolici specifici che normalmente aiutano a bruciare combustibile. Questo legame causa l’aggregazione di tali enzimi e destabilizza piccoli componenti ferro‑zolfo di cui i mitocondri hanno bisogno per funzionare. Il risultato è una sorta di ingorgo interno e un cedimento meccanico che la cellula non riesce a riparare, terminando in morte per stress proteotossico piuttosto che attraverso le vie classiche di suicidio cellulare.
Come le cellule tumorali controllano rame ed energia
Poiché il rame è al tempo stesso essenziale e pericoloso, le cellule mantengono una rete logistica elaborata per muoverlo in sicurezza. Trasportatori dedicati portano il rame all’interno della cellula, proteine chaperone lo scortano verso i mitocondri e altre destinazioni, e molecole di stoccaggio come metallotioneine e glutatione neutralizzano gli eccessi. I tumori spesso riorganizzano questo sistema. Alcuni potenziano importatori o chaperone per soddisfare l’alto fabbisogno energetico; altri aumentano esportatori o proteine di stoccaggio per evitare il sovraccarico di rame. Allo stesso tempo, molti tumori spostano il loro metabolismo — alternando tra la combustione di zuccheri in superficie e una più profonda respirazione mitocondriale. La recensione spiega che la cuprotosi colpisce con maggiore forza le cellule che dipendono ancora pesantemente dai mitocondri, rendendo i tumori con questo profilo metabolico particolarmente vulnerabili.
Interruttori principali che modulano la sensibilità al rame
Grandi «decisori» cellulari influenzano se la cuprotosi può verificarsi. Il soppressore tumorale p53, per esempio, tende a spostare le cellule lontano dalla fermentazione zuccherina rapida verso un uso più ordinato del carburante mitocondriale. Facendo ciò e alterando la gestione degli enzimi leganti il rame, p53 può rendere i tumori più suscettibili alla morte indotta dal rame — mentre le forme mutate di p53 spesso fanno l’opposto. Al contrario, il fattore di ipossia HIF‑1α, attivato nei nuclei tumorali poveri di ossigeno, aiuta le cellule a sfuggire alla cuprotosi riducendo enzimi mitocondriali chiave e potenziando scudi leganti il rame. Altri percorsi, come Wnt/β‑catenina e AKT, promuovono la resistenza stimolando l’esportazione del rame o modificando chimicamente proteine cruciali in modo che non rispondano più al sovraccarico di rame. Insieme, queste reti agiscono come termostati, alzando o abbassando la sensibilità di un tumore ai trattamenti a base di rame.
Il rame, il sistema immunitario e somministrazioni di farmaci più intelligenti
Il ruolo del rame non si limita a uccidere direttamente le cellule tumorali; plasma anche il paesaggio immunitario intorno ai tumori. Uno stress controllato da rame può rendere le cellule cancerose morenti più «visibili», rilasciando segnali di pericolo che reclutano e attivano linfociti T, cellule dendritiche e macrofagi. Il rame può anche influenzare i livelli di checkpoint immunitari come PD‑L1, che i tumori usano per spegnere i linfociti T antitumorali, suggerendo opportunità di combinare farmaci che mirano il rame con le immunoterapie moderne. Poiché il rame libero può danneggiare i tessuti sani, i ricercatori stanno sviluppando strumenti di precisione — ionofori a piccole molecole che trasportano il rame selettivamente nelle cellule tumorali, e piattaforme di nanomedicina che incapsulano rame o farmaci attivati dal rame dentro particelle mirate o idrogeli. Queste tecnologie mirano ad aumentare il rame a livelli letali all’interno dei tumori mantenendo il resto dell’organismo in un range sicuro.
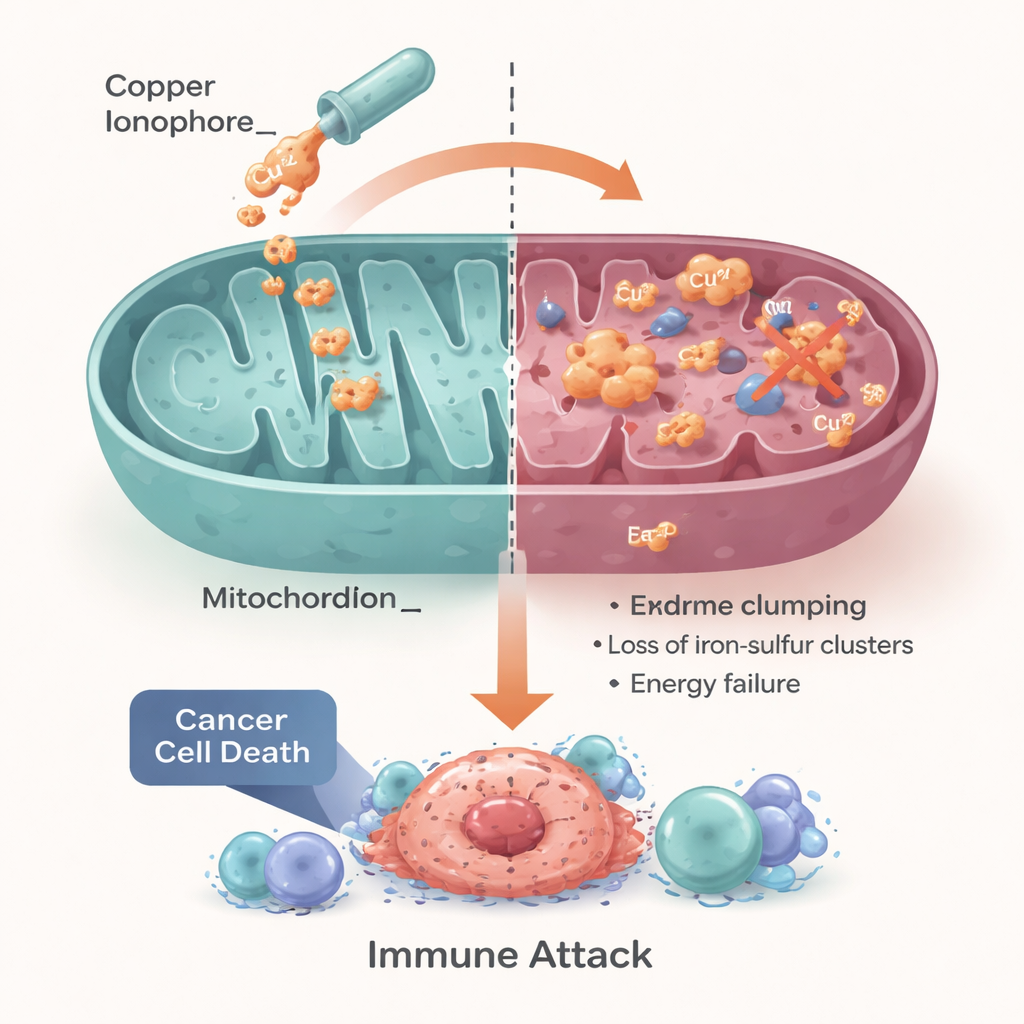
Trasformare una debolezza cellulare in una cura
Gli autori concludono che la cuprotosi trasforma un bisogno cellulare di base — una gestione attenta di rame ed energia — in un possibile tallone d’Achille per il cancro. I tumori con una gestione del rame alterata o una dipendenza eccessiva dal metabolismo mitocondriale possono essere particolarmente sensibili a strategie basate sul rame, inclusi farmaci riproposti come disulfiram ed elesclomol, oltre a nanoparticelle di nuova generazione. Tuttavia, sottolineano che il successo dipenderà dall’abbinare i pazienti giusti all’approccio giusto, usando biomarcatori che riflettano i trasportatori del rame, l’attività mitocondriale e lo stato immunitario e di ossigenazione del tumore. Se questi ostacoli saranno superati, sfruttare la cuprotosi potrebbe offrire agli oncologi una nuova leva potenziata dal metallo per trattare tumori che oggi hanno poche buone opzioni.
Citazione: Hao, Q., Gan, Y. & Zhou, X. Tackling cuproptosis: from metabolic rewiring to therapeutic exploitation in cancer. Cell Mol Immunol 23, 239–260 (2026). https://doi.org/10.1038/s41423-026-01387-x
Parole chiave: cuprotosi, metabolismo del rame, terapia del cancro, metabolismo tumorale, immunoterapia oncologica