Clear Sky Science · it
Forza magneto‑meccanica dinamica nei lisosomi induce una ripolarizzazione duratura dei macrofagi per l’immunità antitumorale
Usare forze delicate per risvegliare il sistema immunitario
Il cancro spesso sopravvive inducendo il sistema difensivo del corpo a “dormire”. Questo studio esplora un modo inatteso per risvegliarlo: tirando fisicamente piccole compartimentazioni all’interno delle cellule immunitarie mediante nanoparticelle attivate magneticamente. Invece di fare affidamento solo sui farmaci, i ricercatori usano forze meccaniche calibrate all’interno delle cellule per riprogrammare i macrofagi in combattenti anti‑tumorali di lunga durata.
Perché i tumori solidi sono difficili da trattare
Le immunoterapie oncologiche moderne, come gli anticorpi che bloccano i checkpoint e le cellule immunitarie ingegnerizzate, hanno trasformato il trattamento di alcuni tumori ematologici. Tuttavia, per molti pazienti con tumori solidi come il cancro polmonare, questi approcci aiutano solo una minoranza. Una ragione importante è il microambiente tumorale. I tumori sono circondati da una nicchia protettiva fatta di cellule e segnali che sopprimono l’immunità. I macrofagi, che possono o attaccare i tumori (stato simile a M1) o sostenerli (stato simile a M2), vengono spesso spinti nella modalità M2 che favorisce il tumore. Ribaltare questa programmazione “scorretta” in modo duraturo è stato difficile usando soltanto farmaci biochimici convenzionali.
Trasformare nanoparticelle in piccoli motori meccanici
Il gruppo ha progettato nanomotori magnetici—particelle a scala nanometrica di ossido di ferro drogato con zinco e rivestite da un polimero caricato positivamente—che vengono facilmente ingerite dai macrofagi e si concentrano nei lisosomi, gli hub di riciclo e segnalazione della cellula. Una volta all’interno, un campo magnetico rotante esterno fa allineare queste particelle in catene a forma di asta che ruotano, mescolando il fluido denso all’interno dei lisosomi e creando piccoli vortici. Simulazioni al computer ed esperimenti su membrane modello hanno mostrato che, calibrando con cura la frequenza di rotazione, lo sforzo di taglio sulla membrana lisosomiale può essere portato a un punto ottimale: sufficientemente forte da rendere la membrana temporaneamente permeabile, ma non così intenso da distruggerla in modo permanente.
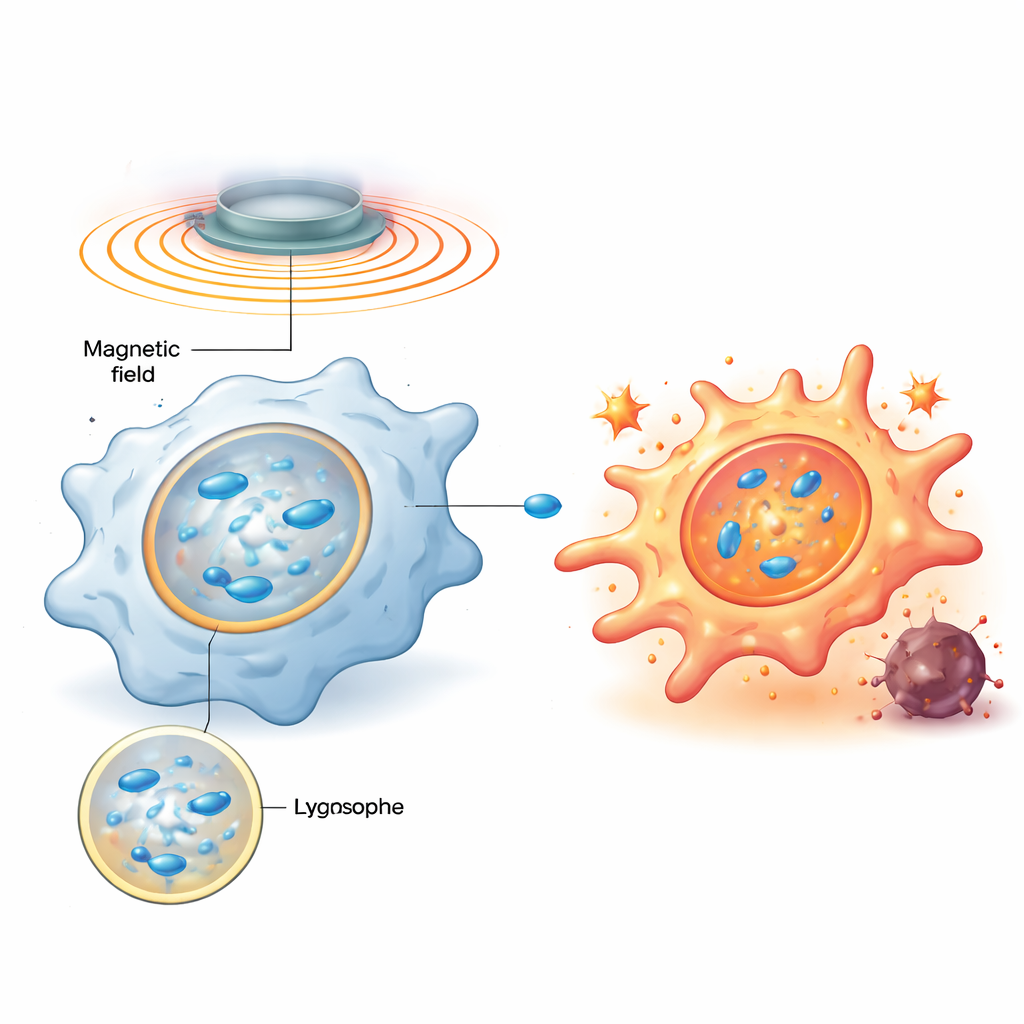
Una spinta meccanica innesca un allarme biochimico
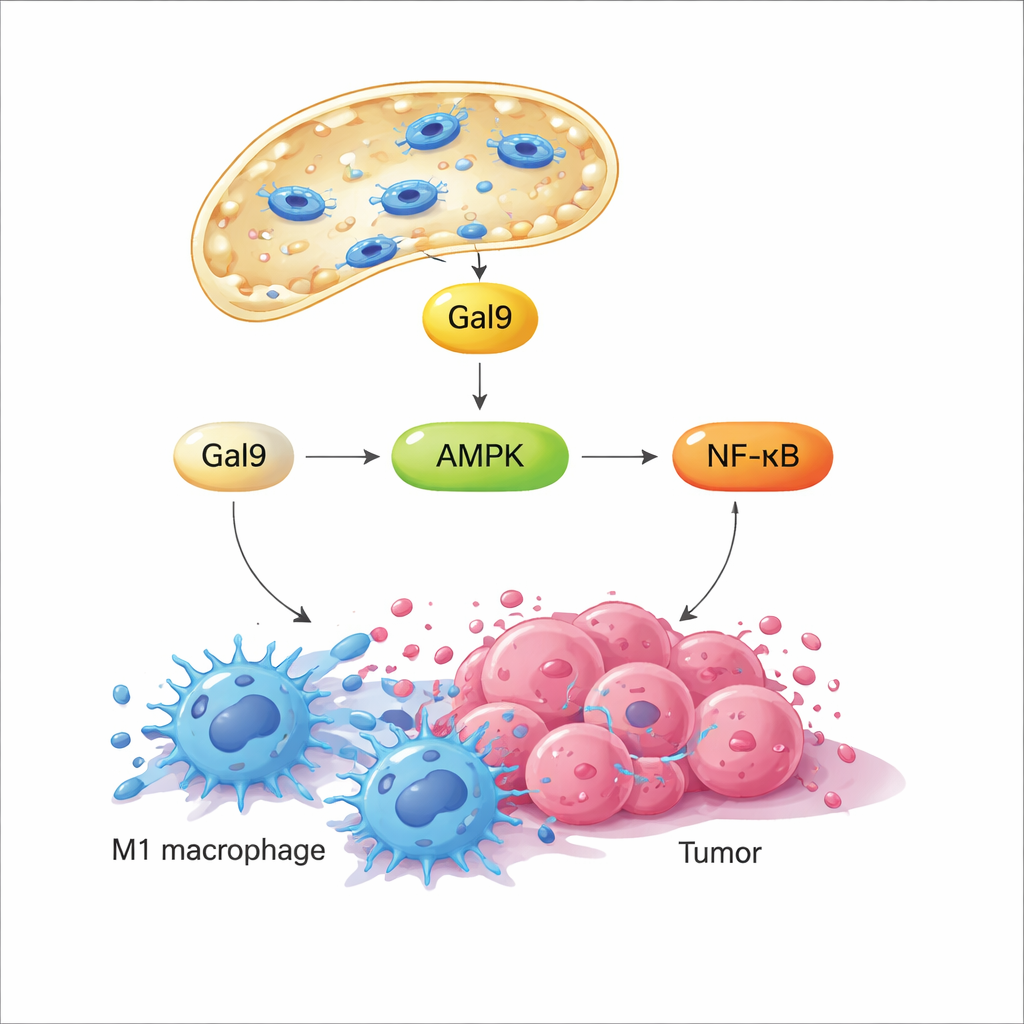
Quando la membrana lisosomiale è brevemente perturbata, una proteina legante zuccheri chiamata galectina‑9 corre verso i punti danneggiati, agendo come sensore di questo stress meccanico. Lo studio dimostra che ciò attiva a sua volta un enzima chiave sensibile all’energia, AMPK, che poi potenzia la via di segnalazione NF‑κB—ben nota per guidare risposte infiammatorie e antimicrobiche. Insieme, questi segnali riscrivono il metabolismo dei macrofagi, spostandolo da uno stato tranquillo ed efficiente dal punto di vista energetico verso una glicolisi rapida, associata a un comportamento ostile simile a M1. Importante: quando il campo magnetico viene spento, il lisosoma si ripara e la segnalazione si attenua; quando il campo viene riacceso in seguito, la stessa via si riattiva. Questo ciclo programmabile on‑off consente ai ricercatori di “sollecitare” ripetutamente lo stesso interruttore meccanico senza uccidere le cellule.
Rieducare i macrofagi a combattere i tumori
In colture cellulari, questa permeabilizzazione lisosomiale indotta magneticamente—chiamata MagLMP—ha convertito macrofagi che erano stati spinti in uno stato simile a M2 di supporto tumorale in uno stato pro‑infiammatorio simile a M1. Queste cellule riprogrammate hanno prodotto più citochine infiammatorie e hanno mantenuto il profilo simile a M1 per giorni, anche in terreni di coltura derivati da tumore che normalmente le indirizzano verso M2. In modelli murini di tumore, l’incorporazione di nanomotori magnetici nei tumori e l’applicazione di cicli giornalieri del campo rotante hanno rallentato la crescita di vari tipi di cancro. Quando i macrofagi sono stati sperimentalmente depletati, il beneficio è in gran parte scomparso, dimostrando che queste cellule sono centrali per l’effetto del trattamento. Il sequenziamento dell’RNA a singola cellula del tessuto tumorale ha mostrato inoltre che MagLMP ha aumentato la proporzione di macrofagi di tipo M1, potenziato neutrofili antitumorali e cellule effettrici CD8, e upregolato geni correlati a NF‑κB e alla glicolisi all’interno dei macrofagi.
Dal controllo locale a una terapia sistemica
I ricercatori si sono poi chiesti se questo approccio potesse funzionare come un trattamento più simile al mondo reale, somministrato attraverso il flusso sanguigno. Hanno iniettato i nanomotori per via endovenosa e usato un semplice magnete esterno per concentrarli all’interno dei tumori, dimostrando un’efficiente captazione da parte dei macrofagi nel letto tumorale. Il trattamento MagLMP successivo ha nuovamente spostato i macrofagi verso lo stato simile a M1 e ha contenuto la crescita tumorale. In un modello murino di cancro polmonare in fase iniziale che cresceva all’interno del polmone stesso, la combinazione di guida magnetica con cicli di MagLMP ha portato a una sopravvivenza notevolmente prolungata: circa un terzo dei topi trattati è vissuto più di 300 giorni, rispetto a sole settimane negli animali di controllo. Combinare MagLMP con un inibitore del checkpoint PD‑1 ha ulteriormente migliorato il controllo del tumore in modelli difficili da trattare.
Un nuovo modo di controllare l’immunità dall’interno
Questo lavoro mostra che forze meccaniche minuscole e ben controllate all’interno di un organello specifico possono essere sfruttate per orientare il comportamento immunitario in animali viventi. Sollecitando ripetutamente e in modo reversibile i lisosomi, MagLMP attiva un asse galectina‑9–AMPK–NF‑κB che riprogramma i macrofagi in combattenti tumorali duraturi senza danneggiare ampiamente le cellule. Per i non specialisti, l’idea chiave è che segnali fisici—erogati da nanomotori mossi magneticamente—possono funzionare come una manopola sul sistema immunitario, offrendo una nuova classe di strumenti per integrare i farmaci nelle future immunoterapie antitumorali.
Citazione: Li, Y., Zheng, M., Zhu, Z. et al. Dynamic magneto-mechanical force in lysosomes induces durable macrophage repolarization for antitumor immunity. Cell Res 36, 197–218 (2026). https://doi.org/10.1038/s41422-025-01217-1
Parole chiave: immunoterapia del cancro, riprogrammazione dei macrofagi, nanoparticelle magnetiche, meccanotrasduzione, segnalazione lisosomiale