Clear Sky Science · it
Attivazione meccanica transitoria del canale Piezo1 facilita l’espansione ex vivo delle cellule staminali ematopoietiche
Produrre più cellule staminali del sangue che salvano vite
I trapianti di midollo osseo possono curare alcuni tumori del sangue e malattie ereditarie, ma i medici sono spesso limitati dalla scarsità di vere cellule staminali ematopoietiche ottenibili da un donatore. Questo studio rivela un modo sorprendente per far crescere queste rare cellule fuori dal corpo toccandole delicatamente con piccole sfere di plastica che stimolano un sensore meccanico sulla loro superficie. Il lavoro suggerisce una nuova strada, potenzialmente più sicura, per generare un numero sufficiente di cellule staminali in modo che più pazienti possano beneficiare del trapianto.
Perché è così difficile far crescere le cellule staminali del sangue
Le cellule staminali del sangue risiedono in profondità nelle ossa e forniscono silenziosamente per tutta la vita tutte le nostre cellule rosse, bianche e le piastrine. Trapiantare queste cellule può ripristinare un sistema ematopoietico danneggiato, come nel trattamento della leucemia, ma solo se sono disponibili cellule staminali sane in numero sufficiente e mantengono la piena funzionalità. I tentativi di espanderle in coltura hanno spesso dato risultati insoddisfacenti: le cellule tendono a interrompere l’auto-rinnovamento o a perdere la capacità a lungo termine di ricostruire il sistema ematopoietico. La maggior parte dei metodi attuali si basa su mix di fattori di crescita e modifiche genetiche, ma non ricrea completamente il complesso ambiente fisico del midollo osseo, dove le staminali percepiscono continuamente spinte, trazioni e pressioni.
Un interruttore meccanico nascosto sulle cellule staminali
I ricercatori si sono concentrati su una proteina chiamata Piezo1, un minuscolo canale a valvola nella membrana cellulare che si apre quando la membrana viene piegata o stirata, permettendo agli ioni calcio di entrare e avviare segnali interni. Esaminando numerosi tipi di cellule del sangue, hanno scoperto che Piezo1 è particolarmente abbondante nelle vere cellule staminali ematopoietiche. Quando hanno eliminato Piezo1 geneticamente o lo hanno bloccato con un farmaco, le staminali coltivate in vitro non riuscivano più ad espandersi bene né a ripopolare il sangue dei topi dopo il trapianto. Interessante, la stimolazione continua di Piezo1 con attivatori chimici risultava anch’essa dannosa: le cellule accumulavano calcio in eccesso, producevano molecole reattive nocive e avevano minore capacità di attecchire. Questi risultati suggerivano che le staminali necessitano di attivazioni meccaniche brevi e ben temporizzate di Piezo1, non di una sollecitazione chimica costante.
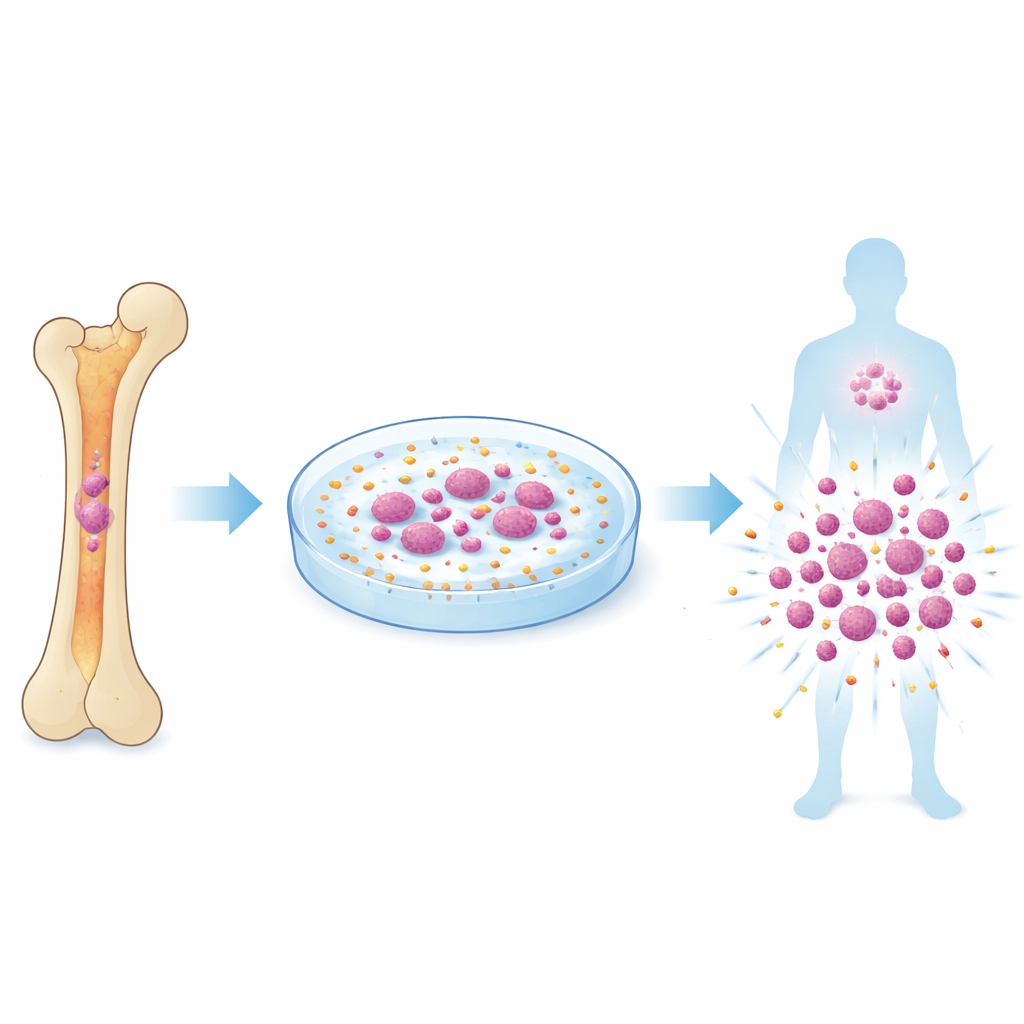
Sfruttare piccole sfere per stimolare il sensore
Per fornire la giusta sollecitazione meccanica, il gruppo ha utilizzato sfere polimeriche microscopiche, in pratica piccole perle di plastica lisce, che potevano urtare le staminali in coltura. Hanno testato sfere di diverse dimensioni e rigidità e scoperto che sfere di polistirene da 500 nanometri—chiamate PS500—erano particolarmente efficaci. Quando le cellule del midollo osseo di topo venivano coltivate insieme a queste sfere, il numero di cellule staminali aumentava notevolmente e queste cellule mantennero una forte capacità di ripopolamento a lungo termine in trapianti seriali attraverso più generazioni di topi. Immagini accurate e misure meccaniche mostrarono che le sfere incidevano ripetutamente la membrana cellulare con forze minime, sufficienti ad aprire i canali Piezo1 in brevi raffiche senza sovraccaricare le cellule.
Dal tocco meccanico ai segnali di crescita
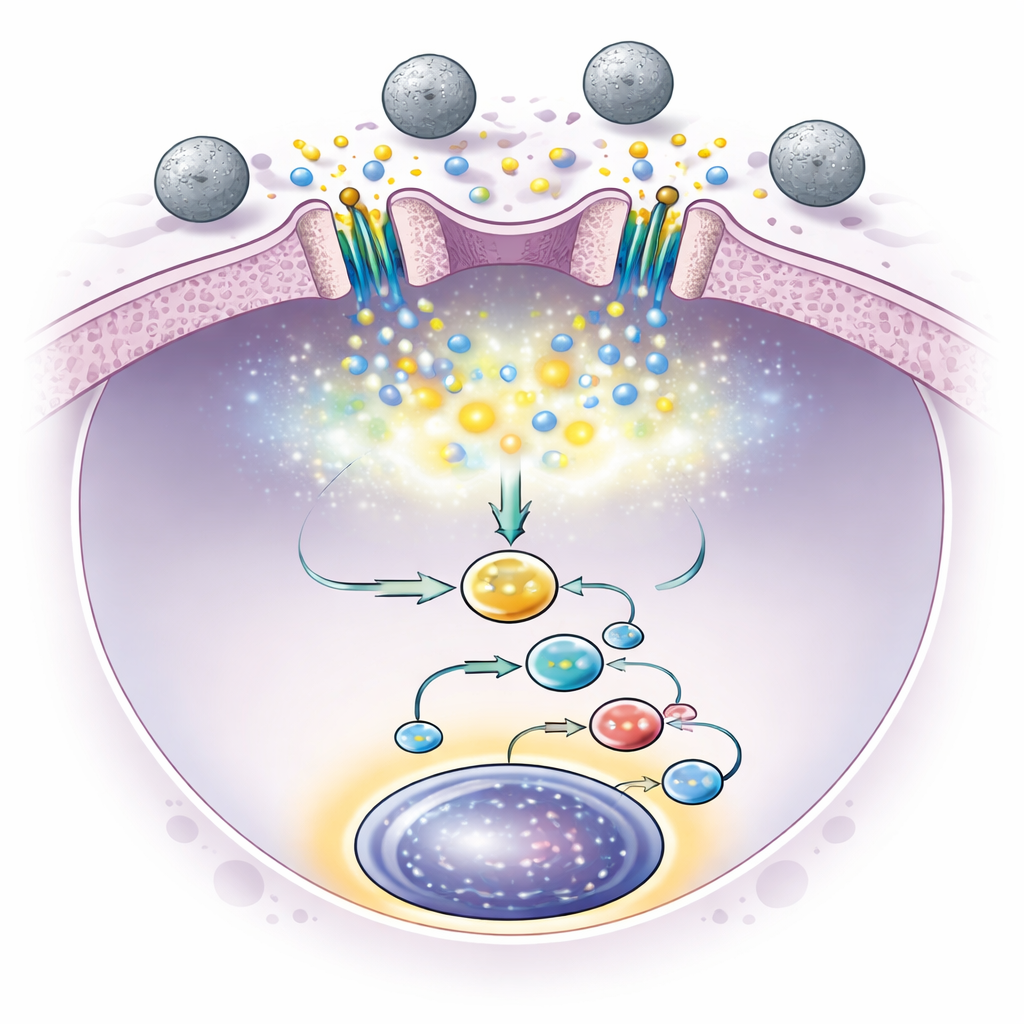
L’apertura transitoria dei canali Piezo1 innescava piccoli impulsi di ingresso di calcio nelle cellule staminali. Ciò, a sua volta, attivava vie intracellulari che portavano le cellule a produrre certe proteine segnalatrici, in particolare il fattore di crescita interleuchina-6. L’interleuchina-6 poi agiva sulle stesse staminali e attivava una proteina chiamata Stat3 nei loro nuclei, nota per sostenere la sopravvivenza e l’auto-rinnovamento delle staminali. Quando i ricercatori bloccarono questa via Stat3, l’effetto benefico delle sfere scomparve, confermando che questa catena di eventi—tocco meccanico, impulso di calcio, rilascio di interleuchina-6 e attivazione di Stat3—era cruciale per l’espansione. Importante, dopo un breve periodo di esposizione alle sfere, la segnalazione rimaneva attiva e il numero di staminali continuava ad aumentare, sottolineando che non era necessaria una stimolazione costante.
Prospettive per i trapianti umani
Il team ha poi applicato lo stesso approccio a cellule staminali del sangue umano raccolte dal sangue del cordone ombelicale, una fonte comune ma spesso limitata per i trapianti. Con le sfere PS500, queste cellule umane si espandevano diverse volte più rispetto ai migliori metodi basati su piccole molecole da soli, pur conservando la capacità di ripopolare permanentemente il sangue di topi immunodeficienti. Studi di sicurezza nei topi hanno indicato che le sfere non penetrano nelle cellule staminali, possono essere rimosse efficacemente con centrifugazione o filtrazione semplice e non causano danni evidenti agli organi o anomalie del sangue alle dosi testate. Ciò pone il sistema a base di sfere come una tecnologia pratica e potenzialmente scalabile per le banche del sangue e i centri trapianti.
Cosa potrebbe significare per i pazienti
In sostanza, lo studio dimostra che un segnale meccanico delicato—fornito da sfere nanoscalari in movimento—può indurre le cellule staminali del sangue a moltiplicarsi preservandone la potenza, attivando brevemente un sensore di pressione intrinseco invece di sovraccaricarlo. Se tradotto in clinica, questo approccio potrebbe rendere più facile generare un numero sufficiente di cellule staminali di alta qualità a partire da una piccola unità di sangue del cordone o da un donatore parziale, ampliando l’accesso a trapianti che curano molte più persone. Evidenzia inoltre come prestare attenzione non solo alla “zuppa” chimica attorno alle cellule ma anche alle sensazioni fisiche che sperimentano possa sbloccare nuovi modi per controllare il destino cellulare.
Citazione: Wang, Q., Zeng, X., Yang, H. et al. Transient mechanical activation of the Piezo1 channel facilitates ex vivo expansion of hematopoietic stem cells. Cell Res 36, 272–285 (2026). https://doi.org/10.1038/s41422-025-01209-1
Parole chiave: cellule staminali ematopoietiche, canali ionici meccanosensibili, Piezo1, micro sfere di polistirene, trapianto di cellule staminali