Clear Sky Science · it
La bilirubina attiva direttamente RIPK3 per indurre necroptosi non classica
Quando una molecola utile diventa dannosa
La bilirubina è meglio nota come il pigmento giallo responsabile dell’ittero neonatale e del tipico colore dei lividi. A bassi livelli contribuisce anzi a proteggere le nostre cellule dai danni. Ma quando la bilirubina si accumula nell’organismo e penetra nel cervello, può provocare danni duraturi, specialmente nei neonati e nelle persone con grave malattia epatica. Questo studio svela un modo sorprendente in cui l’eccesso di bilirubina può attivare direttamente un “interruttore mortale” molecolare all’interno delle cellule cerebrali, scatenando una forma distruttiva di morte cellulare e offrendo un nuovo bersaglio per terapie future.
Da pigmento ematico a minaccia per il cervello
La bilirubina si forma quando il nostro organismo ricicla i globuli rossi. Normalmente il fegato la modifica ed elimina, mantenendone i livelli bassi e relativamente sicuri. In certe condizioni — come l’ittero neonatale, infezioni gravi o insufficienza epatica — la bilirubina non processata può accumularsi. Poiché si scioglie facilmente nei grassi, questa forma “libera” può attraversare la barriera emato-encefalica, soprattutto quando tale barriera è indebolita da malattia o infiammazione. Una volta entrata nel cervello, la bilirubina è nota per essere tossica, ma i passaggi esatti con cui danneggia i neuroni sono rimasti poco chiari.
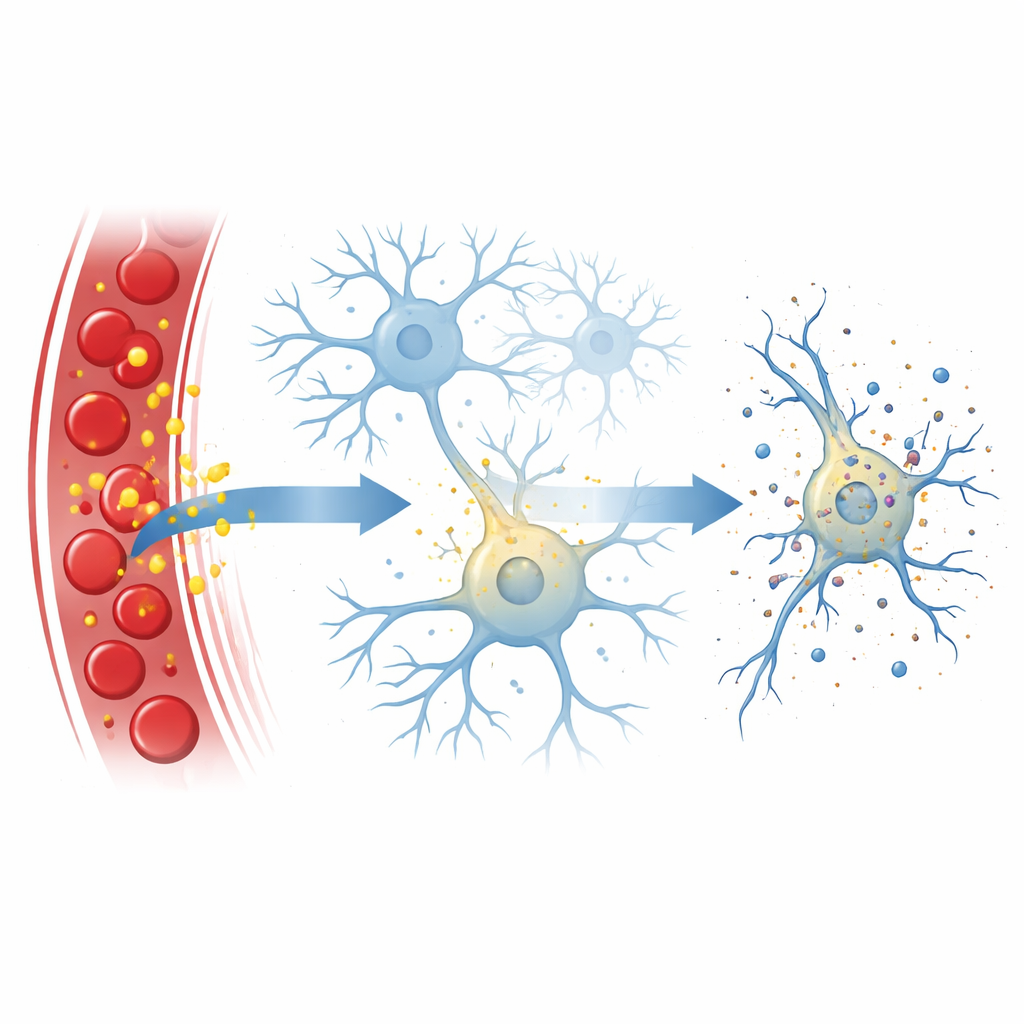
Un’esplosione cellulare controllata
I ricercatori si sono concentrati sulla necroptosi, una forma regolata di morte cellulare che assomiglia a una piccola esplosione: la cellula si gonfia, la membrana esterna si rompe e il contenuto fuoriesce, spesso scatenando infiammazione. Questo processo è normalmente guidato da una catena di proteine, con una chiamata RIPK3 che funge da fulcro e un’altra, MLKL, che perfora la membrana cellulare. Nei percorsi canonici, RIPK3 viene attivata da proteine partner che riconoscono segnali di pericolo come molecole infiammatorie o materiale genetico virale. Qui il gruppo ha scoperto che la bilirubina può bypassare questi partner abituali e comunque indurre necroptosi nei neuroni.
La bilirubina afferra l’interruttore mortale della cellula
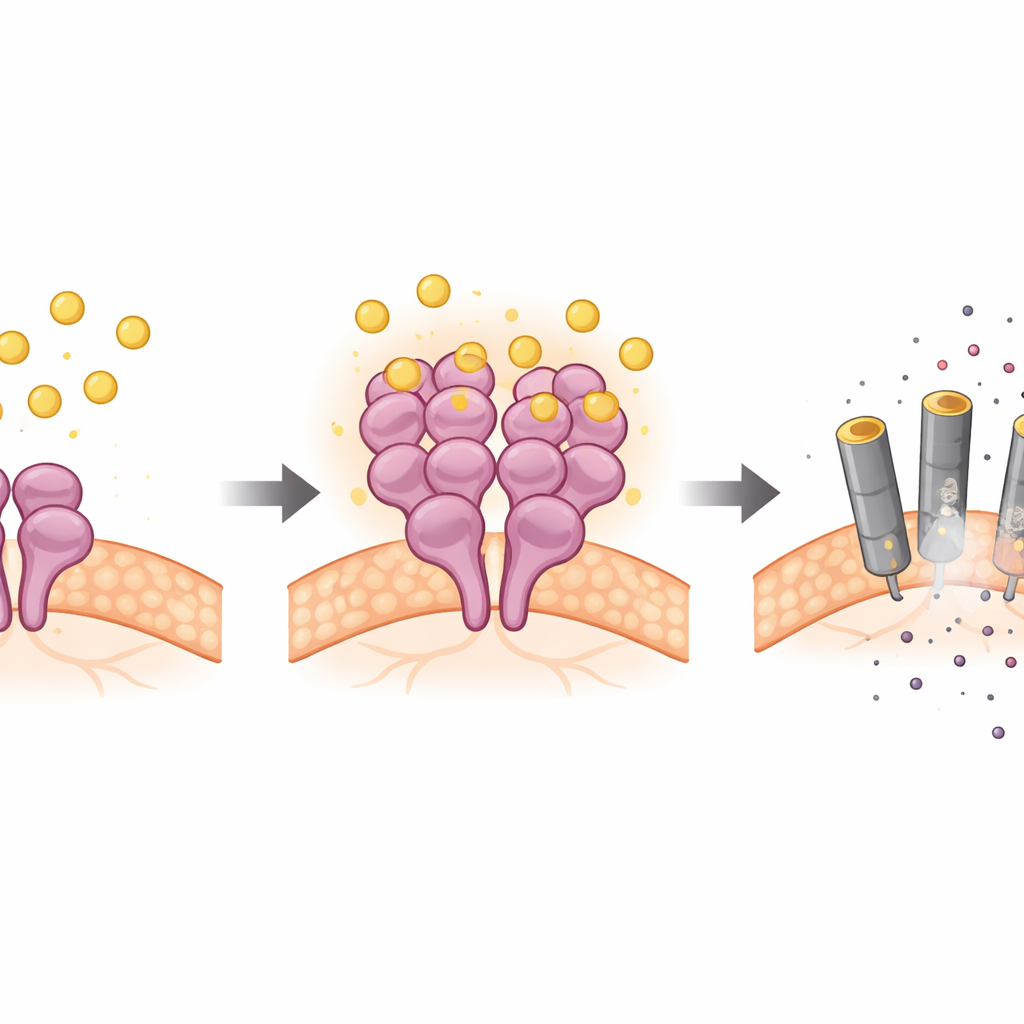
Usando neuroni coltivati, fette di cervello e modelli murini, gli scienziati hanno dimostrato che la bilirubina attiva selettivamente RIPK3 e il suo partner a valle MLKL nei neuroni, lasciando sostanzialmente inalterate le proteine a monte abituali. Esperimenti genetici hanno rivelato che quando RIPK3 o MLKL venivano rimossi, la bilirubina non riusciva più a uccidere efficacemente i neuroni. Test biochimici sono andati oltre: la bilirubina si legava fisicamente a RIPK3 in due punti specifici all’interno del suo nucleo attivo, favoriva l’aggregazione delle molecole di RIPK3 e ne aumentava l’attività chinasica — la funzione chimica che accende la via di morte. Questa presa diretta su RIPK3 non dipendeva dalla superficie di interazione tipica della proteina (il dominio RHIM) né da altri adattatori, delineando una via non classica verso la necroptosi.
Evidenza dal cervello vivente
Per verificare se questo meccanismo avesse rilevanza negli animali interi, il team ha aumentato i livelli di bilirubina nei topi sia iniettandola nel cervello sia inducendo danno epatico e infiammazione in modo che la bilirubina entrasse naturalmente nel cervello. Nei topi normali ciò ha portato a una forte attivazione di RIPK3 e MLKL in regioni cerebrali vulnerabili, a un aumento dei marker di morte cellulare e a una perdita visibile di neuroni sani. I topi ingegnerizzati per essere privi di RIPK3 erano protetti: i loro neuroni mostravano danni molto più contenuti, segnali di morte ridotti e risposte infiammatorie minori, nonostante i livelli di bilirubina fossero analoghi. È importante sottolineare che una forma processata e solubile in acqua della bilirubina, normalmente considerata innocua, né attivava RIPK3 né provocava danni cerebrali simili, sottolineando che il vero colpevole è la forma non modificata e liposolubile.
Cosa significa per i pazienti
Questo lavoro mostra che l’eccesso di bilirubina non coniugata può attivare direttamente RIPK3, scatenando una rottura controllata ma distruttiva delle cellule cerebrali tramite necroptosi. Piuttosto che agire solo come veleno generale o sorgente di stress ossidativo, la bilirubina si comporta come un piccolo attivatore molecolare di un programma di morte specifico in neuroni e cellule immunitarie cerebrali. Per i pazienti con grave ittero o insufficienza epatica, ciò suggerisce che bloccare RIPK3 o MLKL — specialmente con farmaci capaci di attraversare il cervello — potrebbe un giorno aiutare a limitare il danno neurologico. In termini semplici, lo studio mostra come un pigmento normalmente utile possa diventare un sicario molecolare preciso e indica nuove strade per neutralizzarlo senza compromettere i suoi ruoli protettivi quotidiani.
Citazione: Xue, Q., Ma, X., Chen, Z. et al. Bilirubin directly activates RIPK3 to induce non-classical necroptosis. Cell Discov 12, 21 (2026). https://doi.org/10.1038/s41421-026-00876-7
Parole chiave: neurotossicità da bilirubina, necroptosi, RIPK3, insufficienza epatica e danno cerebrale, vie di morte cellulare