Clear Sky Science · it
Pipeline integrata di profilazione spaziale per determinare le architetture del TME in campioni clinici di archivio utilizzando la tecnologia superplex CmTSA
Perché il paesaggio nascosto intorno ai tumori conta
I tumori non crescono in isolamento. Sono circondati da un vivace quartiere di cellule immunitarie, cellule di supporto, vasi sanguigni e tessuto cicatriziale che insieme formano il “microambiente” del tumore. Questo articolo presenta un metodo pratico per mappare in dettaglio quel paesaggio nascosto usando campioni tissutali standard degli ospedali. Rivelando quali tipi di cellule si trovano vicine tra loro e come si organizzano in quartieri utili o dannosi, il metodo potrebbe aiutare i medici a prevedere meglio il comportamento del cancro di un paziente e quali terapie hanno maggiori probabilità di funzionare.
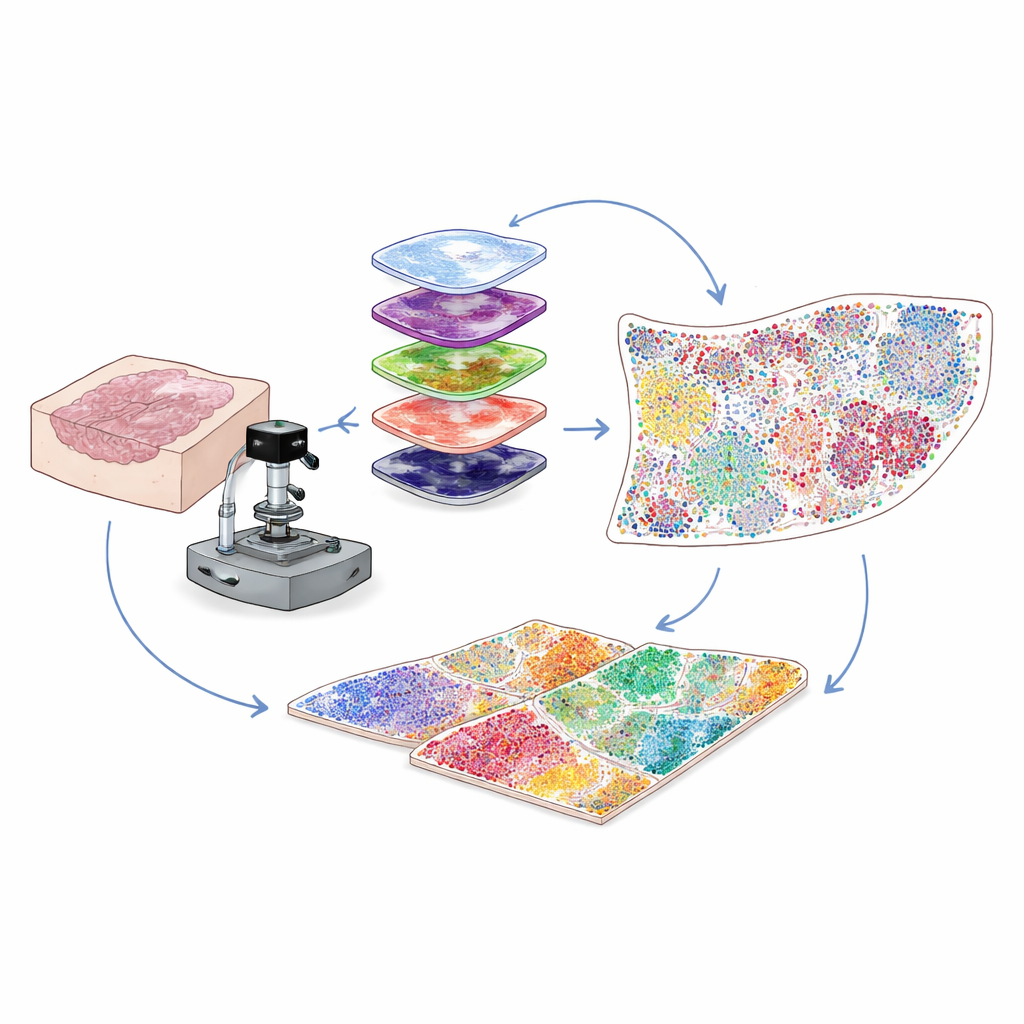
Vedere di più nei campioni ospedalieri di tutti i giorni
La maggior parte dei campioni clinici tumorali sono conservati come sottili sezioni di tessuto inglobato in paraffina, note come blocchi FFPE, che possono essere immagazzinate per anni. Sono una miniera d’oro per la ricerca, ma un problema tecnico ha limitato gli scienziati: questi campioni emettono una fluorescenza di fondo naturale che copre i segnali deboli di molte proteine importanti. Gli autori hanno risolto questo problema combinando luce intensa e attentamente calibrata con un trattamento chimico lieve per cancellare selettivamente quel bagliore di fondo senza danneggiare il tessuto o i bersagli proteici. Questo passaggio ibrido, ottico e chimico di “sbiancamento” aumenta nettamente la nitidezza delle immagini, consentendo di rilevare segnali proteici deboli che altrimenti andrebbero persi.
Dipingere decine di marcatori proteici sulla stessa sezione
Per capire quali cellule sono presenti e cosa stanno facendo, gli scienziati colorano i tessuti con anticorpi che si legano a proteine specifiche. I metodi multiplex tradizionali o faticano con segnali deboli per proteine rare o permettono di monitorare solo un numero limitato di marcatori alla volta. Qui il gruppo utilizza un approccio chiamato amplificazione del segnale tramite tirosina (cyclic tyramide signal amplification). In ogni ciclo, un piccolo set di marcatori viene colorato e sviluppato enzimaticamente in punti fluorescenti brillanti e permanentemente legati. Gli anticorpi vengono poi rimossi delicatamente mentre il segnale rimane, il fondo viene nuovamente sbiancato e si aggiunge il set successivo di marcatori. Ripetendo questo ciclo molte volte e allineando le immagini usando il segnale costante dei nuclei cellulari, è possibile visualizzare in modo affidabile da 30 a 60 proteine diverse su una singola sezione tissutale, sull’intera vetrino, a risoluzione di singola cellula.
Trasformare immagini colorate in un atlante cellula per cellula
Le immagini ad alto plex contengono milioni di pixel, molto più di quanto un essere umano possa analizzare a occhio. Gli autori costruiscono quindi una pipeline di computer vision che prima individua e delimita ogni nucleo cellulare usando strumenti di deep learning sviluppati originariamente per la segmentazione cellulare generale. Poi, in base a dove appare la fluorescenza di ciascuna proteina—sulla membrana, nel citoplasma o nel nucleo—e a insiemi di regole logiche, ogni cellula viene assegnata a un tipo o sottotipo, come cellula tumorale, cellula T helper, cellula T citotossica, cellula B, fibroblasto o altri. Il risultato è una tabella digitale che elenca, per ogni cellula sul vetrino, la sua identità e le coordinate esatte. Questo trasforma un’immagine complessa in una mappa quantitativa di chi si trova dove all’interno del microambiente tumorale.
Rivelare i quartieri cellulari che influenzano l’esito
Le cellule raramente agiscono da sole; ciò che conta sono i vicini che hanno. Per catturare questo, i ricercatori testano diversi modi per definire i quartieri locali intorno a ogni cellula e scelgono un approccio basato su una rete a raggio. Immaginate di tracciare un piccolo cerchio—circa lo spessore di un capello umano—intorno a ogni cellula e di elencare chi vive al suo interno. Raggruppando le cellule i cui cerchi circostanti hanno miscele simili di vicini, il metodo identifica “nicchie funzionali” ricorrenti, come zone ricche di cellule immunitarie, barriere ricche di fibroblasti o regioni dominate dal tumore. Applicando questa strategia al tessuto del colon, i ricercatori mostrano che i quartieri basati sul raggio si allineano meglio con le strutture anatomiche note rispetto a metodi alternativi. In campioni di cancro cervicale provenienti da pazienti con esiti favorevoli rispetto a quelli sfavorevoli, il gruppo trova che le nicchie ricche di cellule immunitarie si raggruppano vicino al bordo del tumore nei pazienti con esito positivo, mentre i pazienti con peggiori esiti mostrano spesse zone dense di fibroblasti che avvolgono le cellule tumorali e sembrano isolare le cellule immunitarie attaccanti.
Dalle mappe spaziali a trattamenti su misura
Combinando colorazioni di alta qualità e a basso costo per molte proteine con un’analisi delle immagini robusta, questo lavoro offre una pipeline end-to-end applicabile a un gran numero di campioni ospedalieri standard. Il metodo trasforma il tessuto conservato in mappe dettagliate su come cellule tumorali, immunitarie e stromali si dispongono e interagiscono. Per i lettori non specialisti, la conclusione è che non solo i tipi di cellule, ma i loro pattern di vicinato precisi, contano per il comportamento del cancro. Questa piattaforma può aiutare i ricercatori a individuare punti caldi immunitari protettivi, identificare barriere cellulari soppressive e, in ultima analisi, supportare prognosi più accurate e strategie di immunoterapia più finemente tarate.
Citazione: Xiao, C., Zhou, R., Chen, Q. et al. Integrative spatial profiling pipeline for determining TME architectures in archival clinical specimens using CmTSA superplex technology. Cell Discov 12, 16 (2026). https://doi.org/10.1038/s41421-026-00874-9
Parole chiave: microambiente tumorale, proteomica spaziale, imaging multiplex, immunologia del cancro, analisi a singola cellula