Clear Sky Science · it
Variazioni dinamiche del microambiente immunitario nel carcinoma ovarico dopo chemioterapia neoadiuvante
Perché questa ricerca è importante per le donne con carcinoma ovarico
Il carcinoma ovarico avanzato viene spesso trattato con chemioterapia potente prima o dopo l’intervento chirurgico, eppure molte donne vedono la malattia ricomparire e perdere sensibilità ai farmaci. Questo studio affronta una domanda pressante: come rimodella silenziosamente la chemioterapia le difese naturali del corpo intorno al tumore e possiamo modulare tale risposta per prolungare l’efficacia del trattamento? Analizzando singole cellule e testando nuove combinazioni di farmaci nei topi, i ricercatori rivelano un ruolo nascosto di molecole lipidiche simili a ormoni chiamate prostaglandine nell’aiutare i tumori a eludere il sistema immunitario dopo la chemioterapia.
Un campo di battaglia che cambia intorno al tumore
I tumori ovarici non crescono isolati: si trovano in un «quartiere» affollato di cellule immunitarie, tessuto connettivo e liquido addominale. Prima del trattamento, questo contesto è già sbilanciato a favore del cancro, con poche cellule T citotossiche aggressive e molte cellule che attenuano l’attacco immunitario. Il gruppo ha analizzato dati di single‑cell RNA sequencing pubblicati in precedenza su donne con carcinoma sieroso di alto grado, confrontando campioni prelevati prima e dopo la chemioterapia neoadiuvante (somministrata prima dell’intervento). Hanno scoperto che la chemioterapia non si limita a uccidere le cellule tumorali; provoca anche un aumento temporaneo dell’attività immunitaria, incrementando segnali legati alla stimolazione delle cellule T e all’infiammazione, mentre riduce alcune cellule T regolatorie che solitamente sopprimono la risposta immunitaria.
Quando cambiamenti utili diventano dannosi
Nonostante questo rapido impulso, la maggior parte delle pazienti va comunque incontro a recidiva e sviluppa resistenza ai farmaci a base di platino come il cisplatino. Per capire il perché, i ricercatori hanno indagato più a fondo come i diversi tipi cellulari comunicano tra loro dopo il trattamento. Hanno scoperto che la chemioterapia aumentava fortemente l’espressione di geni coinvolti nella sintesi delle prostaglandine nei macrofagi associati al tumore e nei fibroblasti, e potenziava la comunicazione tra queste cellule e le cellule T. Utilizzando strumenti matematici avanzati, hanno mostrato che l’insieme del microambiente si spostava verso uno stato pro‑infiammatorio ma sostanzialmente soppressivo, con livelli crescenti di chemochine che attirano cellule mieloidi e vie che possono esaustare le cellule T nel tempo. Ciò suggerisce che le prostaglandine possano funzionare come un interruttore molecolare, trasformando un’impennata immunitaria inizialmente utile in un freno duraturo sull’immunità anti‑tumorale.
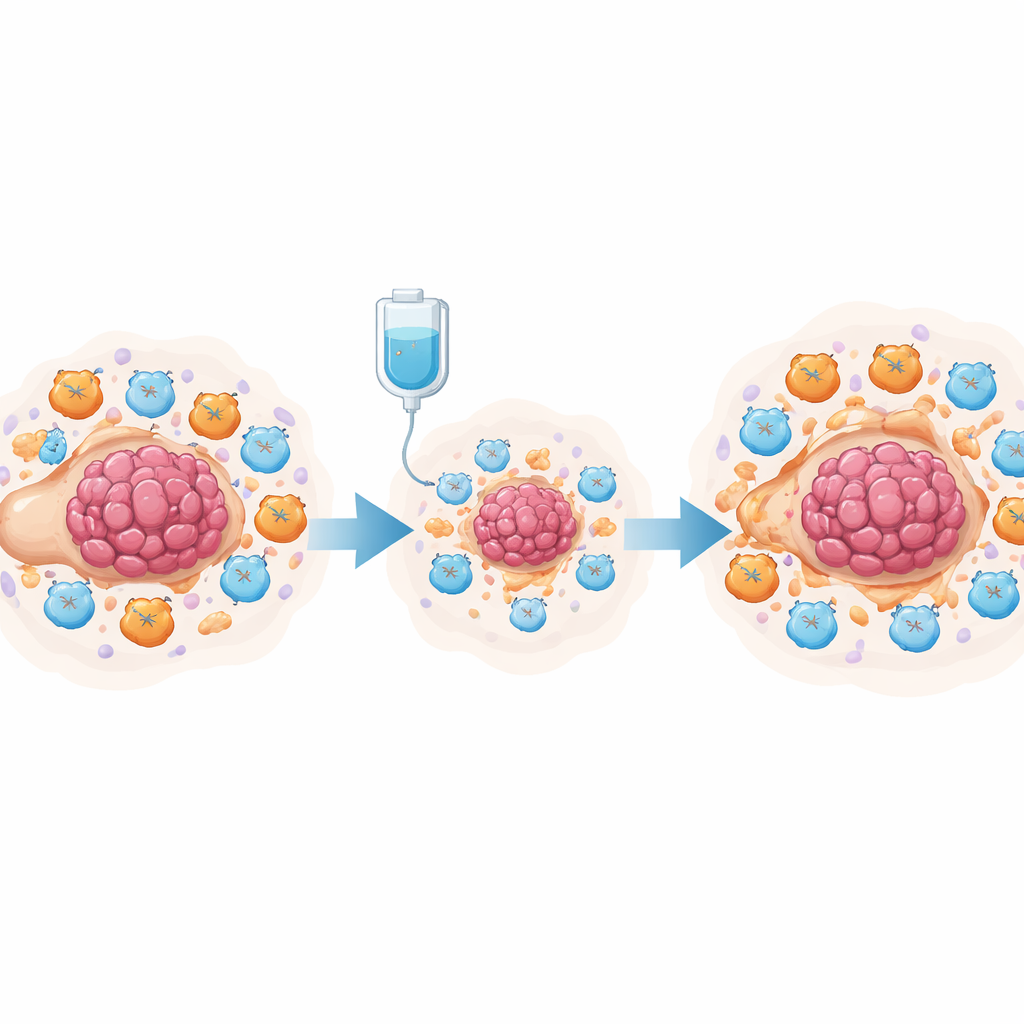
Chemioterapia, prostaglandine e cellule T silenziate
Per verificare sperimentalmente questa ipotesi, il gruppo ha utilizzato un modello murino di carcinoma ovarico trattato con cisplatino. L’analisi single‑cell di decine di migliaia di cellule dal cavo addominale ha mostrato che il cisplatino riduceva le cellule tumorali e aumentava il numero totale di cellule T, ma espandeva in modo marcato le cellule soppressive derivate dalla linea mieloide (MDSC) e le cellule T citotossiche esauste. Sia le cellule tumorali sia queste cellule soppressive esprimevano alti livelli di enzimi per la sintesi delle prostaglandine. In co‑coltura, le cellule tumorali trattate con cisplatino inducevano le cellule del midollo osseo ad assumere uno stato simile alle MDSC e indebolivano l’attività e la proliferazione delle cellule T CD8+ citotossiche. I ricercatori hanno ricondotto questo effetto alla via di segnalazione NF‑κB nelle cellule tumorali, che attiva il gene PTGES, un passaggio cruciale nella produzione di prostaglandina E2. Il blocco di questa via riduceva i livelli di PTGES e la produzione di prostaglandine.
Voltare le sorti con la terapia combinata
La domanda più pratica era se inibire le prostaglandine potesse rendere la chemioterapia più efficace. Nei topi, gli scienziati hanno usato la delezione genetica di Ptges nelle cellule tumorali, anticorpi neutralizzanti la prostaglandina E2 o piccoli inibitori della prostaglandin E synthase. Tutti questi approcci abbassarono i livelli di prostaglandine, ridussero l’accumulo di MDSC e ristabilirono la capacità citotossica e la resilienza «stem‑like» delle cellule T CD8+. In combinazione con il cisplatino, o con il regime standard cisplatino‑paclitaxel, gli inibitori delle prostaglandine rallentarono la crescita e la diffusione tumorale più efficacemente che la sola chemioterapia. I dati indicano che la soppressione immunitaria guidata dalle prostaglandine non è un dettaglio marginale ma una ragione centrale per cui i tumori sfuggono dopo una risposta iniziale.
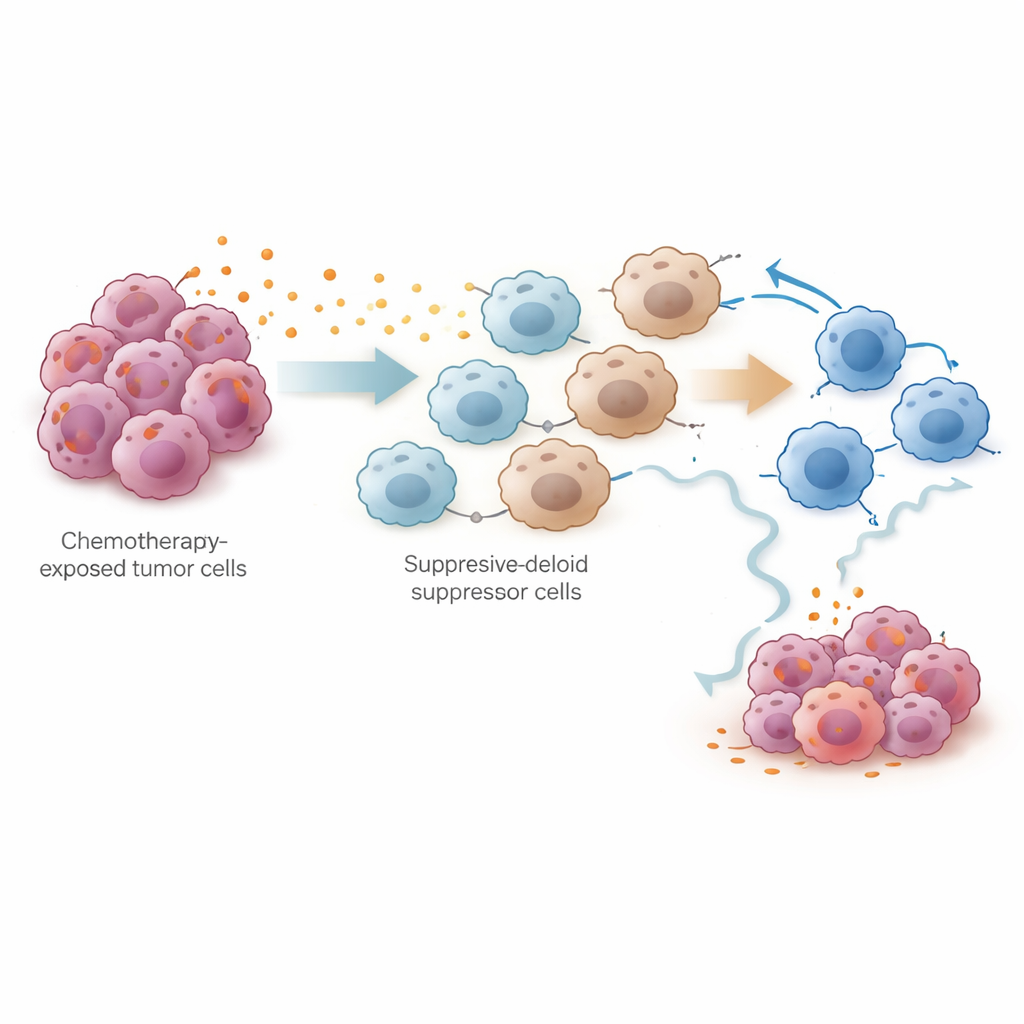
Un nuovo approccio per mantenere il trattamento efficace
In termini pratici, questo lavoro suggerisce che la chemioterapia modifica l’ambiente tumorale in due fasi: prima indebolisce il cancro e mobilita brevemente il sistema immunitario, poi innesca un’ondata di prostaglandine che richiamano cellule soppressive e affaticano le forze naturali che eliminano il tumore. Identificando la produzione di prostaglandine guidata da PTGES come un colpevole chiave, lo studio indica una strategia concreta: associare la chemioterapia a base di platino con farmaci che bloccano le vie delle prostaglandine potrebbe contribuire a mantenere un attacco immunitario efficace e a ritardare o prevenire la recidiva nel carcinoma ovarico. Pur richiedendo ancora studi clinici, questo approccio combinato offre una direzione promettente per estendere il beneficio dei trattamenti esistenti.
Citazione: Wu, M., Lv, F., Jin, Y. et al. Dynamic changes of the immune microenvironment in ovarian cancer following neoadjuvant chemotherapy. Cell Death Discov. 12, 130 (2026). https://doi.org/10.1038/s41420-026-03070-6
Parole chiave: carcinoma ovarico, microambiente tumorale, resistenza alla chemioterapia, prostaglandine, immunoterapia