Clear Sky Science · it
Il contesto epigenetico definisce l’attività trascrizionale dei segnali NF-κB canonici e non canonici nel carcinoma pancreatico
Perché questo studio è importante per i pazienti
Il carcinoma pancreatico è uno dei tumori più letali, in parte perché le sue cellule sono molto abili nel leggere e rispondere ai segnali di pericolo presenti nell’ambiente circostante. Questo studio esamina due di questi segnali, chiamati TNFα e TWEAK, e mostra come essi attivino diverse “modalità di lettura” nel DNA delle cellule tumorali. Comprendere queste modalità potrebbe aprire nuove strade per rallentare la crescita del tumore, limitarne la diffusione e rendere i trattamenti più efficaci.
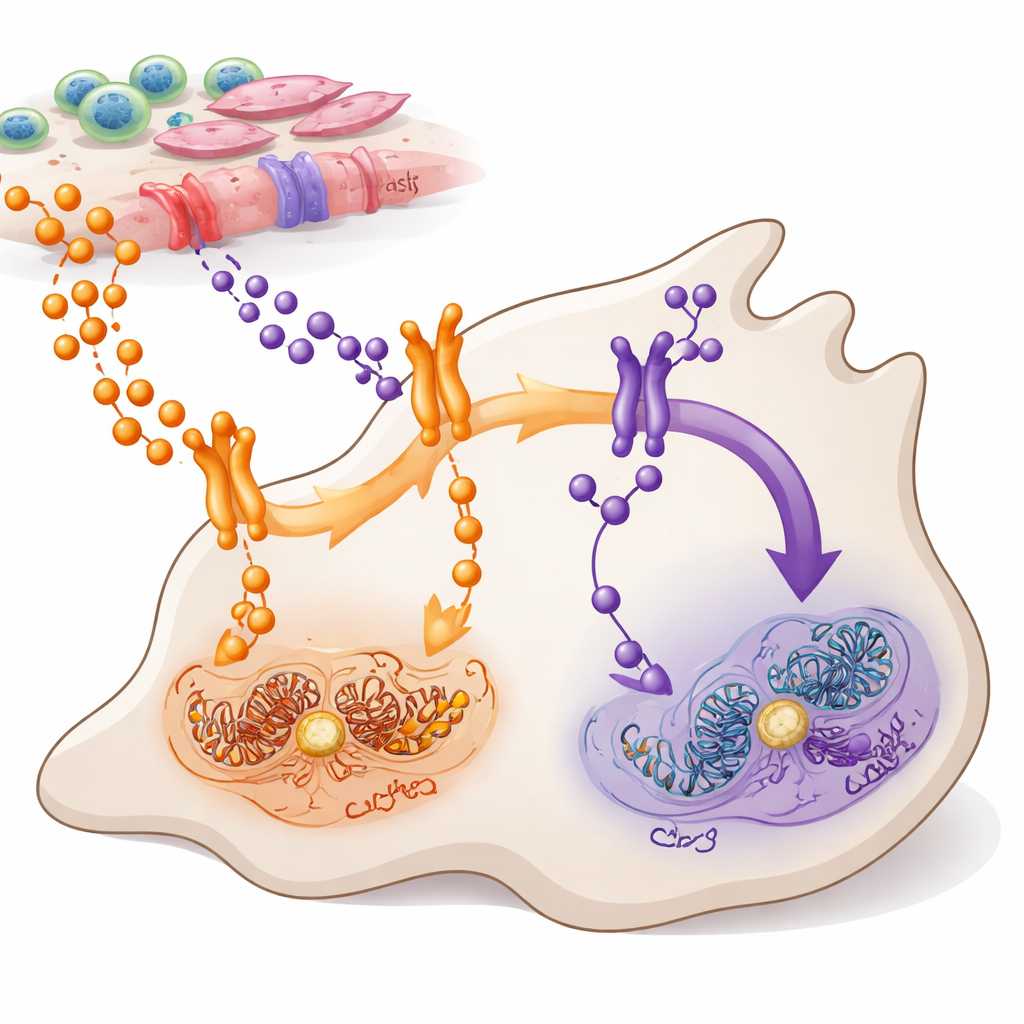
Due percorsi di messaggistica nelle cellule tumorali
TNFα e TWEAK sono piccoli messaggeri proteici rilasciati da cellule dentro e intorno a un tumore. Entrambi comunicano con un importante sistema di controllo intracellulare noto come NF-κB, che contribuisce a decidere se le cellule crescono, si muovono o muoiono. Gli autori si sono concentrati sull’adenocarcinoma duttale pancreatico, la forma più comune e aggressiva di carcinoma pancreatico, in cui NF-κB è anormalmente attivo nella maggior parte dei tumori. Hanno mappato quali cellule producono TNFα e TWEAK, quali cellule esprimono i loro recettori e come questi segnali si propagano attraverso due rami correlati di NF-κB—spesso chiamati il percorso canonico (tramite RELA) e quello non canonico (tramite RELB).
Chi invia i segnali nel quartiere del tumore
Combinando l’analisi di RNA a singola cellula su migliaia di cellule provenienti da tumori di pazienti con microscopia avanzata, il gruppo ha scoperto che TNFα deriva principalmente da cellule immunitarie, in particolare macrofagi e alcuni tipi di cellule T e B. TWEAK, invece, è prodotto da un insieme più ampio di cellule: macrofagi, fibroblasti, cellule endoteliali e stellate. Anche i loro recettori sono diversi. Le cellule tumorali e i fibroblasti vicini esprimono fortemente sia il principale recettore di TNFα sia il recettore chiave per TWEAK. L’analisi di rete ha suggerito che la segnalazione basata su TWEAK costituisce una rete di comunicazione più ampia e complessa tra cellule tumorali e di supporto, mentre la segnalazione mediata da TNFα è più concentrata nelle aree ricche di cellule immunitarie.
Diverse profondità di risposta all’interno delle cellule tumorali
In linee cellulari di carcinoma pancreatico, i ricercatori hanno trattato le cellule con TNFα o TWEAK e misurato quali geni venivano attivati nel tempo. TNFα ha scatenato un’onda rapida e ampia di attività genica collegata a infiammazione, migrazione cellulare, rimodellamento dei tessuti e sopravvivenza. TWEAK ha indotto un set più piccolo e più lento di cambiamenti che si sovrapponevano in larga misura ai bersagli di TNFα anziché avviare un programma del tutto distinto. Entrambi i segnali potevano favorire la migrazione cellulare e, in certe condizioni, la morte cellulare, ma TNFα aveva un effetto più marcato sul movimento. Esaminando i dati dei tumori dei pazienti provenienti da The Cancer Genome Atlas, il team ha visto che i tumori con alti livelli di TNFα o di TWEAK condividevano molti geni attivati, confermando questi schemi nei tumori umani reali.
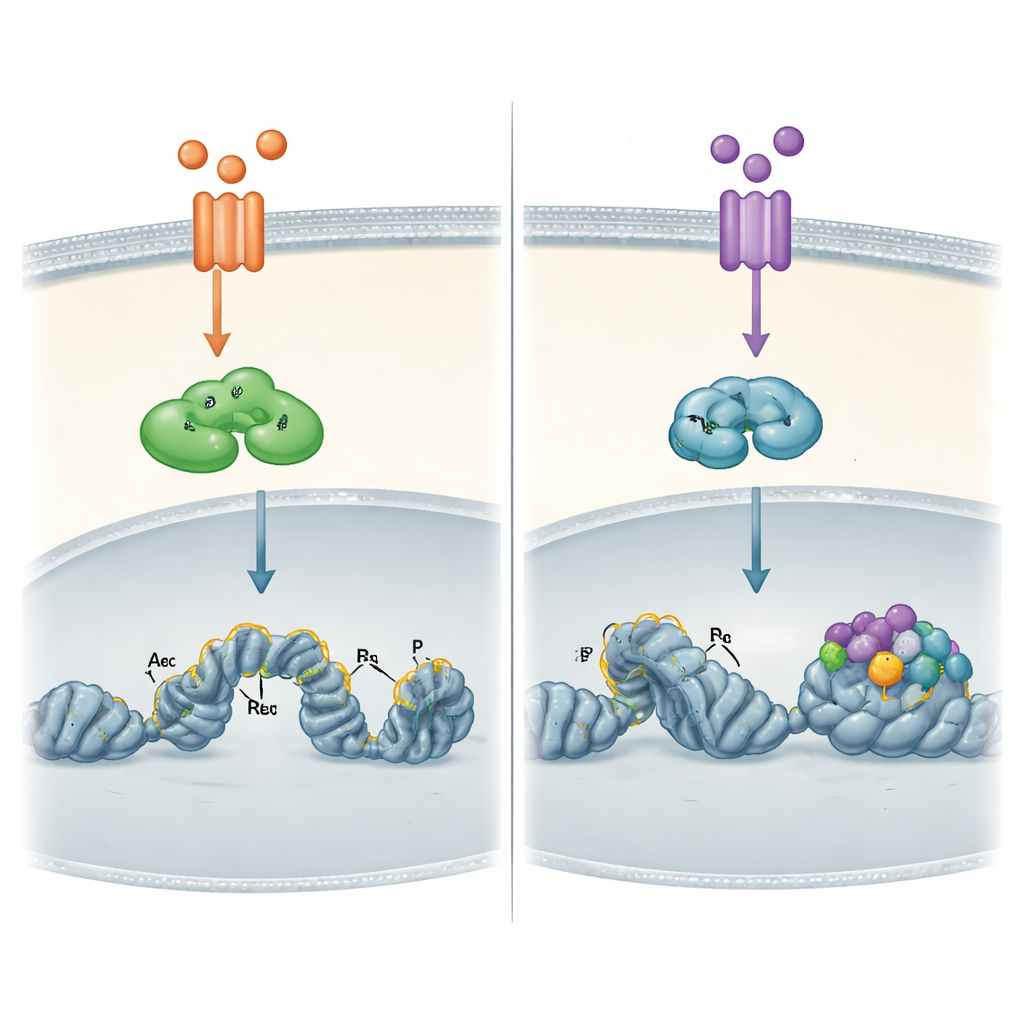
Come il paesaggio del DNA modella ogni via
Le differenze più evidenti sono emerse quando gli autori hanno osservato direttamente la cromatina delle cellule tumorali—la forma condensata del DNA e delle proteine associate. Usando mappe genomiche dei siti di legame, hanno mostrato che RELA attivato da TNFα può legarsi non solo a regioni di DNA già aperte ma anche a regioni più compatte e contribuire poi ad “aprirle” aggiungendo marcature chimiche associate a elementi attivi. RELB, attivato più tardivamente da TWEAK, si legava quasi esclusivamente a siti già accessibili e decorati con tali marche di attività. Questi siti legati da RELB erano particolarmente ricchi di motivi di docking per un’altra famiglia di fattori, AP-1, suggerendo che RELB dipende da altre proteine che preparano il terreno prima che possa agire.
Cosa significa questo per i trattamenti futuri
Per un non specialista, la conclusione principale è che TNFα e TWEAK utilizzano lo stesso arsenale NF-κB in modi molto diversi. TNFα, attraverso RELA, si comporta come un interruttore generale in grado di forzare l’apertura di sezioni chiuse del DNA delle cellule tumorali e di attivare un’ampia gamma di geni coinvolti nella crescita, nella sopravvivenza e nella diffusione. TWEAK, tramite RELB, è più simile a uno specialista che può agire solo dove il DNA è già aperto e dove sono presenti cofattori come AP-1. Questa divisione del lavoro suggerisce che farmaci che prendono di mira il rimodellamento della cromatina, AP-1 o rami specifici di NF-κB potrebbero smorzare selettivamente programmi genici dannosi nel carcinoma pancreatico, lasciando nel contempo altre funzioni relativamente intatte.
Citazione: Aggrey-Fynn, J.E., Busch, J., Saul, D. et al. Epigenetic context defines the transcriptional activity of canonical and noncanonical NF-κB signaling in pancreatic cancer. Cell Death Discov. 12, 152 (2026). https://doi.org/10.1038/s41420-026-03019-9
Parole chiave: carcinoma pancreatico, segnalazione NF-kappaB, microambiente tumorale, regolazione epigenetica, TNF e TWEAK