Clear Sky Science · it
Sfruttare la piroptosi nella terapia del tumore al seno: meccanismi immunologici e strategie emergenti con biomateriali
Trasformare la morte cellulare in una nuova arma contro il tumore al seno
Il tumore al seno rimane uno dei tumori più comuni e difficili da sconfiggere a livello globale. Molti tumori alla fine sfuggono alla chirurgia, alla chemioterapia e persino alle immunoterapie moderne. Questa review esplora un’idea emergente: indurre deliberatamente all’interno dei tumori mammari una forma “infuocata” di morte cellulare chiamata piroptosi. Facendo esplodere le cellule tumorali in modo controllato e infiammatorio, gli scienziati sperano sia di uccidere direttamente il tumore sia di risvegliare il sistema immunitario perché si unisca all’attacco.
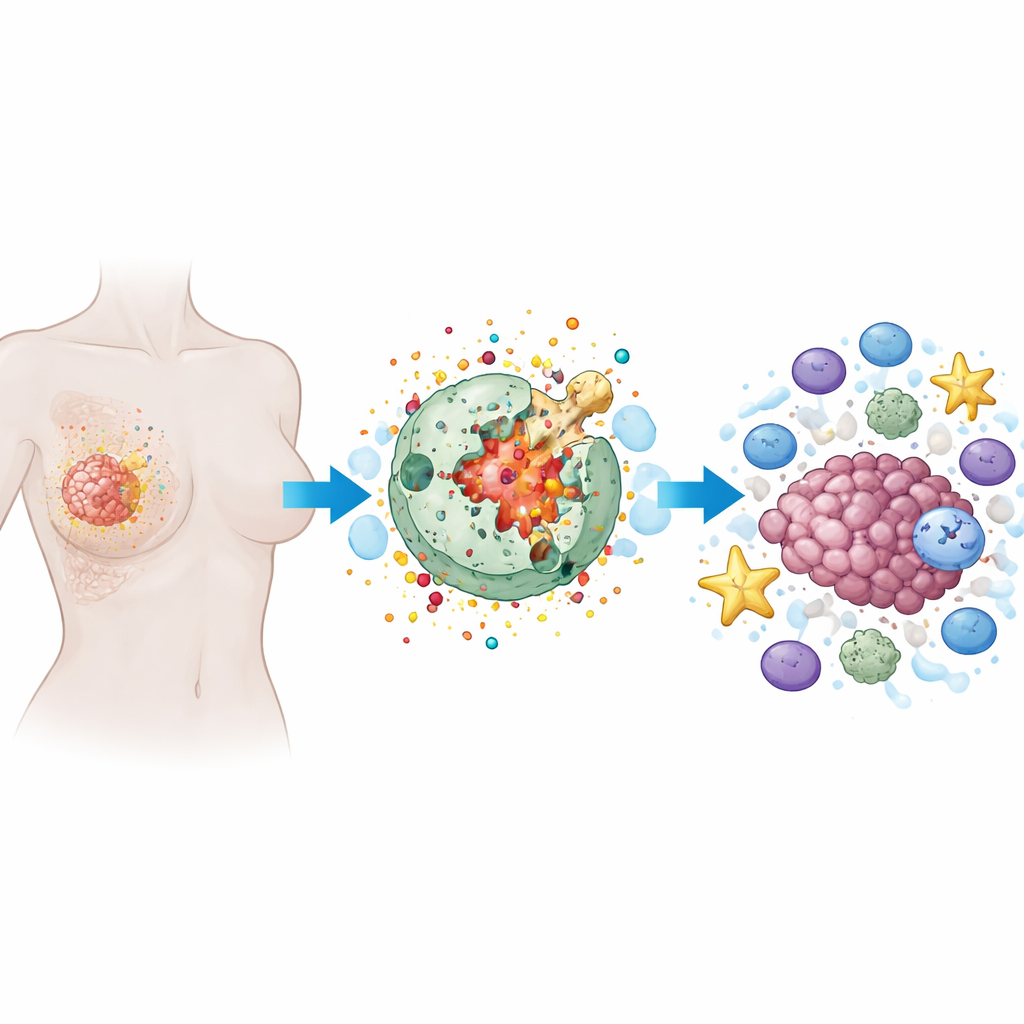
Come funziona una forma «infuocata» di morte cellulare
La piroptosi è una forma programmata di morte cellulare in cui la cellula si rigonfia, la sua membrana esterna viene perforata da pori e infine si rompe, rilasciando il contenuto. A differenza della morte cellulare silenziosa e ordinata osservata in molte terapie, la piroptosi è rumorosa e infiammatoria. Proteine specializzate, in particolare una famiglia chiamata gasdermine, agiscono come piccole cariche di demolizione. Una volta tagliate da enzimi interni, le gasdermine fanno dei fori nella membrana cellulare. Questo non solo distrugge la cellula tumorale, ma rilascia anche segnali d’allarme e molecole infiammatorie che possono richiamare e attivare le cellule immunitarie.
Perché i tumori mammari sono una sfida speciale
Il tumore al seno non è una singola malattia, ma una collezione di sottotipi con comportamenti differenti. Alcuni, come il carcinoma mammario triple‑negativo, sono privi di bersagli farmacologici comuni e spesso resistono ai trattamenti. Molti tumori mammari sono considerati «immunologicamente freddi», cioè contengono poche cellule immunitarie attive. La review spiega come caratteristiche del microambiente tumorale mammario — comprese cellule stromali, cellule immunosoppressive e carenze locali di ossigeno — possano sia predisporre alla piroptosi sia, se mal gestite, trasformare l’infiammazione in carburante per la crescita e la diffusione del tumore. Questa natura a doppio taglio rende la precisione particolarmente importante.
Gli interruttori delle gasdermine all’interno delle cellule tumorali
Un tema centrale dell’articolo è come diverse proteine gasdermina fungano da interruttori molecolari all’interno delle cellule del tumore mammario. Varianti come GSDMD e GSDME possono convertire segnali provenienti da chemioterapia, radioterapia o cellule immunitarie in piroptosi completa. Altre, come GSDMC e alcune forme di GSDMB, sono spesso aumentate nei tumori aggressivi e possono promuovere o limitare la malattia a seconda di come vengono attivate. Molti tumori mammari silenziano chimicamente GSDME, attenuando la piroptosi e l’attivazione immunitaria. Ripristinare o attivare selettivamente le gasdermine giuste potrebbe determinare se una terapia uccide poche cellule o trasforma l’intero tumore in un vaccino in situ che allerta il sistema immunitario.
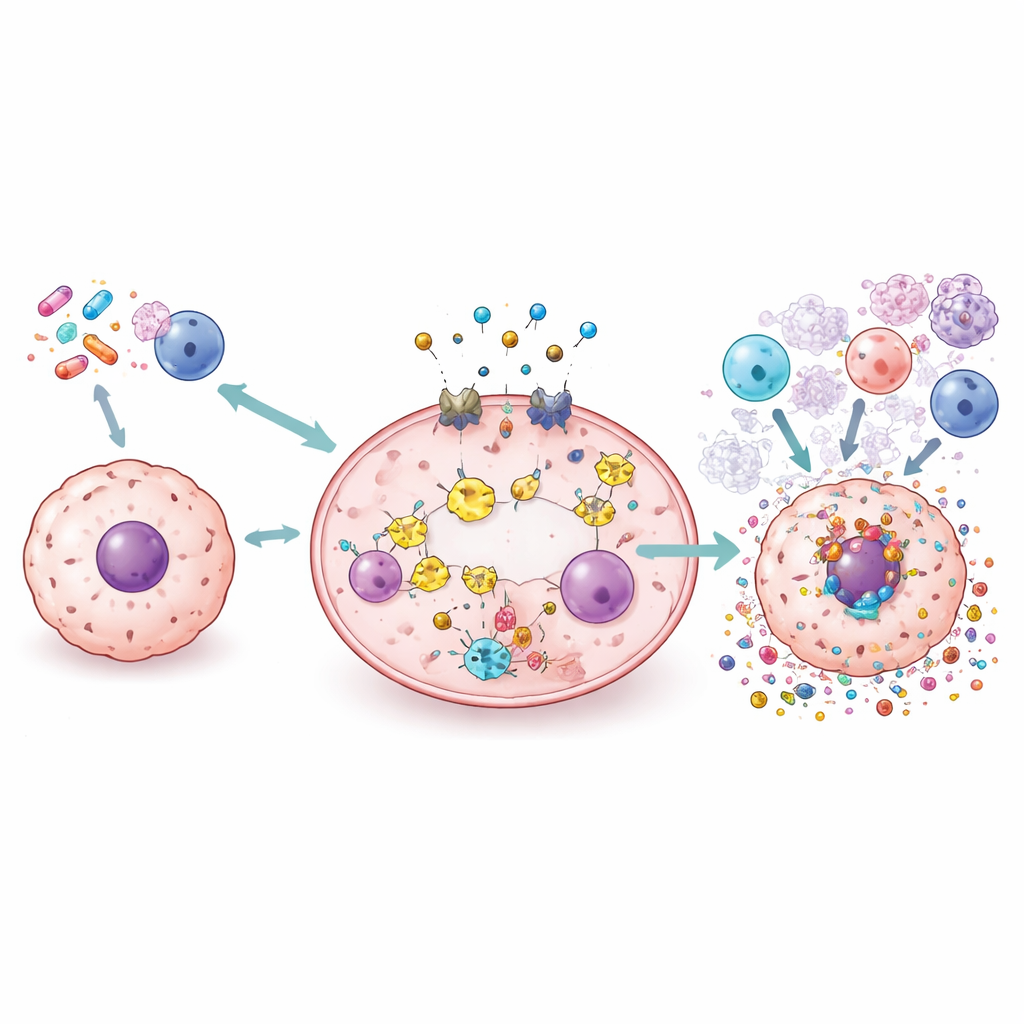
Nuovi strumenti: farmaci, nanoparticelle, virus e radiazioni
La review passa in rassegna una vasta gamma di strategie in studio per sfruttare la piroptosi in modo sicuro. Farmaci standard come cisplatino e doxorubicina possono essere riproposti o riformulati per indirizzare le cellule tumorali verso uno scoppio guidato dalle gasdermine invece che verso una morte silenziosa. Piccole molecole possono amplificare o bloccare parti della via per modulare finemente l’infiammazione. Nanoparticelle e vettori biomimetici sono progettati per veicolare chemioterapici, ioni rame o molecole attivabili dalla luce direttamente nel tumore, dove scatenano la piroptosi risparmiando i tessuti sani. Virus oncolitici e la radioterapia possono essere ingegnerizzati o combinati con altri agenti per provocare piroptosi e rimodellare il paesaggio immunitario tumorale, rendendo potenzialmente più efficaci i farmaci che bloccano i checkpoint immunitari.
Bilanciare benefici potenti e rischi reali
Poiché la piroptosi è altamente infiammatoria, le stesse reazioni che aiutano il sistema immunitario a combattere il cancro possono anche danneggiare tessuti normali o perfino favorire la crescita tumorale se diventano croniche. Gli autori evidenziano biomarcatori precoci — come firme geniche, pattern di metilazione, frammenti di proteine gasdermina nel sangue e profili di citochine — che potrebbero aiutare a identificare quali pazienti beneficeranno maggiormente e chi è a rischio più alto di pericolosi «corticìni» infiammatori. Progettazioni avanzate in nanomedicina, combinazioni farmacologiche scelte con cura e monitoraggio in tempo reale dei marker infiammatori sono tutte strategie in studio per mantenere la risposta efficace ma controllata.
Cosa potrebbe significare per i pazienti futuri
In termini semplici, questa review sostiene che indurre le cellule tumorali a «morire a gran voce» potrebbe trasformare la cura del tumore al seno. Attivando la piroptosi in un sottogruppo mirato di cellule tumorali, i medici potrebbero sia ridurre il volume del tumore sia risvegliare una risposta immunitaria potente e duratura, trasformando tumori freddi in tumori caldi e più sensibili alle immunoterapie moderne. Tuttavia la piroptosi è un’alleata volubile: se liberata troppo ampiamente o per troppo tempo, può peggiorare l’infiammazione o favorire la comparsa di cellule resistenti. Le ricerche future si concentreranno sull’identificare chi trarrà beneficio, perfezionare i sistemi di somministrazione mirata e condurre trial clinici che combinino approcci che inducono piroptosi con farmaci immunoterapici. Se queste sfide saranno superate, sfruttare la piroptosi potrebbe aggiungere una nuova e potente dimensione al trattamento del tumore al seno.
Citazione: Asiedu, R.K.F., Souley Abdou, M., Wei, R. et al. Harnessing pyroptosis in breast cancer therapy: immunological mechanisms and emerging biomaterial strategies. Cell Death Discov. 12, 157 (2026). https://doi.org/10.1038/s41420-026-02996-1
Parole chiave: piroptosi, tumore al seno, gasdermina, microambiente tumorale, nanomedicina