Clear Sky Science · it
Dinamicità assoluta e staticità relativa: la relazione tra glicolisi e OXPHOS nello sviluppo del cancro
Perché contano le scelte energetiche del cancro
Le cellule tumorali sono come atleti di resistenza estremi: devono alimentarsi continuamente per crescere, diffondersi e sfuggire alle terapie. Questa rassegna spiega come le cellule del tumore sfruttino due sistemi energetici principali — uno rapido e uno efficiente — e, soprattutto, come li mescolino e passino dall’uno all’altro. Comprendere queste strategie energetiche in evoluzione offre un nuovo modo di concepire la diagnosi e il trattamento del cancro lungo tutto il decorso della malattia.
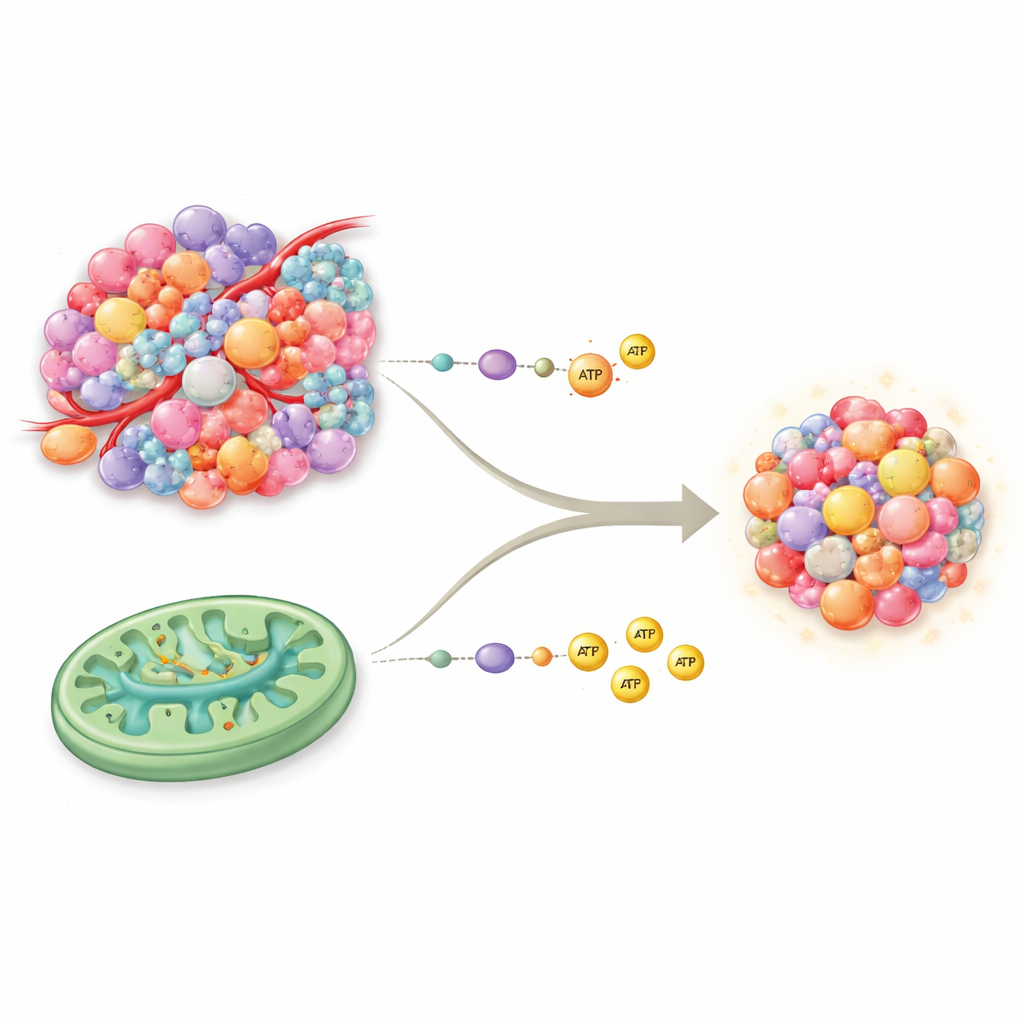
Due vie principali per produrre energia
Le nostre cellule producono energia tramite due percorsi fondamentali. La glicolisi è il sistema veloce, come denaro contante, che scinde rapidamente lo zucchero ma fornisce relativamente poca energia per unità. La fosforilazione ossidativa, o OXPHOS, avviene nei mitocondri e funziona più come una centrale ad alta efficienza, producendo molta più energia ma richiedendo un buon apporto di ossigeno e nutrienti. Per decenni si è ritenuto che il cancro dipendesse quasi esclusivamente dalla glicolisi anche in presenza di ossigeno — un comportamento noto come effetto Warburg. Nuove evidenze ribaltano questa visione semplicistica: molti tumori hanno mitocondri pienamente funzionanti e possono usare OXPHOS e il ciclo degli acidi tricarbossilici (TCA) accanto alla glicolisi, dotandosi così di un kit energetico più ricco e flessibile di quanto si pensasse.
Molti tipi cellulari, molte scelte di combustibile
Un tumore non è una massa uniforme. È un piccolo ecosistema che contiene cellule cancerose, cellule di supporto, vasi sanguigni e cellule immunitarie, ciascuna con esigenze energetiche diverse. Alcune cellule tumorali vivono vicino ai vasi e godono di abbondante ossigeno e nutrienti; altre sono sepolte in regioni scarsamente rifornite. Di conseguenza, cellule all’interno dello stesso tumore possono privilegiare la glicolisi, dipendere principalmente da OXPHOS o usare entrambi i processi contemporaneamente. Questa varietà metabolica — chiamata eterogeneità — deriva da differenze nel flusso sanguigno, nei livelli di nutrienti, nel tipo cellulare e nei segnali dell’ambiente circostante. Inoltre, i tumori mostrano spesso una simbiosi metabolica: le cellule glicolitiche esportano lattato come prodotto di scarto, che le cellule vicine dipendenti da OXPHOS importano e ossidano come combustibile prezioso. Uno scambio simile di lattato avviene tra cellule cancerose e cellule di supporto come fibroblasti, cellule dei vasi e cellule immunosoppressive, contribuendo collettivamente alla sopravvivenza del tumore e alla sua resistenza alle terapie.
In continua trasformazione: come l’energia tumorale cambia nel tempo
Il metabolismo tumorale non è solo vario in un dato momento; è anche altamente dinamico. Con la crescita, i tumori incontrano condizioni mutevoli come ipossia, accumulo di acidi, carenza di nutrienti e variazioni nella rigidità tissutale. In condizioni difficili e a basso ossigeno, molte cellule tumorali virano verso la glicolisi. In presenza di accumulo acido o privazione di zuccheri, possono invece tornare a un uso più intenso di OXPHOS. La stessa flessibilità si osserva in passaggi biologici chiave. Le cellule che si dividono rapidamente fanno affidamento sulla glicolisi per generare i mattoni necessari a nuovo DNA, lipidi e membrane. Le cellule quiescenti o in circolo nel sangue spesso dipendono maggiormente da OXPHOS. Durante invasione e metastasi, le cellule tumorali aggiustano ripetutamente la loro scelta di combustibile: alcuni passaggi favoriscono la glicolisi, altri l’OXPHOS, e le cellule metastatiche che colonizzano nuovi organi modulano il loro metabolismo per adattarsi al “terreno” del tessuto di destinazione.
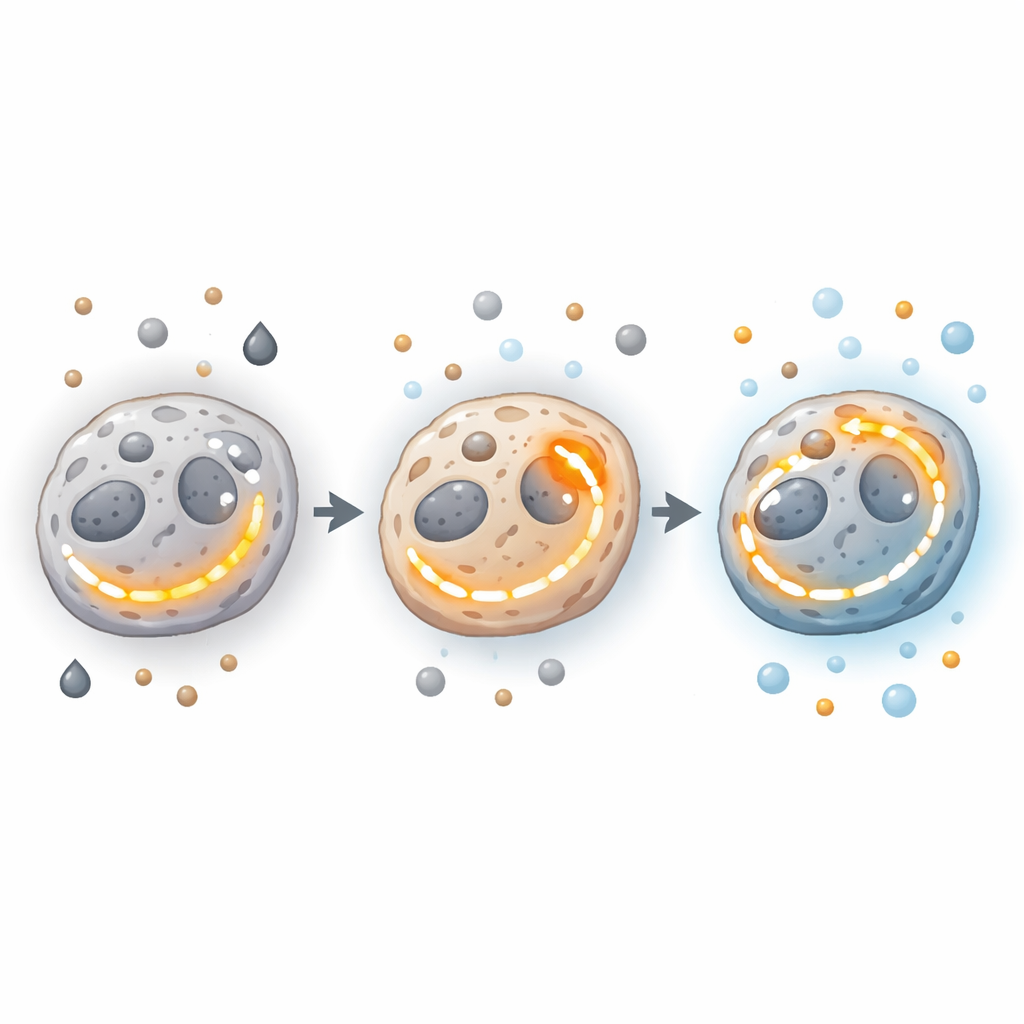
Geni, enzimi e centrali energetiche dietro lo switch
Nella macchina cellulare, geni ed enzimi indirizzano queste decisioni energetiche. Oncogeni e oncosoppressori possono spingere le cellule verso la glicolisi o l’OXPHOS, o abilitarle ad aumentare entrambi i percorsi. Mutazioni o alterazioni in enzimi chiave del TCA, come quelli che gestiscono citrato, succinato o isocitrato, possono spostare l’equilibrio, talvolta promuovendo segnali pro-tumorali come la crescita dei vasi e l’invasione. Enzimi situati in snodi critici — come la piruvato chinasi M2, che contribuisce a decidere se il carbonio derivato dagli zuccheri diventerà energia o materiale di costruzione — collegano la glicolisi alla funzione mitocondriale. Nel frattempo, differenze nel numero, nella struttura e nelle prestazioni dei mitocondri nelle varie regioni del tumore ampliano ulteriormente lo spettro di stati energetici possibili.
Riconsiderare la terapia attraverso un bersaglio energetico in movimento
Poiché le cellule tumorali possono alternare glicolisi e OXPHOS, bloccare semplicemente una via spesso non è sufficiente; il cancro può riorientare il suo uso di combustibile e sopravvivere. Gli autori sostengono che il metabolismo energetico nel cancro è solo temporaneamente stabile ed è fondamentalmente e costantemente in cambiamento. Propongono di considerare i tumori attraverso uno “spettro del metabolismo energetico” che va misurato nel tempo, non soltanto una volta. In pratica, questo potrebbe significare tracciare le preferenze di combustibile di un tumore durante i diversi stadi della malattia e combinare in modo mirato inibitori della glicolisi e dell’OXPHOS. Strategie terapeutiche dinamiche guidate dal metabolismo potrebbero interrompere meglio l’approvvigionamento energetico del tumore, limitarne la capacità di adattamento e migliorare il controllo a lungo termine della malattia.
Citazione: Bao, X., Hou, B., Guo, Z. et al. Absolute dynamic and relative static: the relationship of glycolysis and OXPHOS in cancer development. Cell Death Discov. 12, 136 (2026). https://doi.org/10.1038/s41420-026-02992-5
Parole chiave: metabolismo del cancro, glicolisi, fosforilazione ossidativa, microambiente tumorale, plasticità metabolica