Clear Sky Science · it
Esosomiale S100A9 promuove le metastasi polmonari del carcinoma adenoido‑cistico attivando i fibroblasti associati al tumore
Come un cancro silenzioso delle ghiandole salivari raggiunge i polmoni
Il carcinoma adenoido‑cistico è un tumore a crescita lenta ma tenace che spesso ha origine nelle ghiandole salivari e può manifestarsi nei polmoni anni dopo l’asportazione del tumore primario. Per pazienti e famiglie questa diffusione tardiva è spaventosa e difficile da prevedere o prevenire. Questo studio chiarisce come le cellule del tumore preparino a livello nascosto il tessuto polmonare distante all’invasione, rivelando una comunicazione segreta tra le cellule tumorali e le cellule di supporto circostanti che potrebbe offrire nuovi punti di intervento terapeutico.
Il tumore che persiste e ritorna
Il carcinoma adenoido‑cistico (ACC) è un tumore delle ghiandole della testa e del collo, in particolare delle ghiandole salivari. Chirurgia e radioterapia spesso controllano il tumore primario, ma molti pazienti sviluppano in seguito metastasi polmonari, che rappresentano la principale causa di morte. I farmaci disponibili per l’ACC diffuso sono limitati, in parte perché non si comprendono pienamente i meccanismi con cui le cellule del tumore primario si insediano e crescono nei polmoni. Gli autori di questo lavoro hanno cercato di identificare i segnali chiave che consentono alle cellule ACC di rimodellare l’ambiente circostante e creare un “terreno” favorevole per future colonie polmonari.
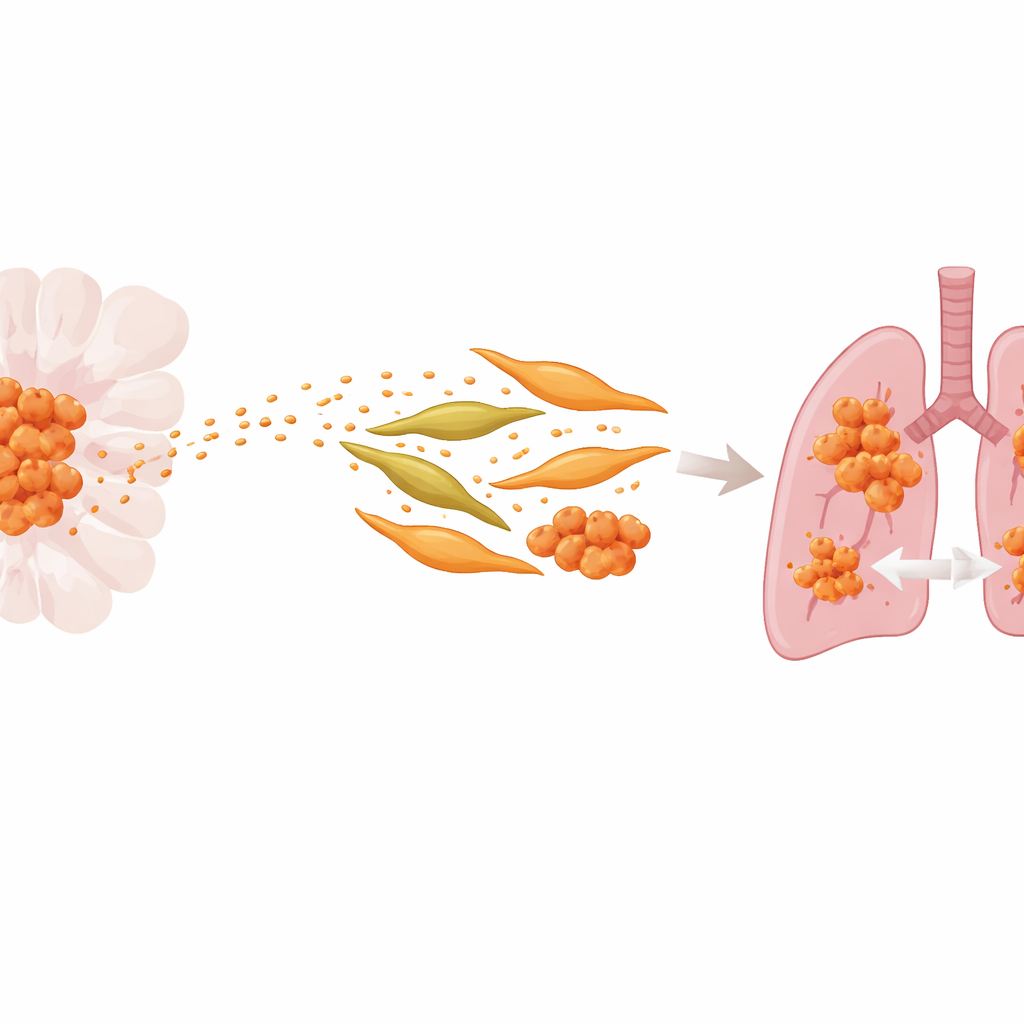
Piccoli pacchetti con grande impatto
I ricercatori si sono concentrati sugli esosomi, piccole vescicole delimitate da membrana che le cellule cancerose rilasciano nel flusso sanguigno. Queste vescicole trasportano proteine e materiale genetico in grado di riprogrammare cellule a distanza. Confrontando una linea cellulare ACC standard con una versione selezionata per una spiccata capacità di metastatizzare ai polmoni, il gruppo ha rilevato che sia le cellule aggressive sia i loro esosomi erano arricchiti in una proteina chiamata S100A9, collegata all’infiammazione. I pazienti i cui tumori e esosomi circolanti contenevano più S100A9 avevano maggior probabilità di sviluppare metastasi polmonari e periodi liberi da malattia più brevi, suggerendo che questa proteina favorisca la diffusione del cancro.
Rimodellare la squadra di supporto del tumore
Usando il sequenziamento dell’RNA a singola cellula, gli autori hanno costruito una mappa dettagliata dei tipi cellulari presenti nei tumori ACC e nelle ghiandole normali vicine. Hanno scoperto un’intensa comunicazione tra le cellule epiteliali tumorali e i fibroblasti circostanti, le cellule strutturali che producono tessuto connettivo. Nel contesto tumorale, questi fibroblasti possono essere “reclutati” e trasformati in fibroblasti associati al tumore (CAF), che irrigidiscono il tessuto, alimentano l’infiammazione e facilitano la migrazione delle cellule tumorali. Lo studio ha mostrato che esosomi ricchi di S100A9 provenienti da cellule ACC aggressive possono convertire fibroblasti normali in CAF attivati: diventano più contrattili, più mobili e iniziano a produrre enzimi e molecole infiammatorie che rimodellano la matrice e favoriscono la crescita tumorale.
Da segnali locali a colonie polmonari
Il gruppo ha quindi verificato se questi fibroblasti attivati dagli esosomi rendessero effettivamente più agevole la colonizzazione polmonare da parte dell’ACC. In modelli murini, l’iniezione di esosomi carichi di S100A9 nel circolo ha preparato i polmoni: i fibroblasti polmonari hanno attivato marcatori di attivazione e il tessuto ha iniziato a esprimere fattori associati alla neoangiogenesi e alla degradazione della matrice. Quando le cellule ACC sono state successivamente introdotte, i topi pretrattati con esosomi S100A9 hanno sviluppato più metastasi polmonari e di dimensioni maggiori. Analisi ulteriori hanno mostrato che questo processo dipendeva da una catena di segnali infiammatori centrata sul mediatore IL‑17, insieme a TNF e NF‑κB, che amplificano l’attivazione dei fibroblasti e rimodellano il microambiente polmonare.
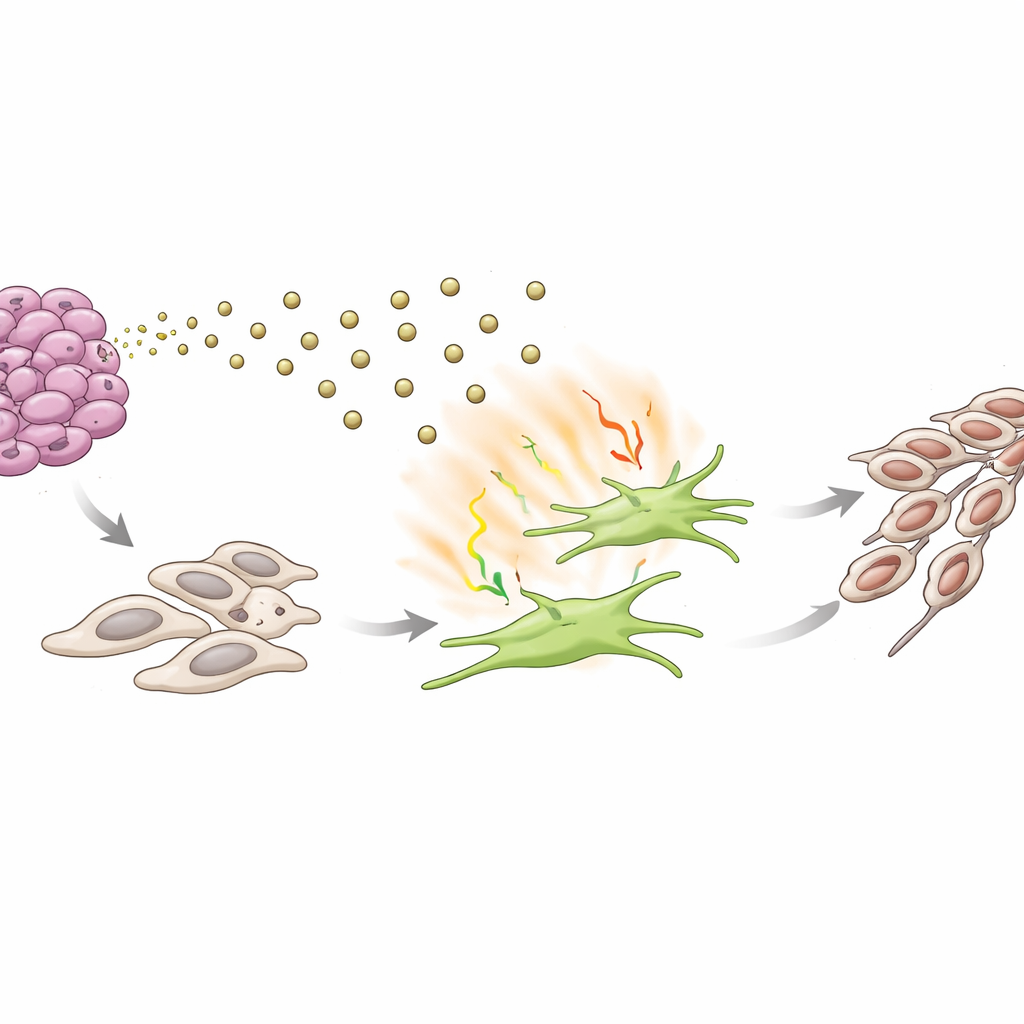
Un circolo vizioso che guida la trasformazione tumorale
In sistemi di co‑coltura in vitro, i fibroblasti “educati” da esosomi ricchi di S100A9, o da questa via di segnalazione guidata da IL‑17, rendevano le cellule ACC vicine più aggressive. Le cellule tumorali miglioravano migrazione, invasione attraverso barriere, crescita in colonie e assumevano una morfologia più mobile e allungata associata a una transizione epitelio‑mesenchimale, un passaggio chiave verso la metastasi. Il blocco di IL‑17 con un anticorpo neutralizzante ha invertito molte di queste modifiche, mentre l’aggiunta di IL‑17 purificato da sola ha spinto le cellule ACC verso uno stato più invasivo. Complessivamente, questi risultati delineano un circuito autoregolante: le cellule tumorali inviano S100A9 negli esosomi per attivare i fibroblasti; i fibroblasti attivati rilasciano IL‑17 e altri segnali che a loro volta rendono le cellule tumorali più propense a disseminarsi.
Interrompere il loop di comunicazione nascosto
Per il pubblico generale, il messaggio è che l’ACC non metastatizza ai polmoni per caso. Il tumore primario addestra segretamente le cellule di supporto e i tessuti distanti per favorirne la crescita altrove, usando piccoli pacchetti proteici come messaggeri. Questo lavoro identifica S100A9 e la via di segnalazione a valle mediata da IL‑17 come nodi centrali di questo processo. Colpendo quest’asse di comunicazione — bloccando S100A9, attenuando la segnalazione di IL‑17 o interferendo con l’attivazione dei fibroblasti — terapie future potrebbero interrompere la «fase di preparazione» delle metastasi polmonari, offrendo agli clinician nuovi modi per impedire che questo cancro silenzioso e pericoloso si ripresenti lontano dal sito di origine.
Citazione: Chen, Cw., Zhang, Sr., Yan, Ym. et al. Exosomal S100A9 promotes lung metastasis of adenoid cystic carcinoma via activating cancer-associated fibroblasts. Cell Death Discov. 12, 120 (2026). https://doi.org/10.1038/s41420-026-02991-6
Parole chiave: carcinoma adenoido‑cistico, esosomi, fibroblasti associati al tumore, metastasi polmonari, asse S100A9 IL-17