Clear Sky Science · it
Transizione endoteliale-mesenchimale mediata da APOA2 e riprogrammazione del metabolismo lipidico nel cancro conferiscono resistenza agli antiangiogenici tramite TGF-β
Perché questa scoperta è importante per i pazienti
I medici ricorrono sempre più spesso a farmaci che privano i tumori del fegato del loro apporto ematico, ma molti pazienti vedono la risposta svanire dopo un beneficio iniziale. Questo studio affronta una domanda urgente: perché alcuni tumori epatici diventano resistenti a questi trattamenti che bloccano i vasi sanguigni e come potremmo aggirarli? I ricercatori rivelano una collaborazione finora nascosta tra una proteina del sangue che trasporta i lipidi e un potente segnale di crescita, che permette ai tumori di riconfigurare sia i propri vasi sia il loro uso energetico, indicando una via alternativa per trattare un cancro difficile da curare.
Un tumore che impara a vivere senza la sua fonte di sostentamento abituale
Il carcinoma epatocellulare, la forma più comune di cancro del fegato, dipende fortemente dalla formazione di nuovi vasi per crescere. I farmaci standard per le malattie avanzate sono progettati per bloccare una via chiave della crescita vascolare centrata su VEGF e sul suo recettore VEGFR2. Eppure in molti pazienti i tumori continuano a prosperare nonostante questi medicinali. Confrontando campioni tumorali di pazienti che hanno risposto o meno all’antiangiogenico apatinib, gli autori hanno individuato un gene, APOA2, come particolarmente rilevante. I tumori dei pazienti resistenti presentavano livelli marcatamente più alti di APOA2, una proteina nota soprattutto per il suo ruolo nel trasporto dei grassi nel sangue. Ciò ha suggerito che APOA2 potrebbe aiutare i tumori a eludere i farmaci mirati ai vasi.
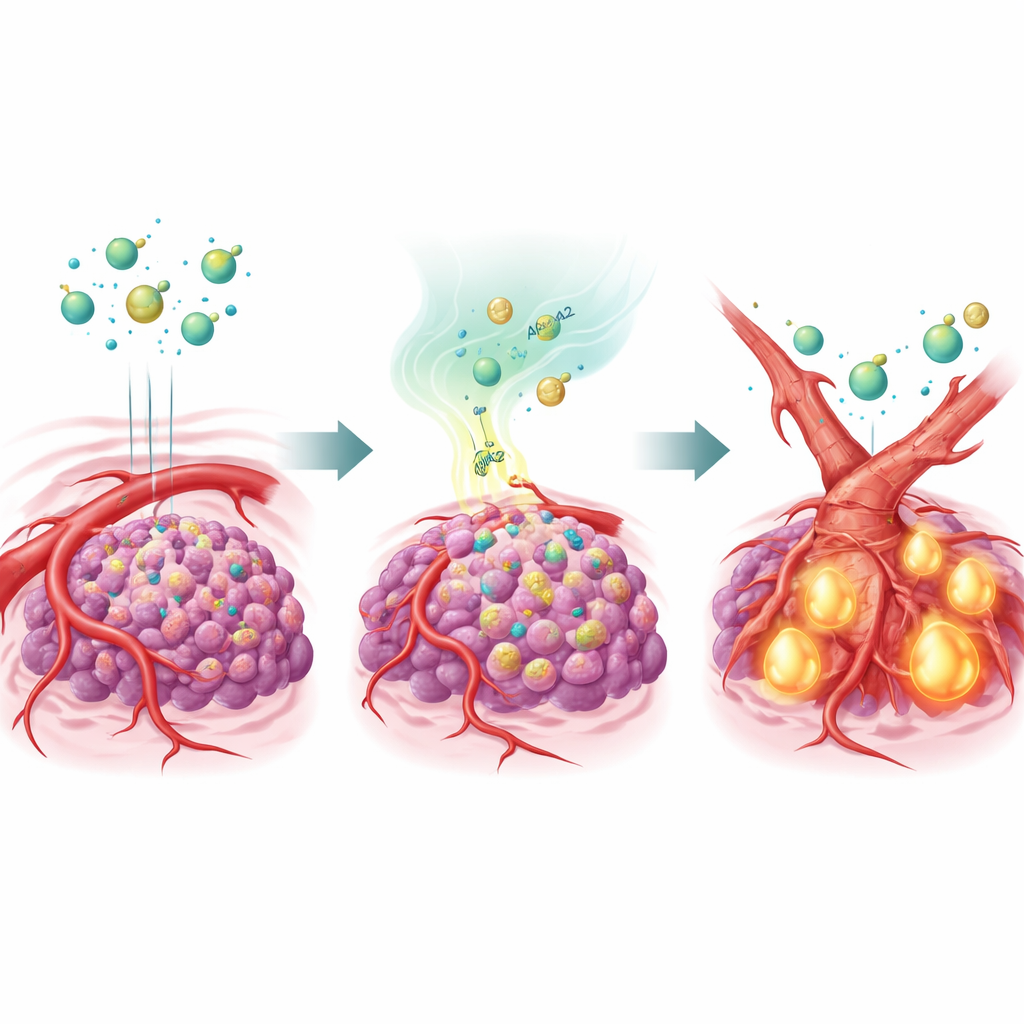
Una proteina di trasporto dei grassi che rimodella i vasi
Per verificare questa ipotesi, il team ha ingegnerizzato cellule di carcinoma epatico per sovraesprimere APOA2 e le ha impiantate in topo. Trattati con diversi antiangiogenici, questi tumori ricchi di APOA2 sono rimasti in gran parte indifferenti alla terapia: i loro vasi persistevano e i tumori continuavano a crescere. Un’analisi dettagliata ha mostrato che un segnale maestro chiamato TGF-β era fortemente attivato in questi tumori, con livelli elevati sia nell’ambiente tumorale sia nel sangue degli animali. TGF-β agiva sulle cellule che rivestono i vasi sanguigni, inducendole a cambiare identità in un processo chiamato transizione endoteliale-mesenchimale. Muovendosi verso uno stato più simile a tessuto cicatriziale, queste cellule perdevano gran parte di VEGFR2, proprio il bersaglio su cui si concentrano gli antiangiogenici. Di fatto, i vasi si rimodellavano in una forma che i farmaci non potevano più colpire.
Una deviazione metabolica che mantiene il carburante dei tumori
La storia non si fermava alla parete vascolare. Lo stesso segnale TGF-β promosso da APOA2 ha anche riprogrammato il modo in cui le cellule tumorali si approvvigionano di energia. Invece di dipendere principalmente dalla degradazione degli zuccheri, le cellule ad alto contenuto di APOA2 hanno iniziato a captare più acidi grassi liberi dall’ambiente e a ossidarli nei mitocondri tramite la beta-ossidazione. Esperimenti che misuravano l’uso di nutrienti e il consumo di ossigeno hanno mostrato che queste cellule divennero più dipendenti dai lipidi come fonte energetica e produssero più ATP. Questo cambiamento ha permesso alle cellule tumorali di continuare a dividersi rapidamente ed evitare la morte cellulare, anche quando l’apporto ematico era compromesso dal trattamento antiangiogenico.
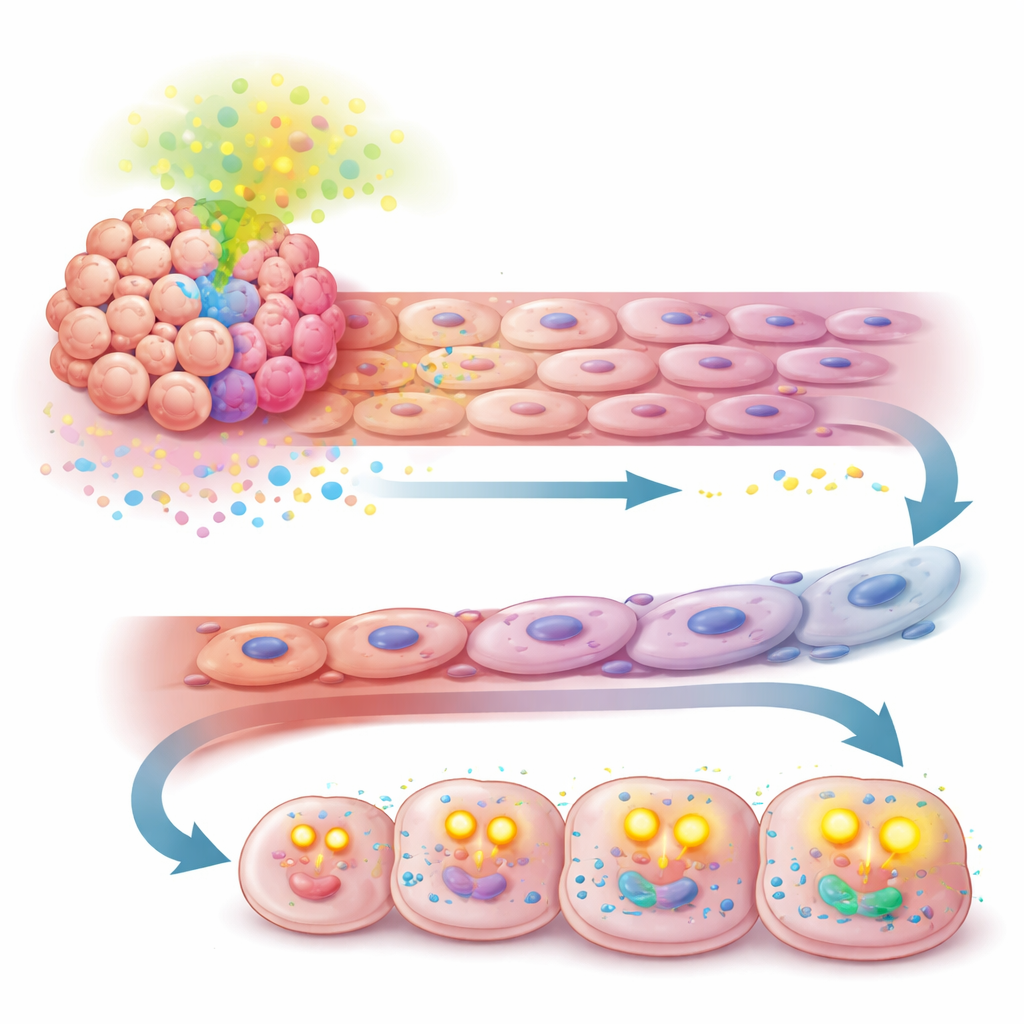
Trasformare una debolezza in un nuovo bersaglio terapeutico
In modo cruciale, quando i ricercatori bloccarono TGF-β, i vantaggi conferiti da APOA2 vennero meno. Inibire questo segnale nei modelli murini ridusse i cambiamenti vascolari anomali, ripristinò la sensibilità alla terapia e rallentò la crescita tumorale. Ancora più promettente, un anticorpo bifunzionale che blocca simultaneamente TGF-β e il checkpoint immunitario PD-1 ha funzionato meglio di ciascun approccio da solo nei tumori con alto APOA2. Questi risultati suggeriscono che, in un sottogruppo di carcinomi epatocellulari caratterizzati da elevata espressione di APOA2, la malattia ha silenziosamente spostato la sua dipendenza dalla via VEGF verso un percorso centrato su TGF-β che sostiene sia i vasi sia il metabolismo tumorale.
Cosa significa per la cura futura del cancro del fegato
Per il lettore non specialista, il messaggio chiave è che alcuni tumori del fegato sfuggono ai farmaci attuali che colpiscono i vasi riscrivendo sia la loro “plumbing” sia la loro fonte di energia. Una proteina associata ai grassi, APOA2, amplifica il segnale TGF-β, che a sua volta camuffa i vasi in modo che i farmaci esistenti non li riconoscano e insegna alle cellule tumorali a vivere di grassi anziché di zuccheri. Lo studio suggerisce che testare i tumori per APOA2 potrebbe identificare i pazienti meno propensi a beneficiare degli antiangiogenici standard ma più suscettibili a farmaci che bloccano TGF-β, specialmente in combinazione con immunoterapie moderne. In breve, mettendo in luce come i tumori si adattano, questo lavoro indica una strategia più mirata che attacca sia i vasi sia la fonte energetica su cui questi tumori resilienti fanno affidamento.
Citazione: Zhang, S., Fu, Z., Zhu, F. et al. APOA2-mediated endothelial mesenchymal transition and cancer lipid metabolism reprogramming confers antiangiogenic drug resistance through TGF-β. Cell Death Discov. 12, 119 (2026). https://doi.org/10.1038/s41420-026-02984-5
Parole chiave: carcinoma epatocellulare, resistenza agli antiangiogenici, APOA2, segnalazione TGF-beta, metabolismo lipidico del cancro