Clear Sky Science · it
KCTD1 stabilizza c-Myc per upregolare PD-L1 e sopprimere l’immunità anti-tumorale nell’epatocarcinoma
Perché è importante per la cura del cancro in futuro
Molte persone affette da tumore al fegato non traggono beneficio dalle attuali immunoterapie più promettenti, progettate per liberare le cellule T del paziente contro i tumori. Questo studio indaga perché una forma principale di cancro del fegato, il carcinoma epatocellulare, può ancora eludere l’attacco immunitario anche durante il trattamento — e identifica un nuovo interruttore molecolare, chiamato KCTD1, che potrebbe rendere più efficaci i farmaci immunoterapici esistenti.
Un aiutante nascosto degli “interruttori” tumorali
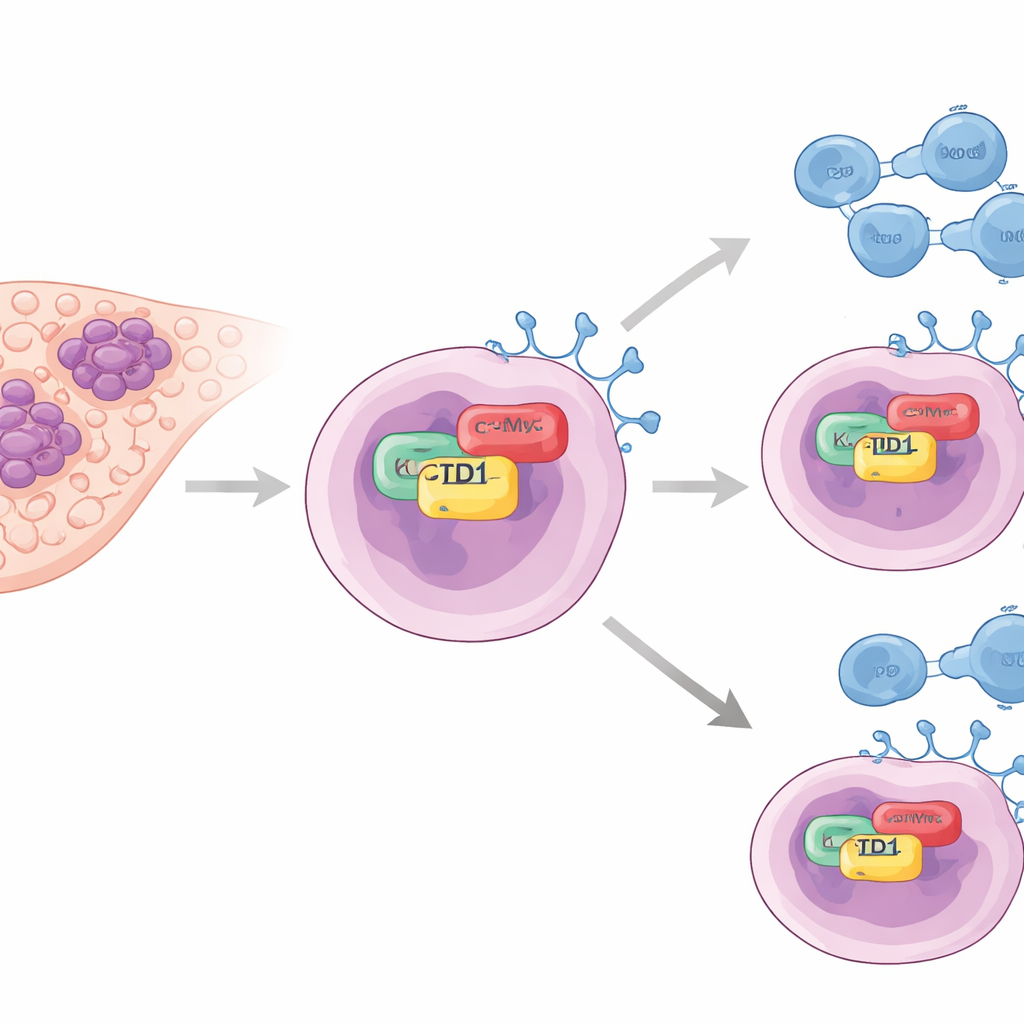
Gli autori si sono concentrati su una proteina chiamata KCTD1, precedentemente collegata alla crescita dei tumori epatici ma non approfondita nello studio dell’elusione immunitaria. Nei campioni tumorali dei pazienti hanno rilevato che i livelli di KCTD1 erano marcatamente più alti nel tessuto epatico canceroso rispetto al fegato normale. È importante che i tumori ricchi di KCTD1 mostravano anche alti livelli di PD-L1, una proteina di superficie delle cellule tumorali che si lega a PD-1 sulle cellule T e di fatto dice al sistema immunitario di arrestare l’attacco. I pazienti i cui tumori presentavano livelli più bassi di KCTD1 tendevano a vivere più a lungo, suggerendo che questa proteina è collegata alla gravità della malattia e alla forza dello scudo immunitario tumorale.
Collegare i punti molecolari all’interno delle cellule tumorali
Per capire come KCTD1 aumenti PD-L1, il team ha utilizzato linee cellulari di carcinoma epatocellulare coltivate in laboratorio. Quando hanno ridotto KCTD1, i livelli della proteina PD-L1 sono diminuiti e la PD-L1 rimasta è stata degradată più rapidamente, indicando che KCTD1 aiuta a stabilizzare PD-L1 piuttosto che limitarsi ad attivare il suo gene. Mediante esperimenti biochimici di pull-down e microscopia a fluorescenza, hanno dimostrato che KCTD1 si lega fisicamente a un altro fattore chiave del cancro, l’oncoproteina c-Myc, all’interno del nucleo cellulare. Questa interazione avviene attraverso regioni di contatto specifiche su entrambe le proteine e porta a una maggiore stabilità di c-Myc, che a sua volta potenzia la produzione di PD-L1. Quando c-Myc è stato ridotto da solo, PD-L1 è diminuita anche se KCTD1 era abbondante, collocando c-Myc come l’anello centrale cruciale nella catena KCTD1–c-Myc–PD-L1.
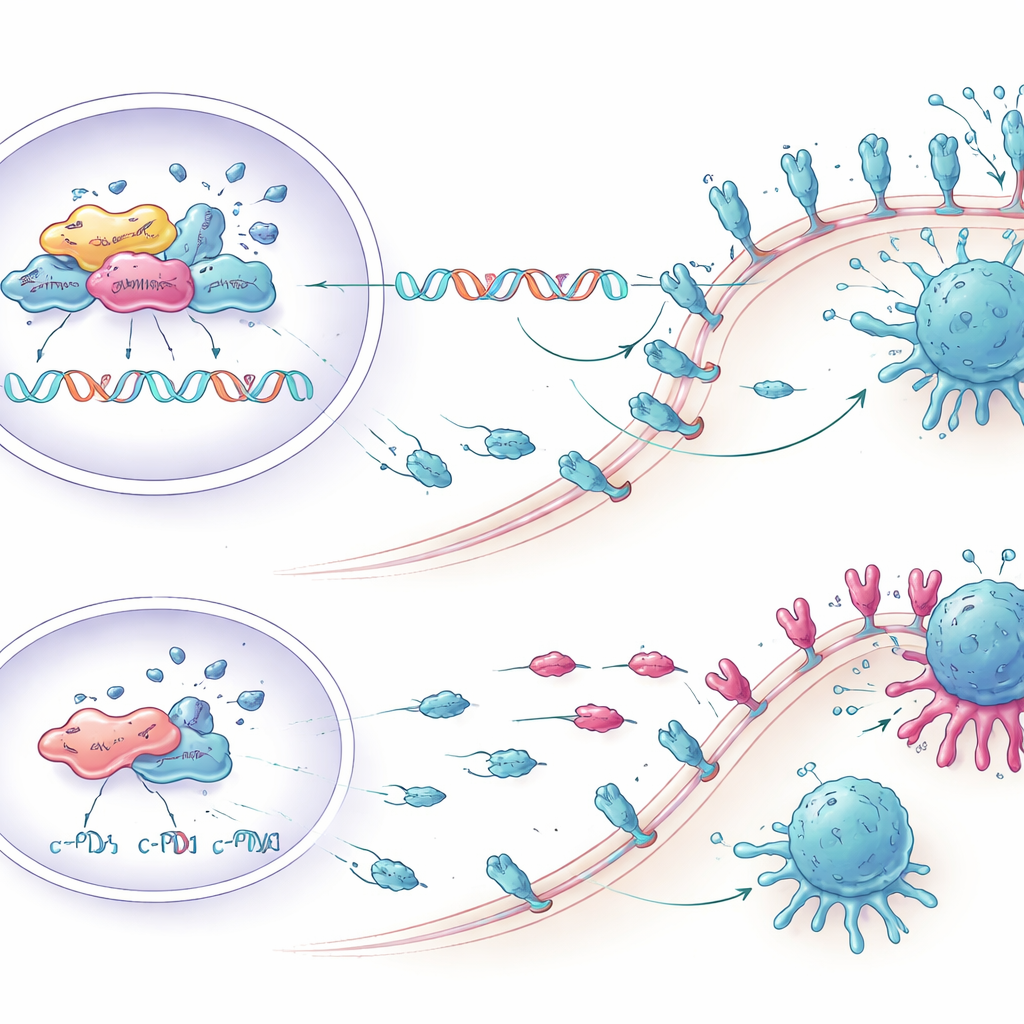
Ririscattare le cellule T in laboratorio
I ricercatori si sono poi chiesti se abbassare KCTD1 potesse effettivamente rafforzare l’attacco immunitario. Hanno co-coltivato cellule di carcinoma epatico umano con cellule immunitarie prelevate da donatori di sangue. Le cellule tumorali ingegnerizzate per esprimere meno KCTD1, e quindi meno PD-L1, hanno indotto risposte più forti da parte delle cellule T CD8 — i principali agenti uccisori del sistema immunitario contro le cellule tumorali. Più cellule T hanno prodotto molecole infiammatorie come TNF-α e interferone-gamma, hanno mostrato marcatori più elevati di proliferazione e attivazione e hanno presentato meno segni di esaurimento. Di conseguenza, un maggior numero di cellule tumorali ha subito morte cellulare programmata quando KCTD1 è stato soppresso, dimostrando che i cambiamenti molecolari si traducevano in reali guadagni nell’eliminazione immunitaria.
Mettere alla prova il meccanismo nei topi
Per verificare se lo stesso schema vale negli organismi viventi, il team ha impiantato cellule di carcinoma epatico murino prive di KCTD1 direttamente nei fegati dei topi. I tumori con KCTD1 ridotto hanno formato noduli meno numerosi e più piccoli, hanno mostrato una divisione cellulare più lenta e hanno avuto più cellule tumorali in apoptosi. Questi tumori esprimevano anche meno c-Myc e PD-L1. La rimozione delle cellule T CD8 nei topi ha annullato gran parte di questo vantaggio, indicando che il rallentamento tumorale dipendeva in larga misura dall’attività delle cellule T. Infine, quando i ricercatori hanno combinato il silenziamento di KCTD1 con un anticorpo anti–PD-1 — un farmaco già esistente contro i checkpoint immunitari — i topi hanno mostrato il carico tumorale più basso e i livelli più alti di infiltrazione di cellule T CD4 e CD8 nei loro tumori.
Cosa potrebbe significare per i pazienti
Nel complesso, il lavoro rivela KCTD1 come un coordinatore centrale che stabilizza c-Myc, aumenta PD-L1 sulle cellule del carcinoma epatocellulare e attenua l’attacco delle cellule T CD8. Disgregare questa via rende i tumori sia più vulnerabili al sistema immunitario sia più sensibili ai farmaci che bloccano PD-1 nei topi. Per i pazienti, ciò suggerisce che farmaci mirati a KCTD1 o alla sua superficie di contatto con c-Myc potrebbero, in futuro, essere associati alle immunoterapie attuali per permettere a più persone affette da carcinoma epatocellulare di beneficiare di un controllo immunitario duraturo della malattia.
Citazione: Zhong, D., Long, S., Dai, Y. et al. KCTD1 stabilizes c-Myc to upregulate PD-L1 and suppress anti-tumor immunity in hepatocellular carcinoma. Cell Death Discov. 12, 129 (2026). https://doi.org/10.1038/s41420-026-02975-6
Parole chiave: carcinoma epatocellulare, immunoterapia tumorale, via PD-1 PD-L1, segnalizzazione c-Myc, immunità T cellulare anti-tumorale