Clear Sky Science · it
Multi-omica rivela eterogeneità e popolazioni funzionali di cellule progenitrici oligodendrocitarie indotte da cellule staminali neurali umane
Perché proteggere l’isolamento del cervello è importante
Il cablaggio del nostro cervello dipende da un rivestimento grasso chiamato mielina, che avvolge le fibre nervose come l’isolamento dei cavi elettrici. Quando la mielina viene danneggiata, come nella sclerosi multipla e in altri disturbi, i segnali rallentano o si perdono, causando problemi di movimento, vista e ragionamento. Questo studio esplora un gruppo speciale di cellule umane in grado di ricostruire la mielina e pone una domanda pratica: quali cellule sono più adatte per future terapie cellulari volte a riparare questo isolamento cruciale?
Dalle cellule neurali di partenza ai costruttori di mielina
I ricercatori hanno iniziato con cellule staminali neurali umane—cellule di partenza versatili ottenute da tessuto fetale cerebrale già indirizzate a diventare cellule del sistema nervoso. In laboratorio hanno indotto queste staminali a trasformarsi in cellule progenitrici oligodendrocitarie, o hOPC, che sono i precursori diretti delle cellule produttrici di mielina. Al microscopio le cellule sono passate da forme rotonde e semplici a morfologie più complesse con molte ramificazioni e hanno attivato proteine caratteristiche che segnano i passaggi verso cellule mature produttrici di mielina. Questo ha fornito una fonte affidabile e relativamente sicura di precursori umani per un’analisi dettagliata.
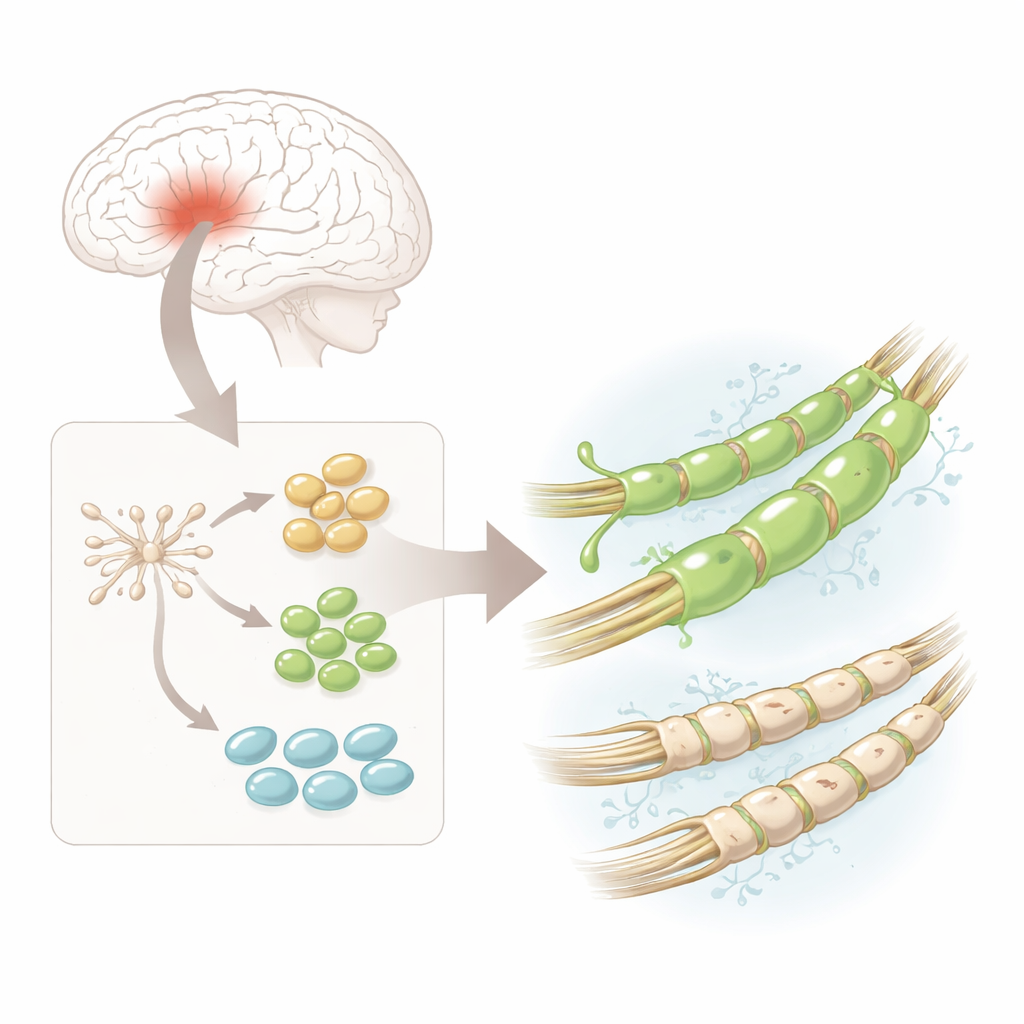
Un tipo cellulare, molte varietà nascoste
Utilizzando il sequenziamento RNA a singola cellula—un approccio che legge quali geni sono attivi in migliaia di singole cellule—il gruppo ha scoperto che gli hOPC non erano tutti uguali. Si sono infatti raggruppati in tre stadi principali: «pre-progenitori» precoci, progenitori più impegnati e cellule prossime a un’identità oligodendrocitaria completa. In tutti questi stadi è emerso un gene in particolare: PDGFRA, che codifica un recettore di membrana. Un metodo di imaging ad alta sensibilità chiamato RNA-Scope ha confermato che l’RNA messaggero e la proteina di PDGFRA erano più abbondanti rispetto ad altri marcatori chiave in ogni stadio, suggerendo che questo recettore potrebbe definire cellule particolarmente capaci di costruire mielina.
Selezionare le cellule di riparazione più potenti
Per mettere alla prova questa idea, gli scienziati hanno separato gli hOPC in due gruppi in base alla presenza del recettore PDGFR-α sulla superficie. Hanno poi confrontato cellule PDGFR-α–positive, PDGFR-α–negative e cellule non selezionate in una serie di test funzionali. Trapiantate in topi «shiverer»—che non possono formare mielina normale—le cellule PDGFR-α–positive hanno prodotto una mielina più densa e compatta attorno alle fibre nervose rispetto agli altri gruppi. Queste cellule hanno inoltre migrato più lontano e si sono moltiplicate più rapidamente in saggi di laboratorio. In altre parole, la popolazione PDGFR-α–positiva è risultata la più vigorosa nel raggiungere il sito di bisogno, aumentare di numero e ricostruire l’isolamento.
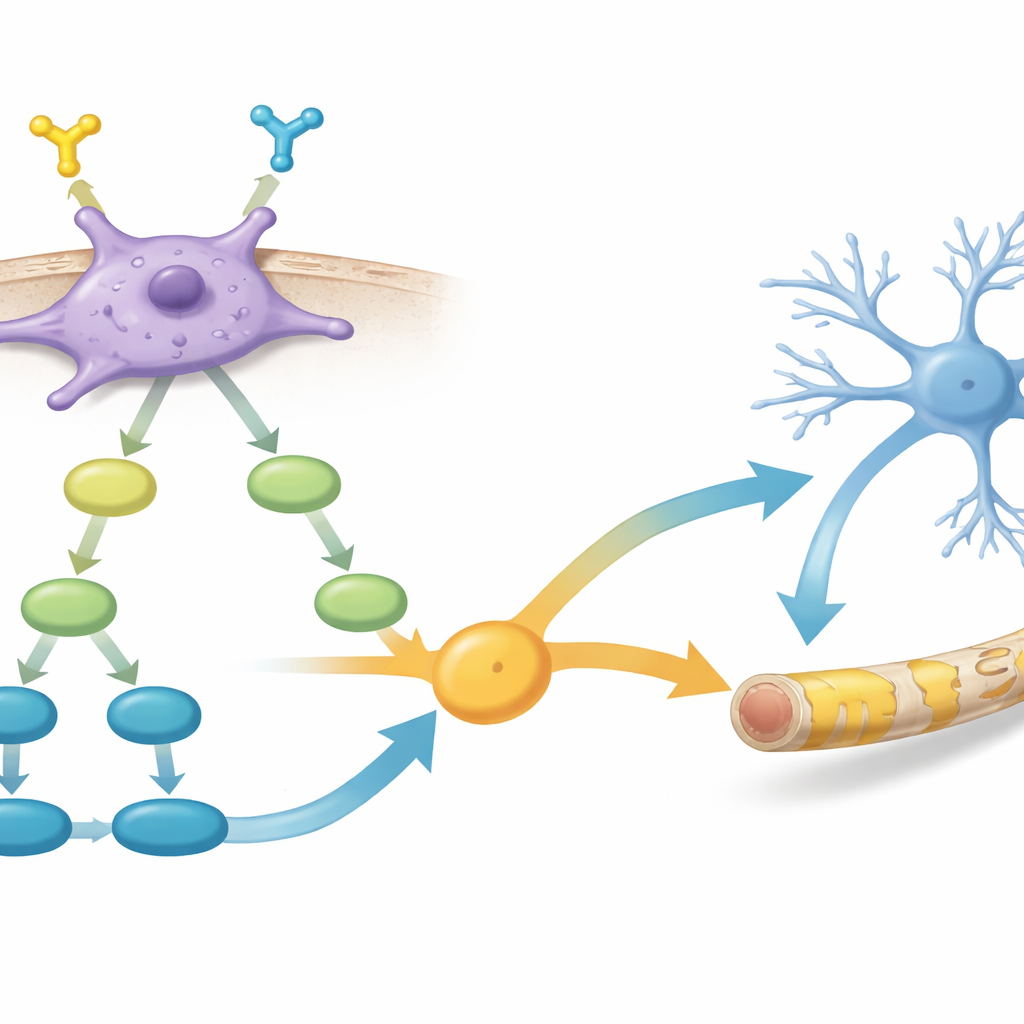
Segnali interni che guidano crescita e riparazione
Approfondendo, il team ha confrontato l’attività genica tra cellule PDGFR-α–positive e –negative. Hanno osservato che le cellule positive attivano reti di geni coinvolte nella crescita delle cellule gliali e nella formazione della mielina, oltre a diverse vie di segnalazione intracellulari chiave. Due percorsi in particolare risaltano: PI3K–AKT–mTOR, da tempo collegato alla crescita cellulare e alla produzione di mielina, e la segnalazione TGF-β, che influenza come le cellule cerebrali giovani scelgono il proprio destino. I dati suggeriscono che l’attivazione di PDGFR-α alimenta PI3K–AKT–mTOR, che a sua volta potenzia i segnali correlati a TGF-β, spingendo insieme le cellule verso l’essere efficaci costruttrici di mielina.
Potenziare la riparazione della mielina con un aiuto chimico
I ricercatori hanno quindi verificato se fosse possibile migliorare ulteriormente queste cellule promettenti. Hanno trattato gli hOPC PDGFR-α–positivi con una piccola molecola che attiva la via TGF-β ed esaminato sia l’attività genica sia il comportamento cellulare. Dopo il trattamento, queste cellule hanno mostrato livelli più alti di diversi geni correlati alla mielina e hanno prodotto guaine mieliniche più spesse e complete quando trapiantate nei topi shiverer, rispetto alle cellule PDGFR-α–positive non trattate. Ciò supporta l’idea che modulare con cura la segnalazione interna in progenitori già ben selezionati può migliorare ulteriormente le loro prestazioni come strumenti viventi per la riparazione della mielina.
Cosa significa per i trattamenti futuri
Per i non specialisti, il messaggio centrale è che non tutti i precursori costruttori di mielina sono uguali. Combinando potenti strumenti di lettura genica e imaging, questo studio identifica un sottogruppo di spicco—hOPC PDGFR-α–positivi—that migrano meglio, si dividono di più e ricostruiscono la mielina in modo più efficace rispetto ai loro pari. Mettere in evidenza anche le vie di segnalazione interne che possono essere chimicamente modulati rende possibile rendere queste cellule ancora più potenti. Questi risultati insieme tracciano una mappa per progettare terapie cellulari più sicure ed efficienti per ripristinare l’isolamento del cervello nelle malattie caratterizzate dalla perdita di mielina.
Citazione: Ye, D., Zhou, H., Qu, S. et al. Multi-omics reveals heterogeneity and functional populations of oligodendrocyte progenitor cells induced by human neural stem cells. Cell Death Discov. 12, 112 (2026). https://doi.org/10.1038/s41420-026-02971-w
Parole chiave: riparazione della mielina, cellule progenitrici oligodendrocitarie, cellule staminali neurali, terapia cellulare, sequenziamento RNA a singola cellula