Clear Sky Science · it
Axin1 stabilizza la S-opsina e mantiene la sopravvivenza dei fotorecettori conici inibendo l'attività di GSK3β
Mantenere viva la nostra visione dei colori
Ogni volta che entriamo alla luce del sole o volgiamo lo sguardo verso uno schermo luminoso, minuscole cellule nei nostri occhi lavorano intensamente per trasformare la luce in visione. Queste cellule, chiamate fotorecettori, sono fragili e possono morire lentamente in molte malattie che portano alla cecità. Questo studio svela come una proteina “organizzatrice” poco conosciuta, Axin1, aiuti a proteggere i fotorecettori conici — le cellule che ci permettono la visione diurna e dei colori — mantenendo le molecole chiave per la fotodetection al posto giusto e attenuando pericolosi stress all’interno della cellula.
Come i coni vedono il mondo
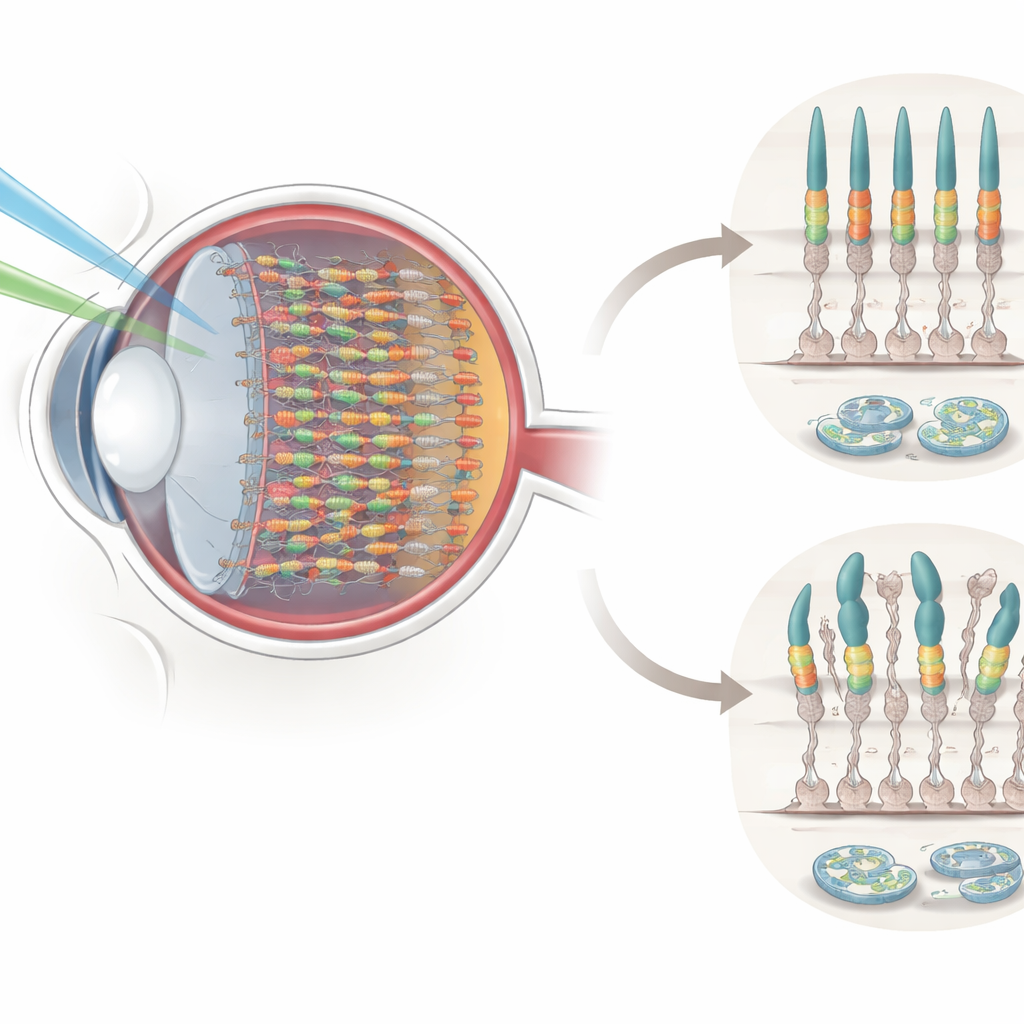
Le nostre retine contengono due principali tipi di fotorecettori: i bastoncelli per la visione scotopica in bianco e nero e i coni per la visione fotopica e a colori. I coni contengono pigmenti speciali, inclusa la S-opsina, particolarmente sensibile alla luce a lunghezza d’onda corta (blu). Questi pigmenti sono collocati in una regione stretta e impilata all’estremità di ogni fotorecettore chiamata segmento esterno, dove la luce entrante viene convertita in segnali elettrici. Poiché questa regione è costantemente bombardata dalla luce e deve rinnovarsi rapidamente, è particolarmente vulnerabile ai danni e allo stress nella “fabbrica” di ripiegamento proteico della cellula, il reticolo endoplasmatico (RE). Quando il RE è sovraccarico di proteine mal ripiegate o mal localizzate, può innescare il suicidio cellulare, contribuendo alla degenerazione retinica e alla perdita della vista.
Un organizzatore nascosto nelle cellule coniche
I ricercatori hanno rivolto la loro attenzione ad Axin1, una proteina impalcatura nota soprattutto per organizzare vie di segnalazione in altre parti del corpo. Tramite colorazioni ad alta risoluzione nella retina del topo, hanno rilevato che Axin1 non è distribuita in modo uniforme nell’occhio. Al contrario, è arricchita nei fotorecettori conici, in particolare nella retina ventrale (inferiore), proprio dove la S-opsina è più abbondante. All’interno di ogni cono, Axin1 si raggruppa nel segmento esterno, sovrapponendosi strettamente con la S-opsina. Nel corso dello sviluppo, Axin1 e S-opsina compaiono insieme, passando da piccoli punti a strutture allungate a forma di asta che caratterizzano i segmenti esterni conici maturi. Questo preciso accoppiamento spaziale e temporale suggeriva che Axin1 potesse essere cruciale per mantenere la S-opsina nella posizione corretta per una rilevazione efficiente della luce.
Cosa succede quando Axin1 viene persa
Per mettere alla prova l’importanza di Axin1, il gruppo ha rimosso selettivamente la proteina dalle cellule coniche nei topi usando un approccio virale di editing genetico. Questi animali privi di Axin1 mostrarono una lenta costrizione pupillare quando esposti a luce blu o verde e si comportarono in modo anomalo in un test di preferenza luce-buio, indicando una percezione della luce compromessa. Al microscopio, i loro segmenti esterni conici apparivano disorganizzati: i livelli di S-opsina calarono e, invece di formare strutture lisce a forma di asta, il pigmento si frammentò in puntini dispersi. Anche i tessuti retinici circostanti mostrarono prime segnali di danno. Le giunzioni strette nello strato pigmentato di supporto risultarono disturbate, i marcatori sinaptici tra i coni e i neuroni a valle diminuirono e le cellule gliali — normalmente cellule di supporto inattive — si attivarono: tutti segni tipici di una degenerazione retinica in corso.
Stress intracellulare e un interruttore pericoloso
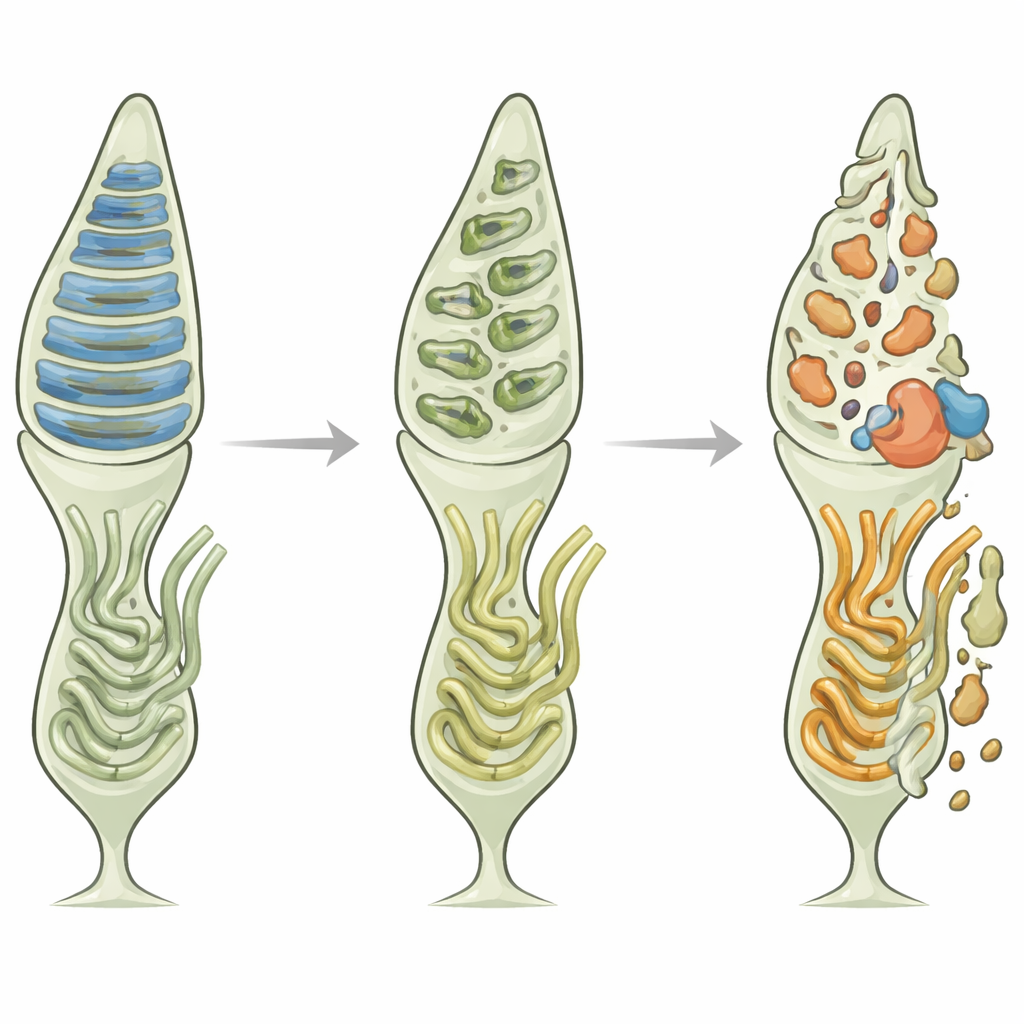
L’assenza di Axin1 non alterò solo la struttura; intensificò anche lo stress biochimico. Nelle retine di topo prive di Axin1, marcatori di stress del RE, come la proteina CHOP, risultarono fortemente elevati negli strati dei fotorecettori. In cellule 661W derivate dai coni in coltura, la riduzione di Axin1 rese l’esposizione alla luce blu e un induttore chimico di stress del RE, la tunicamicina, molto più tossica, innalzando l’espressione di geni dello stress del RE e il numero di cellule in apoptosis. Lo studio collegò questa vulnerabilità a un enzima chiave, GSK3β, che diventa più attivo quando i livelli di Axin1 calano. GSK3β iperattivato spinse le cellule verso maggiore stress del RE e morte. Al contrario, stabilizzare Axin1 con una piccola molecola, o inibire direttamente GSK3β con cloruro di litio, ridusse i marcatori di stress, calmò l’attività di GSK3β e salvò molte cellule dall’apoptosi.
Trasformare la protezione in terapia
Nel loro complesso, i risultati dipingono Axin1 come un guardiano centrale dei fotorecettori conici. Ancorando la S-opsina nella posizione corretta nel segmento esterno e trattenendo l’enzima promotore di stress GSK3β, Axin1 aiuta i coni a far fronte alla continua esposizione a luce intensa e a lunghezza d’onda corta. Quando Axin1 manca o è instabile, la S-opsina si dislocalizza, il RE si ritrova sovraccarico di proteine problematiche, le vie di stress si accendono e i coni vengono spinti verso la degenerazione. Poiché molte patologie umane che causano cecità implicano la perdita dei coni e la morte cellulare guidata dallo stress del RE, strategie che potenzino o imitino la funzione di Axin1 — o che modulino in modo sicuro l’attività di GSK3β — potrebbero offrire nuove vie per rallentare o prevenire la degenerazione retinica e preservare la nostra visione diurna e dei colori.
Citazione: Xu, J., Man, J., Fan, Y. et al. Axin1 stabilizes S-opsin and maintains cone photoreceptor survival by inhibiting GSK3β activity. Cell Death Discov. 12, 109 (2026). https://doi.org/10.1038/s41420-026-02968-5
Parole chiave: degenerazione retinica, fotorecettori conici, stress del reticolo endoplasmatico, Axin1, GSK3 beta