Clear Sky Science · it
La crosstalk tra bioenergetica mitocondriale e SASP determina l’efficacia senolitica nella senescenza indotta da terapia
Perché eliminare le cellule tumorali “zombie” è così difficile
Molti farmaci oncologici moderni non uccidono direttamente tutte le cellule tumorali. Invece, alcune cellule entrano in uno stato liminale chiamato senescenza: smettono di dividersi ma restano vive, un po’ come cellule “zombie”. Queste cellule senescenti indotte dalla terapia possono essere utili all’inizio, ma se persistono possono favorire recidive, resistenza e effetti collaterali. Perciò gli scienziati stanno testando farmaci senolitici progettati per eliminare selettivamente le cellule senescenti. Questo lavoro pone una domanda apparentemente semplice: perché alcune cellule tumorali senescenti muoiono quando esposte ai senolitici, mentre altre resistono ostinatamente?
Centraline che ricordano il passato
Al centro dello studio ci sono i mitocondri, le piccole centrali energetiche dentro le cellule. Gli autori hanno esaminato se il modo in cui i mitocondri ossidano diversi combustibili — come zuccheri, grassi e amminoacidi — influenzi la sensibilità delle cellule tumorali senescenti ai senolitici che prendono di mira una proteina di sopravvivenza chiamata BCL‑xL. Utilizzando un saggio ad alto rendimento (MitoPlate S‑1), hanno tracciato funzionalmente l’attività mitocondriale in diverse linee cellulari tumorali prima e dopo che la senescenza fosse indotta da trattamenti differenti (farmaci che danneggiano il DNA, bloccanti della mitosi, stress ossidativo o inibitori del ciclo cellulare). Hanno scoperto che la senescenza indotta da terapia non produceva un singolo stato mitocondriale uniforme. Al contrario, ogni farmaco lasciava una «impronta bioenergetica» distinta, modificando quanto ampiamente e intensamente i mitocondri potessero attingere a varie fonti di energia. In modo cruciale, questa flessibilità si stratificava su una configurazione di base preesistente: la configurazione mitocondriale originale delle cellule parentali fissava un limite superiore — il «soffitto» — su quanto forte potesse essere una successiva risposta senolitica.
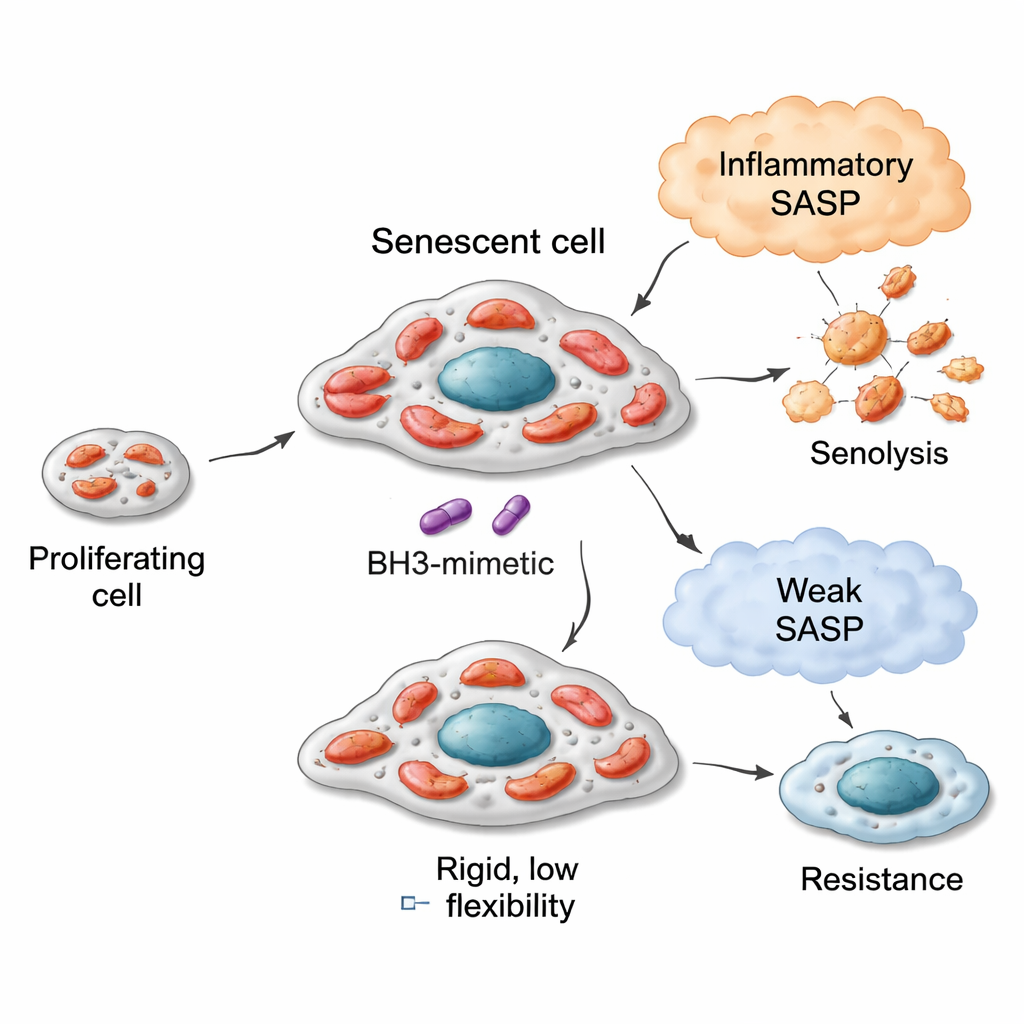
Motori flessibili, carburanti diversi e sensibilità ai senolitici
Nei modelli di cancro al polmone, al seno e al colon, le cellule senescenti con mitocondri più flessibili — in grado di ossidare una gamma più ampia di combustibili — tendevano a essere più vulnerabili ai senolitici diretti contro BCL‑xL come navitoclax (ABT‑263) e A1331852. Ad esempio, le cellule di cancro polmonare indotte alla senescenza dal farmaco bleomicina svilupparono mitocondri che utilizzavano vigorosamente molti substrati, in particolare quelli legati alla degradazione degli acidi grassi e ad alcune vie degli amminoacidi. Queste cellule erano altamente sensibili ai senolitici. Al contrario, le cellule spinte in senescenza da un inibitore di CDK4/6 (palbociclib) mostraronoun repertorio metabolico più ristretto e risposero poco agli stessi agenti senolitici. Tuttavia questa relazione aveva dei limiti: le cellule di cancro al seno potevano anch’esse diventare metabolicamente flessibili dopo la senescenza, ma poiché i loro mitocondri di partenza erano meno «preparati» all’apoptosi, la loro risposta senolitica massima era modesta. Le cellule di cancro del colon con macchinari apoptotici difettosi rimasero resistenti indipendentemente da come il loro metabolismo cambiasse. Una singola misura — quanto bene le cellule ossidavano il combustibile succinato al baseline — è risultata un indicatore semplice di questa capacità mitocondriale ereditata.
Quando il metabolismo parla con l’infiammazione
Le cellule senescenti sono famose per la SASP, un cocktail di fattori secretori infiammatori e di crescita che può influenzare i tessuti circostanti. Il gruppo ha indagato come il metabolismo mitocondriale si collega a questo comportamento secretorio usando cellule ingegnerizzate con un reporter per miR‑146a, un microRNA attivato dal master regolatore infiammatorio NF‑κB. Hanno scoperto che, mentre i profili SASP complessivi erano in gran parte dettati dal tipo cellulare, solo alcuni stati senescenti attivavano questo asse NF‑κB/miR‑146a. Questi erano gli stessi stati che rispondevano bene ai senolitici contro BCL‑xL. Importante, queste cellule senescenti «positive per SASP infiammatoria» mostravano anche un incremento nell’uso dell’ossidazione degli acidi grassi e un rialzo trascrizionale di geni che trasportano grassi a catena lunga nei mitocondri. Bloccare l’ingresso degli acidi grassi con il farmaco etomoxir attenuava l’attivazione di miR‑146a senza invertire completamente la senescenza, suggerendo che la scelta del combustibile mitocondriale contribuisce a consentire una SASP infiammatoria permissiva per i senolitici.
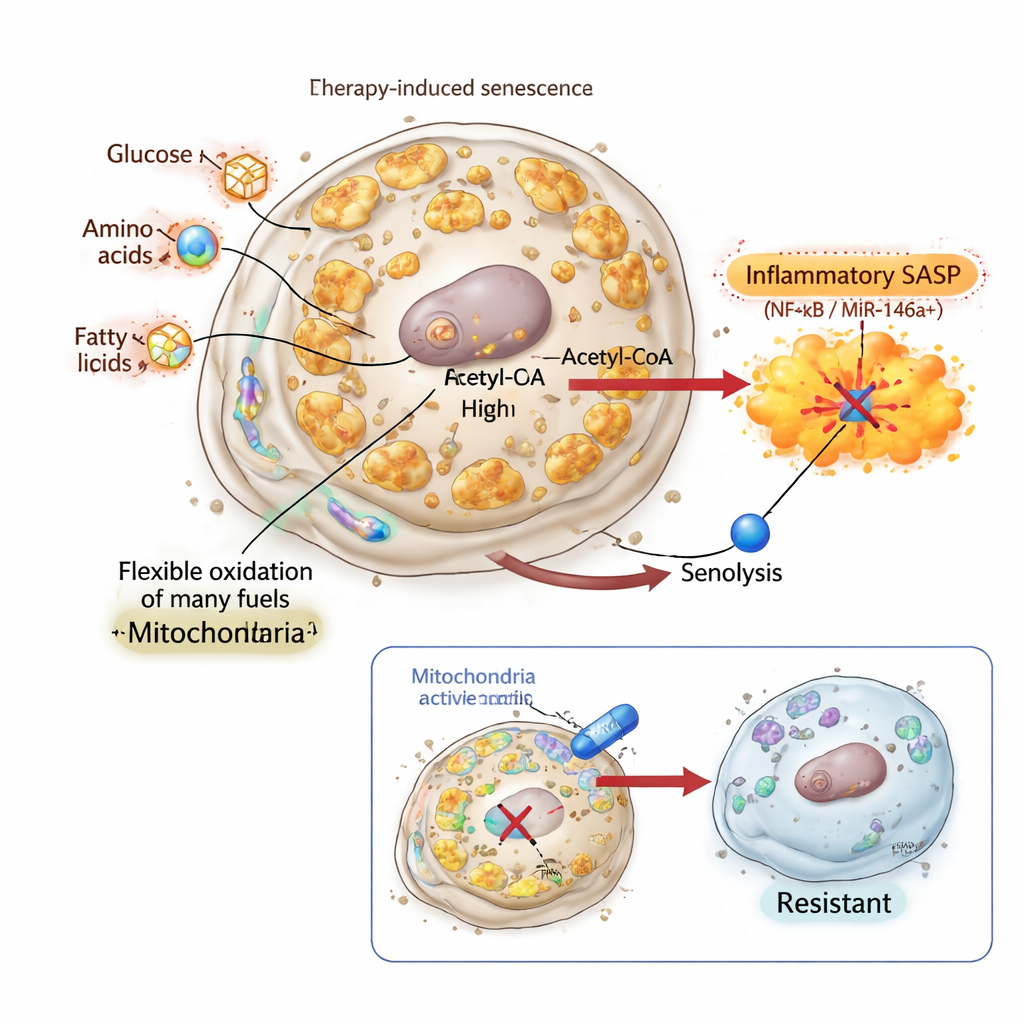
Spegnere il segnale e creare cellule senescenti impossibili da uccidere
Per testare se la SASP infiammatoria sia davvero necessaria per il kill senolitico, i ricercatori hanno usato l’inflachromene, un composto che si lega alle proteine della cromatina HMGB1 e HMGB2 e blocca il loro ruolo nell’attivare i geni SASP. Nelle cellule di cancro al polmone e al seno, l’inflachromene ha indotto un fenotipo senescente tipico: le cellule sono diventate grandi, hanno smesso di dividersi e hanno accumulato marcatori di senescenza. La loro massa mitocondriale e l’attività bioenergetica sono aumentate sostanzialmente e l’utilizzo dei carburanti è stato chiaramente rimodellato. Eppure la loro SASP era attenuata e il reporter di miR‑146a rimaneva sostanzialmente silente. Colpisce che queste cellule senescenti prive di SASP fossero completamente resistenti ai senolitici mirati a BCL‑xL, nonostante avessero mitocondri bioenergeticamente attivi e riprogrammati e una ridotta espressione del classico gene anti‑apoptotico BCL2. Ciò dimostra che i cambiamenti mitocondriali da soli non sono sufficienti; senza un’uscita infiammatoria guidata dai mitocondri, il «secondo colpo» senolitico fallisce.
Cosa significa per i futuri trattamenti contro il cancro
Per il lettore non specialistico, la conclusione dello studio è che eliminare le cellule tumorali “zombie” indotte dalla terapia è governato da un circuito stratificato. Primo, lo stato iniziale e il cablaggio dei mitocondri di una cellula tumorale determinano quanto lontano i senolitici possano arrivare. Secondo, il trattamento specifico che causa la senescenza può spingere il metabolismo mitocondriale verso maggiore o minore flessibilità, avvicinando o allontanando le cellule dal baratro dell’apoptosi. Terzo — e in modo decisivo — i senolitici funzionano bene solo se la riorganizzazione metabolica riesce ad attivare un programma SASP infiammatorio che comunica con il nucleo. Senza quel dialogo infiammatorio, le cellule senescenti possono diventare uno stato terminale resistente ai farmaci. Praticamente, questo suggerisce che le future terapie potrebbero essere ottimizzate testando funzionalmente sia la flessibilità mitocondriale sia l’infiammazione SASP nei tumori, quindi scegliendo combinazioni di farmaci che inducono senescenza e senolitici in modo da garantire che le cellule “zombie” non siano solo congelate, ma anche preparate per essere eliminate.
Citazione: Llop-Hernández, À., Verdura, S., López, J. et al. Mitochondrial bioenergetics-SASP crosstalk determines senolytic efficacy in therapy-induced senescence. Cell Death Discov. 12, 103 (2026). https://doi.org/10.1038/s41420-026-02967-6
Parole chiave: senescenza cellulare, mitocondri, senolitici, metabolismo del cancro, SASP infiammatoria