Clear Sky Science · it
La soppressione di SREBP1 induce ferroptosi sopprimendo l’asse Nrf2-XCT/GPX4 nel cancro ovarico
Rivoltare la fabbrica dei grassi del cancro contro se stessa
Il cancro ovarico viene spesso scoperto in fase avanzata ed è molto difficile da trattare. Questo studio esplora una debolezza sorprendente di questi tumori: la loro dipendenza dalla sintesi di grassi e lipidi. I ricercatori mostrano che spegnere un interruttore chiave della “fabbrica dei grassi” nelle cellule tumorali può sia rallentarne la crescita sia attivare un particolare tipo di morte cellulare, facilitando nel contempo l’attacco del sistema immunitario al tumore.
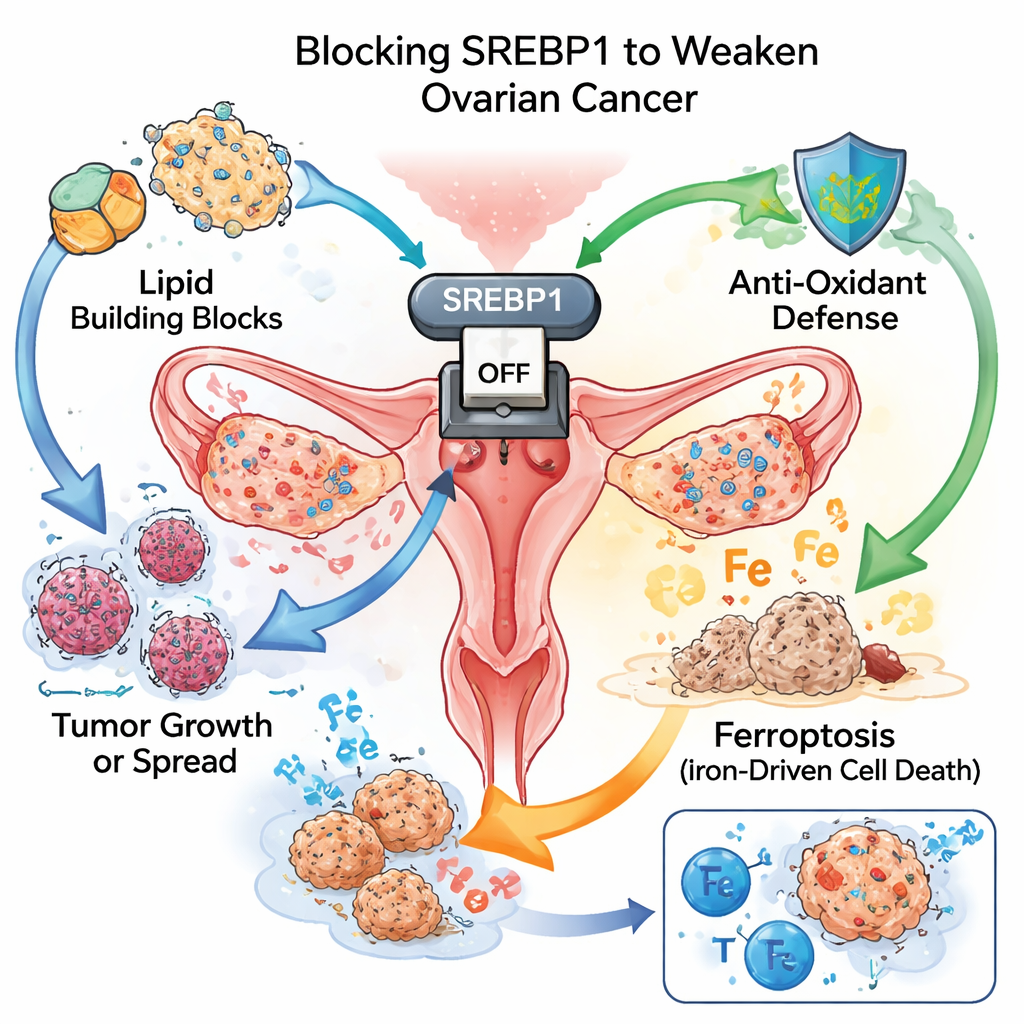
Un interruttore maestro per il carburante tumorale
Come piante infestanti a crescita rapida, le cellule tumorali necessitano di grandi quantità di mattoni e di energia. Un modo per soddisfare questa domanda è riconfigurare la sintesi e l’uso dei lipidi. Il gruppo ha concentrato l’attenzione su SREBP1, una proteina che funge da interruttore maestro per la produzione di grassi. Nei campioni di tessuto di oltre cento pazienti, i tumori ovarici presentavano livelli di SREBP1 molto più alti rispetto ai tessuti normali circostanti. Le donne i cui tumori mostravano una colorazione più intensa di SREBP1 tendevano ad avere una malattia più aggressiva e una sopravvivenza più breve, segnando questa proteina sia come motore della progressione sia come indicatore di esito sfavorevole.
Rallentare crescita e diffusione tagliando i rifornimenti di grasso
Nelle linee cellulari di cancro ovarico coltivate in laboratorio, la riduzione di SREBP1 ha ridotto drasticamente la capacità delle cellule di moltiplicarsi e formare colonie. Le cellule sono rimaste bloccate in fasi specifiche del ciclo cellulare, il che ha impedito loro di dividersi efficacemente. I ricercatori hanno osservato anche minori segnali di movimento e invasione: test di scratch e Transwell hanno mostrato che le cellule con minore SREBP1 migravano meno, e marcatori chiave di un processo di cambio di forma chiamato EMT sono tornati verso uno stato più “normale”. Allo stesso tempo, le misurazioni di trigliceridi e colesterolo sono diminuite e la colorazione ha mostrato meno goccioline lipidiche all’interno delle cellule, confermando che il loro apparato interno di sintesi lipidica era stato ridotto.
Scatenare una morte cellulare alimentata dal ferro
L’effetto più impressionante del blocco di SREBP1 è stato l’attivazione della ferroptosi, una forma di morte cellulare riconosciuta di recente e guidata dal ferro e dalla ruggine, ossia la perossidazione, delle membrane cellulari. Solo un bloccante della ferroptosi, e non gli inibitori di altre vie di morte, è stato in grado di salvare le cellule con SREBP1 silenziato, indicando la ferroptosi come causa principale della loro scomparsa. I test chimici hanno mostrato un aumento dei prodotti di danno derivanti dai lipidi ossidati, una riduzione del glutatione antiossidante e livelli più elevati di molecole lipidiche reattive. Due proteine che normalmente proteggono le cellule dalla ferroptosi, chiamate xCT e GPX4, sono risultate fortemente ridotte quando SREBP1 è stato abbassato, rimuovendo un buffer protettivo cruciale contro questo processo distruttivo.
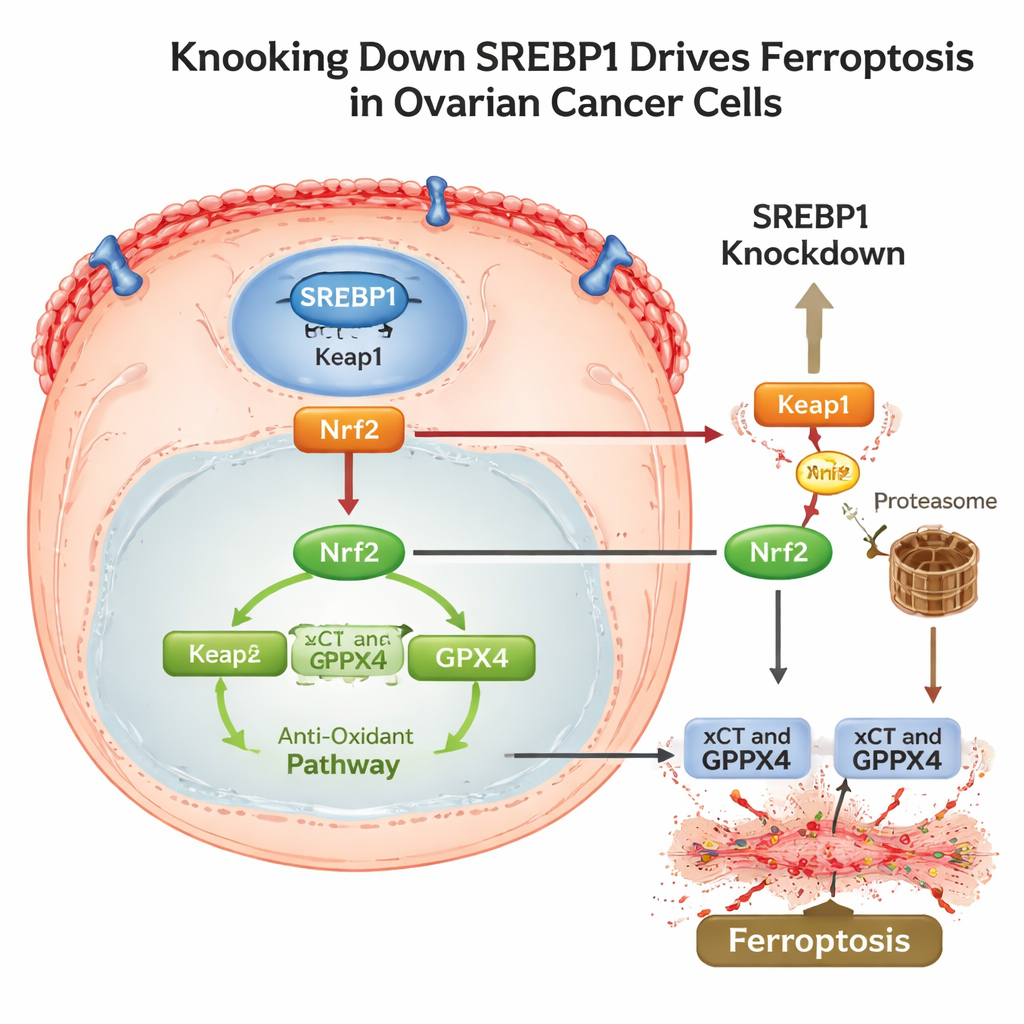
Disarmare lo scudo antiossidante e i trucchi di evasione
Per comprendere come SREBP1 si connetta a questo programma di morte, gli scienziati hanno seguito una via che coinvolge un altro importante proteina di risposta allo stress, Nrf2. In condizioni normali Nrf2 aiuta le cellule a sopravvivere attivando geni antiossidanti, inclusi xCT e GPX4. Lo studio ha rilevato che l’abbassamento di SREBP1 aumentava i livelli di Keap1, una proteina che marca Nrf2 per la degradazione, portando a un maggiore smaltimento di Nrf2 e a meno Nrf2 che raggiunge il nucleo. Con la diminuzione di Nrf2, le difese a valle si indebolivano e seguiva la ferroptosi. È importante che i tumori ricchi di SREBP1 presentassero anche livelli più elevati di PD-L1, una proteina di superficie che aiuta le cellule tumorali a nascondersi dai linfociti T attaccanti. Quando SREBP1 è stato silenziato in tumori di topo, i tumori crescevano più lentamente, mostravano più segni di danno lipidico, meno Nrf2 e GPX4 e livelli inferiori di PD-L1, insieme a un aumento dell’attività immunitaria.
Perché questo è importante per i trattamenti futuri
In termini semplici, i tumori ovarici sembrano usare SREBP1 come uno strumento di sopravvivenza a doppio filo: alimentano la loro crescita aumentando la produzione di lipidi e allo stesso tempo si dotano di uno scudo antiossidante e di un travestimento immunologico. Questo lavoro dimostra che spegnere SREBP1 può affamare il tumore di lipidi, spogliarlo della sua protezione contro il danno indotto dal ferro e ridurne la capacità di sfuggire all’attacco immunitario. Ciò rende SREBP1 un target attraente per nuovi farmaci e suggerisce che combinare inibitori di SREBP1 con trattamenti che inducono la ferroptosi o liberano il sistema immunitario potrebbe offrire ai pazienti un controllo della malattia più efficace e duraturo.
Citazione: Nie, R., Zhou, H., Chen, L. et al. SREBP1 knockdown triggers ferroptosis by suppressing the Nrf2-XCT/GPX4 axis in ovarian cancer. Cell Death Discov. 12, 101 (2026). https://doi.org/10.1038/s41420-026-02964-9
Parole chiave: cancro ovarico, metabolismo dei lipidi, ferroptosi, SREBP1, immunità tumorale