Clear Sky Science · it
PDHA1 aumenta la resistenza alla ferroptosi nel cancro della prostata resistente all'anoikis regolando al rialzo AIFM2
Perché alcune cellule del cancro della prostata si rifiutano di morire
Quando le cellule tumorali si staccano da un tumore e entrano nel flusso sanguigno, la maggior parte dovrebbe morire prima di raggiungere un nuovo organo. Eppure una pericolosa minoranza sopravvive, viaggia e dà origine a metastasi spesso letali. Questo studio pone una domanda chiave: che cosa permette ad alcune cellule del cancro della prostata di resistere a una forma di morte cellulare che normalmente si manifesta quando perdono il contatto con il tessuto d'origine? Svelando un circuito di sopravvivenza nascosto all'interno di queste cellule, la ricerca indica nuovi modi per bloccare le metastasi alla loro fonte.
Fuggire dalla morte nel flusso sanguigno
Per diffondersi, le cellule del cancro della prostata devono sopportare la vita senza il supporto del tessuto circostante, noto come matrice extracellulare. In queste condizioni “staccate”, le cellule normali vanno incontro a una morte programmata chiamata anoikis, e molte cellule tumorali sono anche vulnerabili a un processo correlato guidato dal ferro chiamato ferroptosi. Gli autori hanno creato in laboratorio cellule di carcinoma prostatico resistenti all'anoikis e le hanno confrontate con le cellule “parentali” originali. Hanno scoperto che le cellule resistenti non solo migravano e invadevano in modo più aggressivo, ma sopravvivevano meglio in condizioni di distacco, suggerendo di aver riorganizzato i propri meccanismi interni per evitare la ferroptosi e continuare a crescere.
Un interruttore metabolico con un secondo ruolo
Approfondendo, il gruppo si è concentrato su un enzima metabolico chiamato PDHA1, noto soprattutto per il suo ruolo nella conversione del piruvato derivato dagli zuccheri in acetil-CoA nei mitocondri, alimentando la produzione di energia. Nelle cellule resistenti all'anoikis, i livelli e l'attività di PDHA1 erano marcatamente più alti, e nei campioni dei pazienti si osservava più PDHA1 nei tumori primari di uomini il cui cancro prostatico si era diffuso ai linfonodi o a sedi distanti. Quando i ricercatori riducevano PDHA1, le cellule resistenti perdevano gran parte della loro capacità di muoversi, invadere e sopravvivere. Sorprendentemente, una parte consistente di PDHA1 in queste cellule non era più confinata ai mitocondri; si era trasferita nel nucleo, dove il DNA è impacchettato con gli istoni che possono essere modificati chimicamente per accendere o spegnere i geni.
Riscrivere l'attività genica per bloccare la ferroptosi
All'interno del nucleo, PDHA1 sembrava alimentare la produzione locale di acetil-CoA, un elemento chiave per l'acetilazione degli istoni. Gli autori hanno dimostrato che PDHA1 nucleare aumentava un marcatore specifico, l'acetilazione di H3K9, nella regione di controllo di un gene chiamato PPARA. Questo cambiamento funzionava come un allentamento degli “avvolgimenti” della cromatina, rendendo più facile l'attivazione di PPARA. PPARA, a sua volta, fungeva da interruttore maestro che aumentava la produzione di un'altra proteina, AIFM2, legandosi al suo promotore e innalzandone la trascrizione. Piuttosto che agire direttamente sul gene AIFM2, PDHA1 operava dunque attraverso PPARA, stabilendo un percorso a più tappe dal metabolismo alterato alla regolazione genica modificata.
Costruire uno scudo contro il danno indotto dal ferro
AIFM2 è noto come un freno interno alla ferroptosi: aiuta a proteggere i lipidi nelle membrane cellulari dall'ossidazione distruttiva. Nelle cellule resistenti del carcinoma prostatico, l'aumento di PDHA1 innalzava i livelli di AIFM2, mentre la diminuzione di PDHA1 li riduceva. Test funzionali hanno mostrato che ridurre PDHA1 intensificava i segni caratteristici della ferroptosi—più specie reattive dell'ossigeno, maggiore danno ai lipidi, potenziale di membrana mitocondriale più basso e tipico restringimento mitocondriale—soprattutto quando le cellule erano esposte al farmaco induttore di ferroptosi erastin. La sovraespressione di AIFM2 invertiva questi effetti, salvando la sopravvivenza cellulare in coltura e ripristinando le metastasi polmonari nei topi, anche quando PDHA1 era soppresso. Ciò confermava che AIFM2 è un effettore a valle critico della resistenza alla ferroptosi guidata da PDHA1.
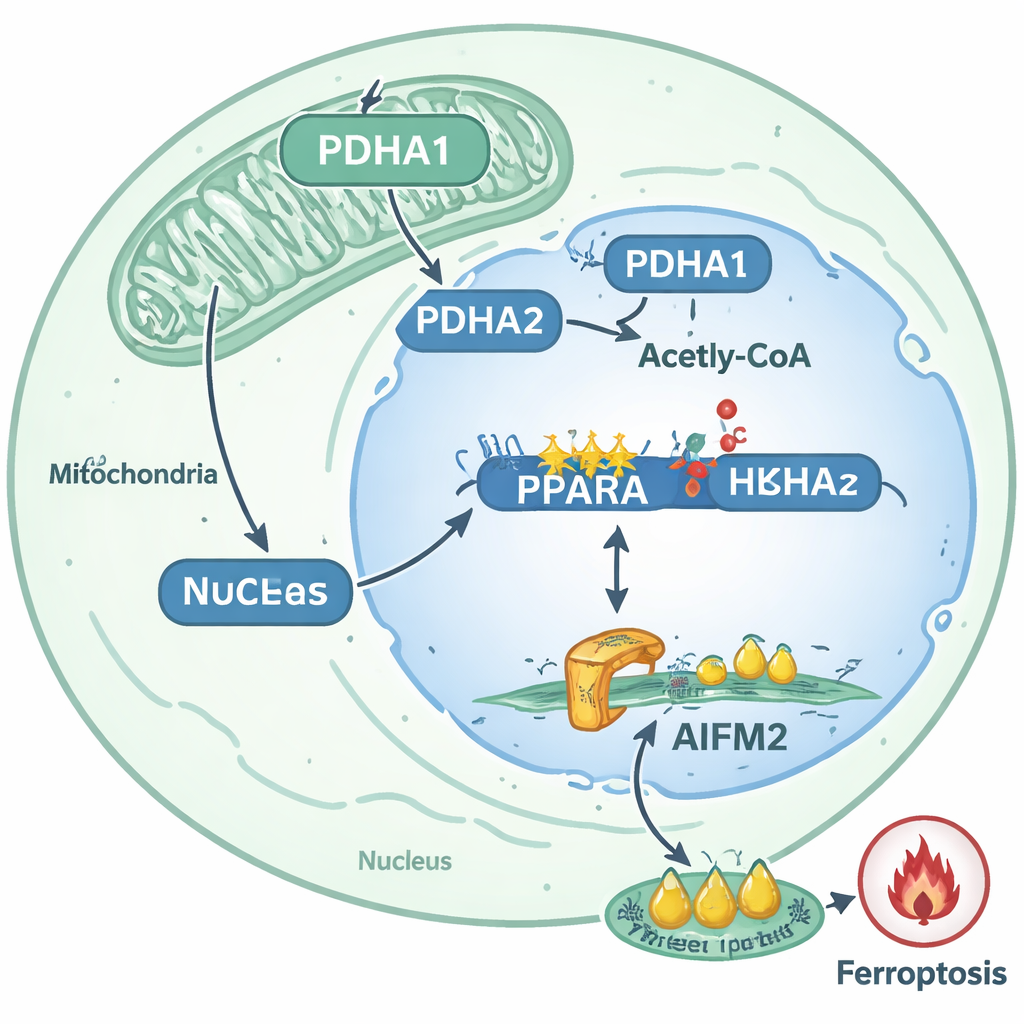
Dal circuito molecolare alle idee terapeutiche
Mappando questi eventi, lo studio delinea una via chiara con cui le cellule prostatiche staccate diventano più difficili da uccidere: PDHA1 si sposta nel nucleo, aumenta l'acetilazione degli istoni nel gene PPARA, potenzia l'attività di PPARA e così innalza i livelli di AIFM2 per bloccare la ferroptosi. Questa via è fortemente correlata al comportamento metastatico nei tumori dei pazienti e nei modelli animali. Per i non specialisti, la conclusione è che certe cellule tumorali riadattano un comune enzima metabolico come strumento epigenetico che riorganizza l'attività genica e costruisce uno scudo biochimico contro una potente forma di morte cellulare. Gli autori suggeriscono che farmaci che prendono di mira PDHA1, PPARA o AIFM2—o terapie che inducano intenzionalmente la ferroptosi—potrebbero un giorno essere combinati per privare le cellule metastatiche del cancro della prostata di questo vantaggio di sopravvivenza e renderle molto più vulnerabili durante il loro viaggio più critico: il salto da un organo a un altro.
Citazione: Cong, Y., Chen, K., Ju, Y. et al. PDHA1 enhances resistance to ferroptosis in anoikis-resistant prostate cancer by upregulating AIFM2. Cell Death Discov. 12, 105 (2026). https://doi.org/10.1038/s41420-026-02958-7
Parole chiave: metastasi del cancro della prostata, ferroptosi, resistenza all'anoikis, PDHA1, AIFM2