Clear Sky Science · it
La DNA polimerasi kappa stabilizzata da Ptbp2 interagisce con MRE11 e promuove l’instabilità genomica nella leucemia
Come le cellule leucemiche mantengono il DNA rotto e continuano a sopravvivere
Il nostro DNA è costantemente sotto attacco, eppure le cellule sane sono di solito molto efficaci nello scoprire e riparare i danni. Nella leucemia, però, alcune cellule imparano a convivere con un DNA rotto e instabile—e talvolta trasformano quell’instabilità in un vantaggio per la sopravvivenza. Questo studio svela una “alleanza” molecolare tra una proteina dello splicing (Ptbp2), un enzima speciale che copia il DNA (DNA polimerasi kappa, o Polk) e un fattore sensore del danno (MRE11) che aiuta le cellule leucemiche a riparare abbastanza danno da restare in vita, accumulando però il caos genetico che guida la progressione del tumore.
Un aiutante nascosto nelle cellule leucemiche
I ricercatori si sono concentrati sulla leucemia mieloide cronica (CML), un tumore del sangue solitamente guidato dal gene di fusione BCR::ABL1. Mentre i farmaci moderni che bloccano BCR::ABL1 funzionano bene nelle fasi iniziali della malattia, molti pazienti che arrivano alla fase aggressiva detta “blast crisis” rispondono male. Studi precedenti avevano mostrato che Ptbp2, una proteina che lega l’RNA e influenza l’elaborazione degli mRNA, è potenziata da BCR::ABL1 e si comporta come un oncogene nella CML. Qui il team ha scoperto che Ptbp2 si lega alla porzione terminale (3′ UTR) dell’mRNA di Polk e lo protegge dalla degradazione. Di conseguenza, le cellule leucemiche producono più proteina Polk quando i livelli di Ptbp2 sono elevati.
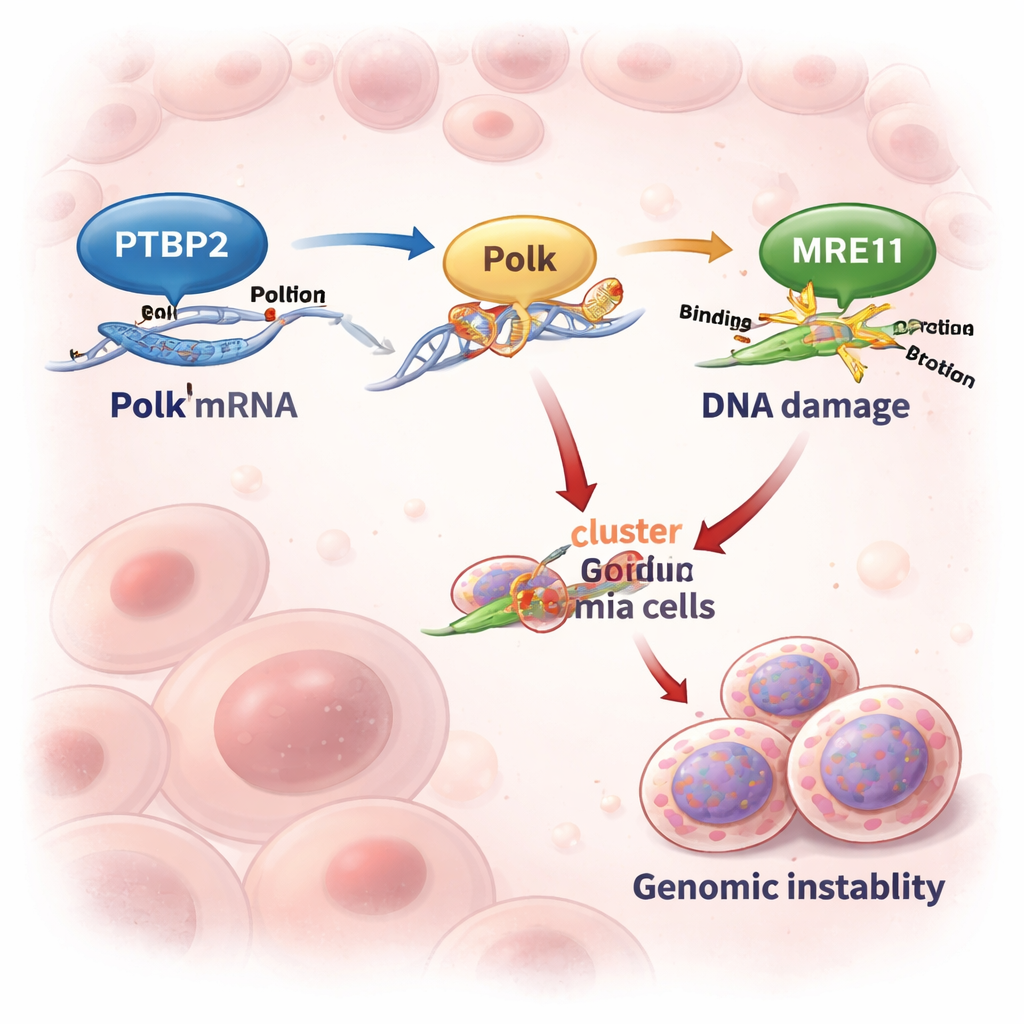
Attivare una macchina di copia del DNA incline agli errori
Polk è una DNA polimerasi “di riserva” che può copiare sopra DNA danneggiato quando la normale macchina di replicazione si blocca. Questa capacità può salvare cellule sotto stress—ma ha un costo, perché Polk è propensa agli errori e può introdurre mutazioni. In linee cellulari e campioni di pazienti con CML avanzata, i livelli di Ptbp2 e Polk aumentavano e diminuivano insieme. Quando gli scienziati hanno eliminato Ptbp2 nelle cellule leucemiche, i livelli di Polk sono calati bruscamente e l’RNA di Polk è decaduto quasi il doppio più rapidamente. Reintrodurre Polk in cellule prive di Ptbp2 ha ripristinato il fenotipo, dimostrando che il ruolo principale di Ptbp2 qui è mantenere Polk abbondante e attivo.
Riparare il danno—ma non perfettamente
Per valutare come questa coppia influenzi la riparazione del DNA, i ricercatori hanno trattato le cellule con idrossiurea, un farmaco che arresta la replicazione del DNA e viene spesso usato nei pazienti con CML. Le cellule prive di Ptbp2 hanno accumulato molto più danno al DNA, visibile come lunghe “code di cometa” e foci γH2AX intensi—segni caratteristici di cromosomi rotti. Queste cellule danneggiate erano più propense ad andare incontro alla morte. Al contrario, le cellule con alti livelli di Ptbp2 e Polk tolleravano meglio il farmaco, riparavano il danno in modo più efficiente e sopravvivevano, anche se la riparazione era approssimativa. La sovraespressione di Polk in cellule knock-out per Ptbp2 ha annullato questa sensibilità, confermando che la partnership Ptbp2–Polk aiuta le cellule leucemiche a superare lo stress da replicazione ed evitare l’apoptosi.
Una rete di risposta al danno del DNA che favorisce l’instabilità
La storia non finisce con Polk. Il team ha dimostrato che Polk interagisce fisicamente con MRE11, un componente chiave del complesso MRN che rileva le rotture del DNA e attiva la via di risposta al danno ATM–CHK2. Quando Ptbp2 è stato rimosso, Polk è diminuito, i livelli e l’attività di MRE11 sono calati e la segnalazione ATM–CHK2 si è indebolita. Ripristinare Polk ha riportato MRE11 e la sua attivazione. Esperimenti dettagliati con fibre di DNA hanno rivelato che Ptbp2 e Polk aiutano a proteggere le forcelle di replicazione bloccate dall’essere erose, in gran parte tramite MRE11. Bloccare MRE11 con un farmaco ha compromesso questa protezione delle forcelle e aumentato il danno al DNA. Paradossalmente, le cellule con segnalazione attiva Ptbp2–Polk–MRE11 hanno accumulato più anomali cromosomiche, come scambi tra cromatidi fratelli, rotture, gap, fusi multipolari e cellule giganti multinucleate—segni classici di instabilità genomica che possono alimentare una forma di cancro più aggressiva.
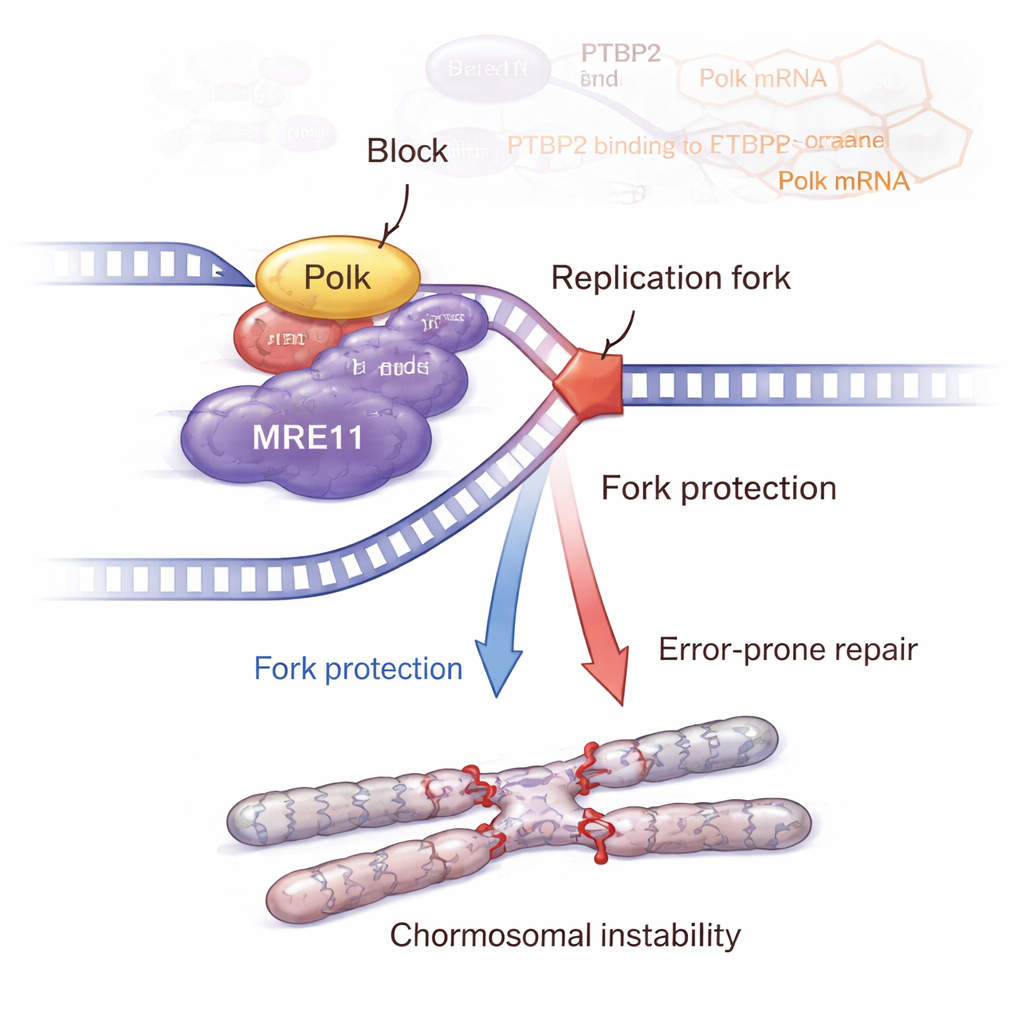
Dai topi a possibili nuovi trattamenti
Nei modelli murini, le cellule leucemiche con Ptbp2 intatto hanno generato tumori più grandi e più anomali rispetto a cellule prive di Ptbp2. I tessuti di questi topi mostravano livelli più alti di Ptbp2, Polk, del marcatore di proliferazione Ki-67 e strutture di divisione cellulare distorte. In un modello murino simile alla CML guidato da BCR::ABL1, l’aggiunta di Ptbp2 ha aumentato Polk e il numero di cellule in divisione atipiche e di ammassi leucemici invasivi nella milza e nel fegato, indicando una progressione più rapida della malattia. Insieme, questi risultati suggeriscono che l’asse Ptbp2–Polk–MRE11–ATM–CHK2 permette alle cellule leucemiche di sopravvivere a intensi stress del DNA mentre accumulano progressivamente mutazioni dannose.
Perché questo conta per i pazienti
Per un pubblico non specialistico, il messaggio chiave è che alcune cellule leucemiche sfuggono al controllo camminando su una fune: riparano il DNA quanto basta per restare vive, ma non così bene da evitare le mutazioni. Ptbp2 stabilizza Polk, che poi si associa a MRE11 per proteggere il DNA stressato e mantenere attivi i segnali di danno—eppure questa riparazione è imperfetta e favorisce il caos genetico. Poiché la CML avanzata e altri tumori sembrano dipendere da questo equilibrio precario, mirare a Ptbp2 o al suo controllo su Polk potrebbe spingere le cellule lontano dalla sopravvivenza verso l’autodistruzione, offrendo un nuovo e promettente approccio terapeutico, soprattutto nella difficile fase di blast crisis.
Citazione: Lama, S., Barik, B., IS, S. et al. DNA polymerase kappa stabilized by Ptbp2 interacts with MRE11 and promotes genomic instability in leukemia. Cell Death Discov. 12, 96 (2026). https://doi.org/10.1038/s41420-026-02951-0
Parole chiave: leucemia mieloide cronica, instabilità genomica, riparazione del DNA, DNA polimerasi kappa, PTBP2